您还不是认证园区!
赶快前去认证园区吧!

5月18日,CDE官网显示浙江医药注射用重组人源化抗HER2单抗-AS269偶联物(ARX788)获CDE拟突破性疗法认定并开始公示,拟用于HER2阳性晚期乳腺癌二线治疗。


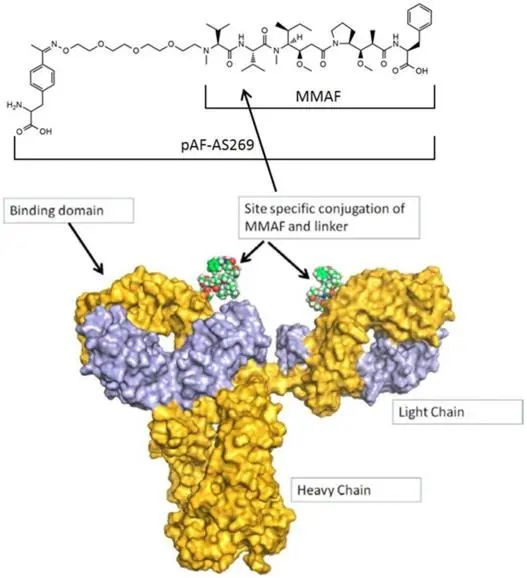
ARX788是浙江医药于2013年6月14日与美国Ambrx(安博生物)签署《合作开发和许可协议》合作研发的新一代新型位点特异性抗体偶联药物(ADC),包含一个靶向HER2的单抗(曲妥珠单抗)、两个细胞毒性有效载荷AS269。中间的linker是能够与曲妥珠单抗重链特异性结合位点连接的非天然氨基酸,AS269可在水溶液中通过单步共轭反应共价偶联于非天然氨基酸。
2020年12月Ambrx公司在圣安东尼奥乳腺癌研讨会(SABCS)上公布了ARX788的最新临床结果。在中国进行的I期HER2阳性乳腺癌试验中,ARX788 1.5mg/kg剂量组的ORR为74% (14/19),DCR为100%。在美国和澳大利亚开展的I期HER2阳性泛肿瘤试验中,ARX788 1.5mg/kg剂量组ORR为67% (2/3),DCR为100%。RX788耐受性良好,大多数不良事件为轻中度,且可控。
ARX788已于2019年12月获国家药监局批准开展治疗 HER2 阳性局部晚期或转移性乳腺癌临床研究,于今年2月25日获国家药监局批准开展治疗胃癌和胃食管连接部腺癌的II/III 期临床试验。3月17日ARX788获FDA治疗胃癌的孤儿药资格认定。

点亮“在看”,好文相伴



 个人中心
个人中心
 我是园区
我是园区




