针对儿童近视!兆科眼科引进的眼科新药在中国启动3期临床,拟入组526人
收藏
关键词:
临床期临床
资讯来源:医药观澜 + 订阅账号
发布时间:
2022-02-17
▎药明康德内容团队报道
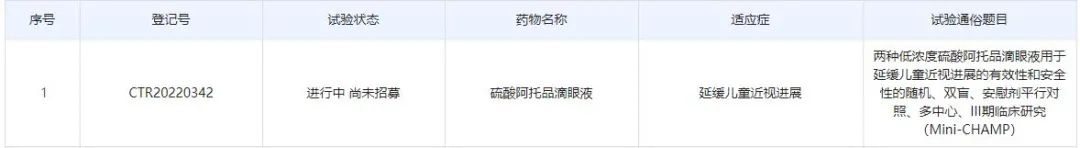
今日(2月17日),中国药物临床试验登记与信息公示平台显示,兆科眼科公司已启动一项硫酸阿托品滴眼液(NVK-002)用于延缓儿童近视进展的3期临床试验,计划在中国境内入组526例患者。公开资料显示,NVK-002由兆科眼科从Nevakar公司引进,全球范围内已进入3期临床试验阶段。
近视已成为全球的公共卫生问题之一。研究表明,儿童近视进展可能与聚焦疲劳有关。对于儿童青少年近视的防控,低浓度阿托品已被公认为是一种持续有效的药物。阿托品为一种抗胆碱药物,可阻断中枢神经系统以及周围神经系统中神经递质的作用,通过禁用聚焦机制来控制近视加深。
然而,低浓度阿托品存在不稳定性的缺点,这是此类药物长期以来面临的一个药物开发挑战。
因此,研究人员正在开发一些新型的阿托品药物,以期在保证安全性、有效性及依从性的同时,也能降低低浓度阿托品的降解速度,进而可以实现长期储存。
NVK-002是由Nevakar公司开发的一种无菌、无防腐剂的低浓度阿托品滴眼液,拟开发用于控制儿童及青少年的近视进展。2020年10月,兆科眼科与Nevakar公司达成合作,获得了NVK-002在大中华区、韩国及若干东南亚国家和地区的独家开发和商业化许可权。
根据兆科眼科早前发布的资料,NVK-002的专有剂型成功解决了低浓度阿托品的不稳定性问题,预期有效期至少为24个月。此外,由于NVK-002不含防腐剂,因此可以避免由防腐剂引起的灼伤及部分眼表疾病等副作用。
目前,Nevakar公司正在美国及欧洲开展一项名为CHAMP的3期临床试验,以评估NVK-002在控制儿童及青少年近视进展方面的疗效及安全性。根据兆科眼科之前发布的公告,CHAMP临床试验初步安全性报告显示,NVK-002的耐受性良好,且并无发现新的重大安全性问题。
根据中国药物临床试验登记与信息公示平台,兆科眼科本次在中国启动的是一项名为Mini-CHAMP的随机、双盲、安慰剂平行对照、多中心3期临床试验,旨在评估两种低浓度硫酸阿托品滴眼液(0.01%和0.02%)用于延缓儿童近视进展的有效性和安全性。研究的主要终点是0.02%阿托品对比安慰剂在M12(治疗12个月)访视时近视进展(SER)小于-0.50D的受试者比例的组间差异。该研究将在中国18个临床试验中心召开,计划入组526例患者。

图片来源:123RF
值得一提的是,此前,兆科眼科已在中国启动了另外一项名为China-CHAMP的3期临床,以评估两种低浓度硫酸阿托品滴眼液(0.01%和0.02%)对比安慰剂用于延缓儿童近视进展的有效性和安全性。该试验的主要研究终点是:在M24(治疗24个月)访视时,0.02%阿托品对比安慰剂睫状肌麻痹后,电脑验光等效球镜度数较基线变化值的组间差异。这项研究计划在中国境内入组770例患者,目前正在进行中。
希望这款硫酸阿托品滴眼液的后续临床研究顺利进行,并取得好的结果,早日为患者带来新的选择。
[1] 中国药物临床试验登记与信息公示平台.Retrieved Feb 17,2022, from http://www.chinadrugtrials.org.cn/clinicaltrials.searchlistdetail.dhtml
[2]兆科眼科招股章程..Retrieved Apr 27, 2021, from https://www1.hkexnews.hk/listedco/listconews/sehk/2021/0416/2021041600010_c.pdf
本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。









 个人中心
个人中心
 我是园区
我是园区




