
撰文 | 雪月
肿瘤相关基因突变会产生抗原,可以激活细胞毒性CD8+T细胞
(cytotoxic T lymphocytes CTLs)
。但是在肿瘤中CTL通常是处于抑制状态,出现功能失调的衰竭状态。尽管靶向PD-1和PD-L1可以增强肿瘤引流淋巴结内的CTL活性而成功提高了肿瘤治疗效果,但是在肿瘤中如何诱导T细胞耗竭还知之甚少,而且T细胞耗竭在抗PD-1/PD-L1疗法中并未得到逆转。
单核吞噬细胞包括单核细胞、巨噬细胞和树突状细胞,可以参与固有免疫以及作为抗原递呈细胞启动和调节适应性免疫应答。树突状细胞
(dendritic cell
DC
)
可以捕获肿瘤组织中的抗原并迁移到淋巴结激活特异性T细胞。DC包含有DC1和DC2,DC1主要由IRF8分化决定,可以将外源性抗原呈递给CTL,而DC2依赖于IRF4调节CD4+T细胞。在多种肿瘤模型中,DC1的缺失会损伤CTL的启动。
2022年10月25日,来自纪念Sloan-Kettering癌症中心和康奈尔大学的李明
(Ming O. Li)
团队在Immunity 上发表题为
Tumor-associated macrophages expressing the transcription factor IRF8 promote T cell exhaustion in cancer
的文章。该文章
揭示了肿瘤相关巨噬细胞受到IRF8调控,产生DC样特点,递呈肿瘤抗原促进CD8+T细胞功能耗竭。
作者首先在MMTV-PyMT
(PyMT)
乳腺癌模型中检测单核吞噬细胞系统的变化,分析发现肿瘤组织中驻留的肿瘤相关巨噬细胞数量增加,而DC1比例减少,DC2无明显变化。大部分的DC1会表达与成熟和迁移到次级淋巴结相关的标志物CD103。对各个细胞群进行转录组分析表明肿瘤相关巨噬细胞与DC具有共同的特征,而单核细胞、乳腺组织巨噬细胞的特征与肿瘤相关巨噬、DC1以及DC2不同。
为了探究从ly6C+单核细胞分化而来的肿瘤相关巨噬细胞是否受到细胞内在转录程序的调控,作者对比了单核细胞、乳腺组织巨噬细胞以及肿瘤相关巨噬细胞中转录因子的差异表达,并重点关注了调控多种细胞命运决定的IRF家族。作者发现IRF4和IRF8在乳腺组织巨噬细胞和肿瘤相关巨噬细胞中表达模式相反,IRF8在肿瘤相关巨噬细胞中高表达。为了验证IRF8这种表达模式,作者用IRF8-EGFP乳腺癌小鼠模型进行检测,发现肿瘤相关巨噬细胞确实表达的EGFP水平高于单核细胞和乳腺组织巨噬细胞,DC1也会表达更高水平的EGFP。
接下来作者用CD11cCreIrf8fl/fl PyMT小鼠
(可以同时敲除DC和肿瘤相关巨噬中的IRF8)
来分析IRF8对于肿瘤相关巨噬细胞和DC1的影响。分析表明肿瘤DC1数量明显下降,肿瘤相关巨噬细胞的扩增和成熟受到破坏。虽然作者检测到CTL也明显受损,但是肿瘤的生长与对照组无明显区别。作者分析了从CD11cCreIrf8fl/fl PyMT小鼠中分离而来的肿瘤相关巨噬细胞的转录组特征,结果验证了IRF8可以驱动肿瘤相关巨噬中的DC样属性特点,IRF8激活肿瘤相关巨噬细胞的基因表达程序,这些程序与DC共享,促进抗原获取和呈递以及与T细胞相互作用。IRF8介导了肿瘤相关巨噬细胞呈递肿瘤抗原并诱导CTL表达PD-1。
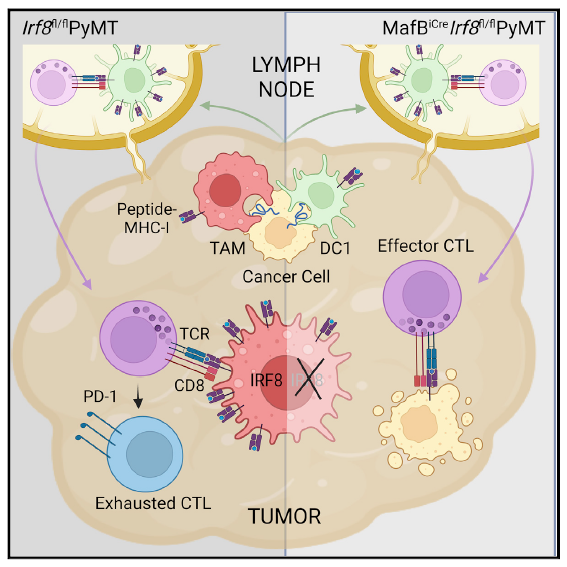
为了探究IRF8在肿瘤相关巨噬细胞的体内效应,作者用MafBiCreIrf8fl/fl PyMT小鼠
(可以特异性敲除单核、肿瘤相关巨噬、乳腺组织巨噬中的IRF8)
进行接下来的研究。分析发现相较于对照组小鼠,肿瘤生长在敲除组小鼠中受到抑制。对比与CD11cCreIrf8fl/fl PyMT小鼠中各个细胞比例的变化,作者总结发现DC1对于肿瘤特异性CD8+T细胞的启动是必需的,CD8+T细胞在肿瘤中会被表达IRF8的肿瘤相关巨噬呈递抗原,促进T细胞耗竭,减弱抗肿瘤免疫反应。最后作者在多种人肿瘤中验证了IRF8依赖的肿瘤相关巨噬也能够促进CD8+T细胞耗竭。
本研究揭示了转录因子IRF8在肿瘤相关巨噬细胞中的重要作用,探究了其对于促进CD8+T细胞耗竭的重要贡献。对于IRF8相关肿瘤巨噬细胞在抗PD-1肿瘤治疗中的作用还有待研究。
原文链接:
https://doi.org/10.1016/j.immuni.2022.10.002
制版人:十一

【原创文章】BioArt原创文章,欢迎个人转发分享,未经允许禁止转载,所刊登的所有作品的著作权均为BioArt所拥有。BioArt保留所有法定权利,违者必究。











 个人中心
个人中心
 我是园区
我是园区





