新领医药刘昆│技术之外的那些事--研发公司的客户沟通与服务
收藏
关键词:
那些医药研发药
资讯来源:医药前途汇 + 订阅账号
发布时间:
2020-08-21


▎大会还有部分展位、路演名额可合作,如有商务合作意向请咨询前途汇工作人员。

北京站展位号:F05

届时,新领先常务副总裁刘昆先生将做“技术之外的那些事——研发公司的客户沟通与服务”的主题发言,建立在一致性评价技术要求基础上的研发工作,非常主要的一个关键词就是“产业化”。围绕产业化的相关研究工作(包括技术与注册等),需要研发单位与药企进行充分沟通、密切配合才能够达成。
在合作过程中,影响项目开发进度与质量的,很大一部分并不是技术因素,而是沟通因素。高效沟通能够极大地提高项目达成率与成功率。在新形势下,药企与研发单位,建立战略合作伙伴关系,是最安全有效的合作方式。
讲者将根据本公司多年积累的经验,并结合行业的发展情况,对上述内容进行解读和交流。
北京新领先医药科技发展有限公司
为国内最大的全产业链CRO公司之一。公司成立于2005年1月,注册资本9155.42万元,于2015年通过重组实现主板上市(股票代码:600222)。创建十六年以来,北京新领先在药学研究、临床CRO研究、IVIVR体内外桥接研究和药品进出口注册等领域,一直处于行业领先地位,并连续四年(2017-2020年)被评为“中国医药研发公司10强”(2020年位居榜首)。
目前,公司已经和国内外300多家医药企业建立起了合作关系,成功承接了400个余项仿制药品种的药学研发、近500个项目的临床研究,申请专利近100项,获得授权近50项。
2020年,新领先依托既有的技术和管理团队,整合郑州临空生物园平台,全面入资,建设并运营了六大技术平台,包括新药筛选及检测平台、药物评价平台(动物房)、大分子中试及商业化生产服务平台(大分子CDMO)、小分子CMC研究及商业化生产服务平台(小分子CDMO)、细胞治疗技术服务平台和临床CRO服务平台,覆盖临床前及CMC研发、委托加工、临床CRO、申报注册及MAH委托质量管理等药品生命全周期,为全球客户提供真正意义上的一站式服务。
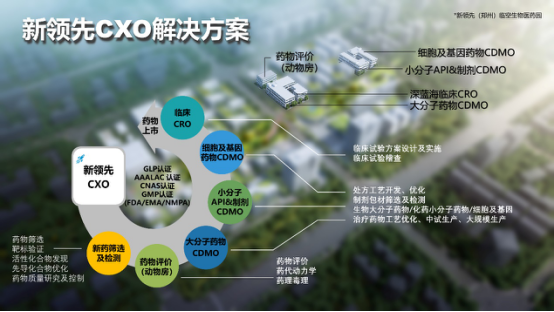
(1)新药筛选及检测平台
新药筛选及检测平台是医药研发和创新的基础。建立配备HPLC、UPLC、GC/GC-MS、LC-MS、ICP-MS、TGA、溶出仪、核磁等先进大型精密仪器设施的高标准研发实验室。为新药实验开发提供有力保障。
服务内容:
高通量药物筛选、活性化合物发现、靶标验证、先导化合物优化、临床前候选药物选择等技术研发服务,并以数据库支持整个体系运转,大幅度地缩短新药发现的时间,增加高特异性、高活性药物的发现率,促使新药流程快速进入候选物的确定和新药临床研究,有效帮助客户控制新药开发成本。
(2)药物评价平台(动物房)
药物评价平台(动物房)按照国际化标准设计建造,平台共5层,总建筑面积4920.75m2,能够满足AAALAC、中国GLP、CNAS要求。
服务内容:
药物发现、化学合成、生物分析、PKPD模型拟合、大分子药、临床申报、毒性毒理、药代动力学、药效学以及细胞/基因治疗药物体内外药效评价、DMPK等。
(3)大分子中试及大规模生产服务平台
大分子中试及大规模生产服务平台共4层,总建筑面积11453 m2,符合美国FDA、欧盟EMA和中国NMPA GMP标准,旨在为生物大分子药物提供研发生产一体化CDMO服务。
服务内容:
稳定细胞系筛选、中试发酵工艺、大规模培养工艺及大分子纯化工艺开发服务,抗体药物、重组蛋白药物、蛋白疫苗中试和大规模生产服务,生物大分子药物制剂的生产技术服务,支撑产品在中、美、欧等地同时进行临床试验并快速上市,实现客户的研究成果全球同步转化。
(4)小分子CMC制剂研究生产平台
北京中关村高新技术园区拥有9000平米研发实验室,近800人的研发团队,配备160余台高效液相、50余台溶出仪、LC-MS/GC-MS等30余台大型精密检测仪器以及压片机、流化床、冻干机、呼吸模拟机、药用多级撞击器(NGI)等工艺设备。
郑州小分子CMC制剂研究生产平台总建筑面积6651.54m2,符合美国FDA、中国NMPA GMP标准,具有面向国际市场服务能力的小分子制剂研究、临床样品生产及商业化生产能力。
服务内容:
难溶性药物解决方案、常规口服和注射给药剂型的中试试验(片剂、胶囊、颗粒剂、小容量注射液、口服溶液等)、临床样品生产及商业化生产服务,支撑创新药企、MAH持有人及仿制药研发公司进行创新药研发、仿制药一致性评价和研发申报。
(5)细胞技术服务平台
细胞技术服务平台总建筑面积6651.54m2,符合美国FDA、欧盟EMA和中国NMPA GMP标准,可满足细胞与基因治疗药物的小试、中试及商业化生产需要。
服务内容:
细胞与基因治疗药物(质粒、病毒、细胞药物形式)全流程CDMO服务——小试、中试、临床前研究、IND注册申报、临床试验及商业化药品生产,干细胞免疫细胞存储,专项质量检测指标的开发和检测,并可为医疗机构、研发机构等提供质粒、慢病毒载体的现货供应及细胞制剂的制备服务。
(6)临床CRO服务平台
临床CRO平台具有ICH-GCP临床研究质量管理体系和标准操作规程(SOP),通过ISO9001质量标准认证,拥有 300 余人高专业水准的临床服务团队,在全国20多个中心城市设立分公司管理模式的驻地办事处。已经与国内400 多家GCP医院建立了合作,并与其中 80 余家医院有 5 年以上合作关系。通过创新的服务模式和多维的信息化技术,推动临床研究的发展及临床研究外包服务模式的变革。全面覆盖大小分子药物、满足不同需求研发型企业的临床研究。
服务内容:
创新药和仿制药的Ⅰ~Ⅳ期临床试验、仿制药生物等效性(BE)试验及药代动力学(PK/PD)临床研究、体内外相关性研究(IVIVR)、医疗器械临床研究及第三方稽查等,为国内外客户打通新药上市前关键瓶颈。

电话:86-10-61006450



 点击“阅读原文”查看2020年线下会议安排!
点击“阅读原文”查看2020年线下会议安排!












 点击“阅读原文”查看2020年线下会议安排!
点击“阅读原文”查看2020年线下会议安排!


 个人中心
个人中心
 我是园区
我是园区




