您还不是认证园区!
赶快前去认证园区吧!
2020年11月,安进公司(Amgen)已通知百济神州,其为双方合作中涵盖的管线药物在中国开展临床研究而向中国国家人类遗传资源管理(HGRAC)递交的相关申报目前将延迟,其中包括同类第一在研KRAS G12C抑制剂sotorasib(AMG 510)的申报项目。

2020年4月底开始获批开始第一项临床,但是关键还要看遗传办

在中国,涉及人类遗传资源信息采集的临床试验必须获得HGRAC许可才能开展。在安进公司等待HGRAC进一步信息的同时,百济神州和安进公司将继续就这些临床试验的开展进行准备工作。除与安进公司合作中涵盖的管线药物外,百济神州候选药物在中国开展临床试验预计将不会受到影响。估计Amgen受到监管,核查中,🍵。在中国必须遵守中国法律法规,按需申报。
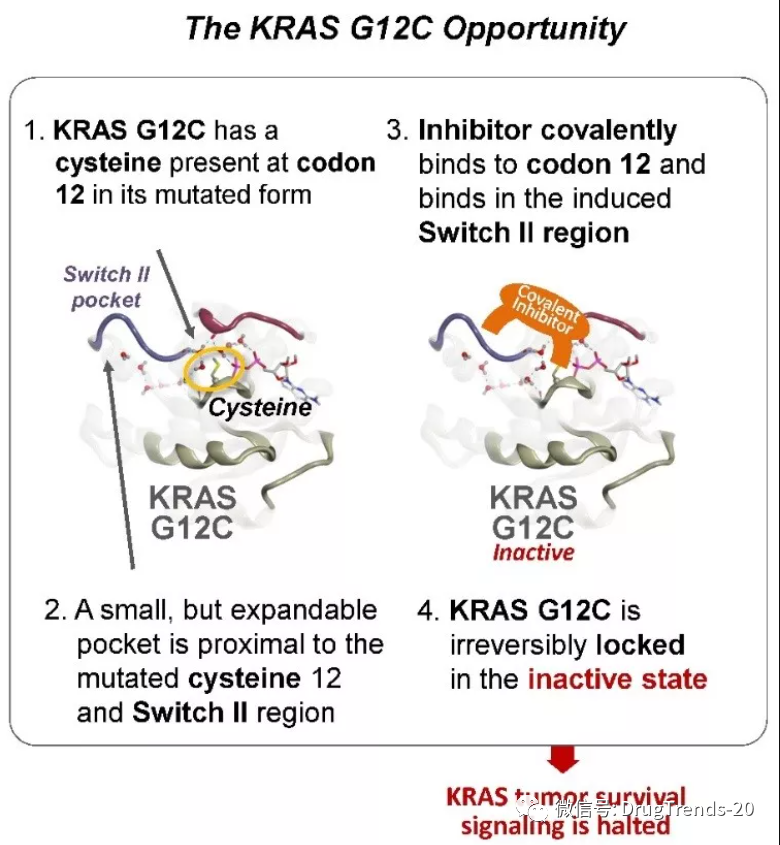
2020年12月16日,安进宣布向美国FDA递交Sotorasib的新药上市申请,用于治疗KRAS G12C突变的晚期转移性非小细胞肺癌。此前,FDA已经授予Sotorasib突破疗法认证资格,并采取实时审评(RTOR)以加快审评进度。




 个人中心
个人中心
 我是园区
我是园区




