6月8日,中国国家药监局(NMPA)官网最新公示,贝达药业递交的1类新药伏罗尼布片的上市申请已获得批准,与依维莫司联合,用于既往接受过酪氨酸激酶抑制剂(TKI)治疗失败的晚期肾细胞癌患者
。公开资料显示,这是一款具有全新化学结构的新一代多靶点激酶抑制剂。根据贝达药业此前发布的新闻稿,伏罗尼布也是贝达药业申报的首个非肺癌适应症新药,它的获批意味着该公司向肺癌之外的其它癌症领域迈出一大步。

截图来源:NMPA官网
肾细胞癌是常见的一种肾癌类型,约占肾癌总数的90%,在55~74岁的男性中尤为普遍。不少局部肾细胞癌初次手术治疗后会发生转移。转移性疾病患者的预后较差,5年生存率约为13%。
伏罗尼布(CM082,vorolanib)是贝达药业在研的新一代多靶点激酶抑制剂。它针对VEGFR、PDGFR、c-Kit、Flt-3、CSF1R等多靶点具有抗血管生成的明显疗效,并且能够满足靶点的特殊药代动力学/药效动力学(PK/PD)要求,达到保留活性、降低毒性的目的。公开资料显示,伏罗尼布自获批临床以来,已开展了多项临床研究以支持其治疗肾细胞癌的新药上市申请。
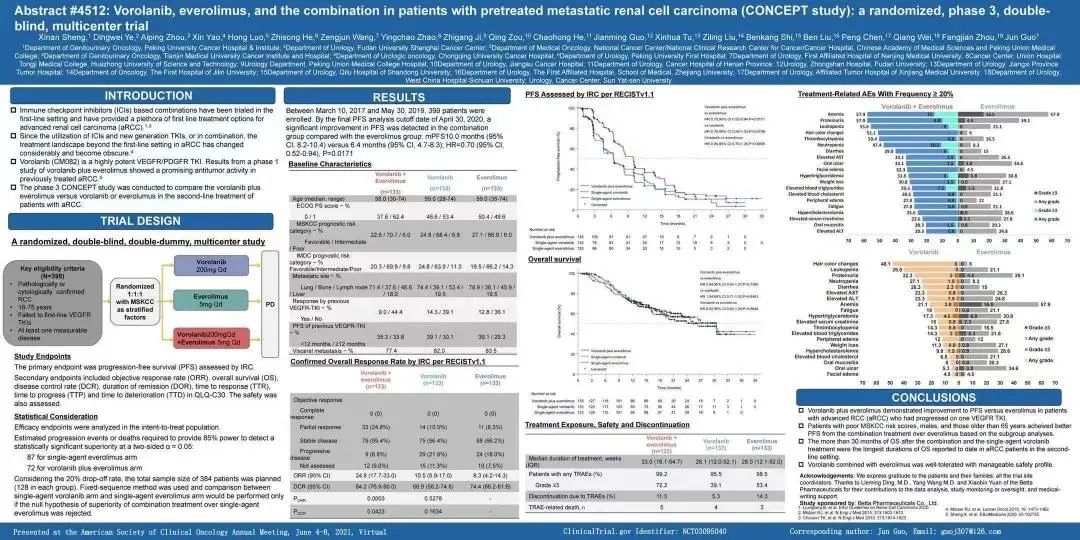
其中,伏罗尼布的2/3期注册性临床试验(CONCEPT研究)由北京肿瘤医院郭军教授牵头,中国共计36家医院共同参加。该研究目的是评估伏罗尼布联合依维莫司治疗肾癌患者的疗效和安全性,共399例患者随机接受伏罗尼布+依维莫司、伏罗尼布单药或依维莫司单药治疗,每组133例。该研究结果已在2021年美国临床肿瘤学会(ASCO)年会上公布。
数据显示,伏罗尼布+依维莫司联合治疗组中位无进展生存期(PFS)达到10.0个月,明显长于依维莫司单药组的6.4个月;伏罗尼布单药组与依维莫司单药组PFS没有差异,中位PFS均为6.4个月。133例接受伏罗尼布+依维莫司联合治疗的患者中,33例(24.8%)获得客观反应,该数据在伏罗尼布单药组与依维莫司单药组分别为14例(10.5%)和11例(8.3%)。在安全性方面,三组患者分别有132例、127例和131例发生治疗相关不良事件(TRAE),其中联合用药组最常见的TRAE是蛋白尿和贫血。
▲CONCEPT研究结果(图片来源:参考资料[3])
CONCEPT研究结果显示,与依维莫司单药相比,伏罗尼布联合依维莫司对转移性肾癌患者有PFS获益,且具有安全耐受性。
除了肾细胞癌,贝达药业还在开展伏罗尼布治疗其它适应症的临床试验,包括继发于病理性近视的脉络膜新生血管(mCNV)、湿性年龄相关性黄斑变性(w-AMD)、急性髓系白血病等。
[1]国家药监局批准伏罗尼布片上市.Retrieved Jun 8,2023, From https://www.nmpa.gov.cn/yaowen/ypjgyw/20230608165801122.html
[2] 贝达药业伏罗尼布片(CM082)上市申请获受理. Retrieved Jan 14,2022, from https://mp.weixin.qq.com/s/yHrneAxiUBC2OfXxkQX0XA
[3]贝达药业埃克替尼和伏罗尼布临床研究成果亮相ASCO年会. Retrieved Jun 4, 2021, from https://www.bettapharma.com/News/show/id/2388
[4]贝达药业官网. From https://www.bettapharma.com/Newdrug/projects
本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。






 个人中心
个人中心
 我是园区
我是园区




