
10 月 9 日,据 NMPA 官网显示,礼来高选择性 RET 抑制剂塞普替尼(40 mg & 80 mg 胶囊)获 NMPA 批准,用于治疗转染重排(RET)基因融合阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者、需要系统性治疗的晚期或转移性 RET 突变型甲状腺髓样癌(MTC)成人和 12 岁及以上儿童患者、以及需要系统性治疗且放射性碘难治(如果放射性碘适用)的晚期或转移性 RET 融合阳性甲状腺癌(TC)成人和 12 岁及以上儿童患者(受理号:JXHS2101071)。
塞普替尼是首个获批专门用于治疗携带 RET 基因变异癌症患者的精准疗法。
塞普替尼是一种强效、高选择性、口服 RET 酪氨酸激酶抑制剂。
塞普替尼于 2020 年 5 月获 FDA 批准,成为全球首个获批的高选择性 RET 抑制剂。在国内,塞普替尼于 2019 年 11 月首次获批临床,次年 1 月首次公示临床试验,于 2021 年 11 月申报上市
,并被纳入优先审评,加速其获批进程,于本周获批上市。
来自:Insight 数据库(http://db.dxy.cn/v5/home/)
此次在国内获批是基于全球研究 LIBRETTO-001 数据和 LIBRETTO-321 研究中国人群数据。
LIBRETTO-001 研究
是一项评估塞普替尼治疗 RET 驱动型癌症患者的最大规模的全球 I/II 期临床试验。研究终点主要的疗效考量是确认的客观缓解率(ORR)和中位缓解持续时间(DoR)。NSCLC 人群最新研究结果已在 2022 年欧洲肺癌大会(ELCC)上发表,而甲状腺癌人群最新研究结果已在 2022 年欧洲肿瘤内科学会(ESMO)大会上发表。
研究结果显示
,对于 RET 融合阳性的局部晚期或转移性 NSCLC 患者、RET 突变型的晚期或转移性 MTC 患者、RET 融合阳性的晚期或转移性 TC 患者,塞普替尼均具有缓解率高,持续时间久的优势。
NSCLC 患者中
,IRC 评估的 ORR 为 84.1%(95%CI:73,92),中位 DoR 为 20.2 个月(95% CI:13,NE),中位 PFS 为 22 个月(95% CI:14,NE)。在 247 例经治患者中,ORR 为 61.1%(95%t CI:55,67),中位 DoR 为 28.6 个月(95% CI:20,NE),中位 PFS 为 24.9 个月(95% CI:19,NE)。
在未接受过卡博替尼/凡德他尼治疗的 142 例 RET 突变的晚期 MTC 患者中
,IRC 评估的 ORR 为 81%(95% CI:74,87),随访 2 年左右,中位 DoR 和中位 PFS 均未达到;在既往接受过卡博替尼/凡德他尼治疗的 151 例 RET 突变的晚期 MTC 患者中,ORR 为 73.5%(95% CI:66,80) ,中位 DoR 未达到,中位 PFS 为 34 个月(95% CI:26, NE)。
在 12 例初治 RET 融合阳性的晚期 TC 患者中
,IRC 评估的 ORR 为 92%(95%CI:62,100),中位 DoR 未达到(95% CI: 15, NE),1 年 PFS 率为 100%(95% CI: 100, 100);22 例既往接受过系统性治疗的 RET 融合阳性的晚期 TC 患者,ORR 为 77%(95% CI:55,92),中位 DoR 为 18 个月(95% CI:10,NE),1 年 PFS 率为 69%(95% CI: 43, 85)。
安全性方面,塞普替尼耐受性良好,大部分不良反应(AE)为低级别,可控制并且可逆,仅 3-4% 的患者因治疗相关的 AE 停药。
LIBRETTO-321 研究
则是一项旨在评估塞普替尼用于中国 RET 变异晚期实体瘤患者疗效与安全性的开放标签、多中心、Ⅱ 期临床试验,共入组 77 例 RET 基因变异晚期实体瘤中国患者,包括 47 例 RET 融合阳性晚期 NSCLC 患者,29 例 RET 突变晚期 MTC 患者和 1 例 RET 融合阳性晚期 TC 患者。该研究全文已分别于 2022 年 7 月(NSCLC 部分)5 和 8 月(MTC/TC 部分)6 发表在《Therapeutic Advances in Medical Oncology》期刊上。
研究结果显示,中国数据与 LIBRETTO-001 全球数据具有高度一致性,验证了塞普替尼在中国人群中良好的疗效与安全性。
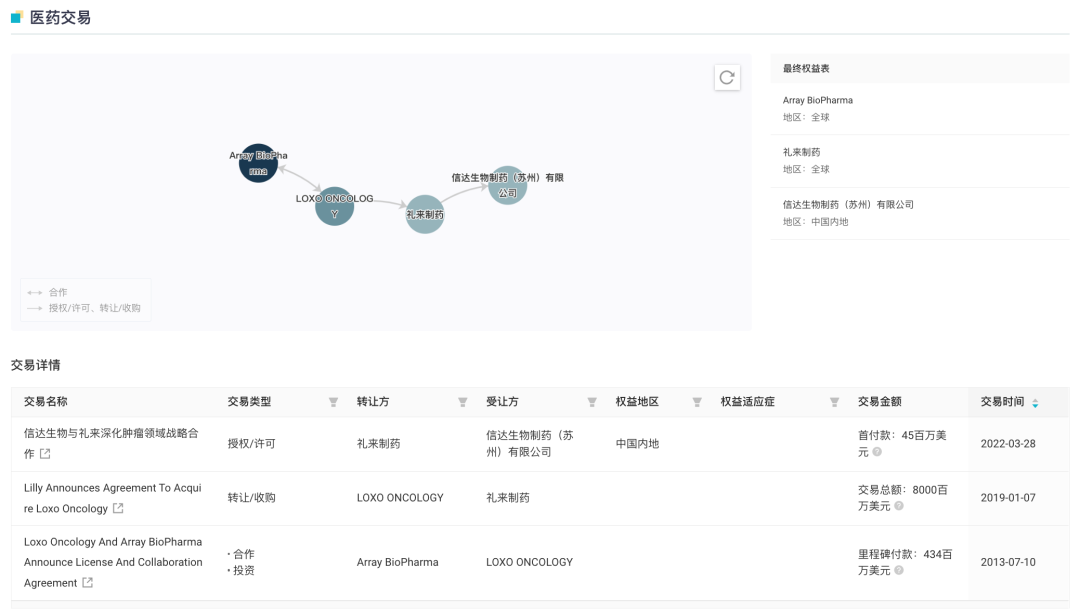
2022 年 3 月,礼来制药与信达生物进一步深化肿瘤领域的战略合作,其中包括信达获得塞普替尼在中国的独家商业化权利,全权负责塞普替尼的定价、进口、营销、分销和销售推广。
免责声明:
本文仅作消息分享,
并不构成投资建议,也不代表 Insight 数据库的立场,文章观点仅供分享行业见解,请广大投资者谨慎。
投稿:微信 insightxb;邮箱 insight@dxy.cn
免费试用 Insight 数据库












 个人中心
个人中心
 我是园区
我是园区




