 2021年10月29日,诺华宣布FDA批准其
BCR-ABL变构抑制剂Asciminib
(原始编号:ABL-001,商品名为:Scemblix
)
,用于治疗慢性粒细胞白血病
(CML)
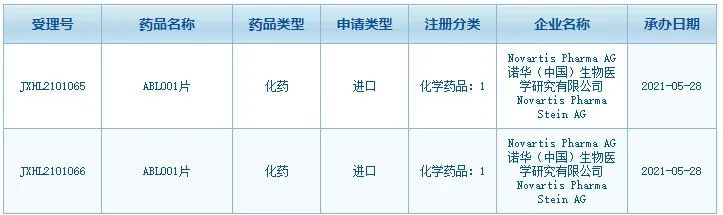
。今年2021年5月28日,中国NMPA承办了诺华BCR-ABL变构抑制剂ABL001片临床申请。
2021年10月29日,诺华宣布FDA批准其
BCR-ABL变构抑制剂Asciminib
(原始编号:ABL-001,商品名为:Scemblix
)
,用于治疗慢性粒细胞白血病
(CML)
。今年2021年5月28日,中国NMPA承办了诺华BCR-ABL变构抑制剂ABL001片临床申请。

ASCEMBL是首个针对既往接受TKI治疗的CML患者的头对头随机对照研究,Ⅲ期临床研究中,在第24周时,与Bosutinib相比,Asciminib的MMR率和CCyR率分别为25%和41%,Bosutinib为13%和24%,提高均接近1倍。凭借另一项一期临床结果,FDA同时批准Asciminib第二项适应症,即携带T351I突变的Ph+ CML-CP患者。

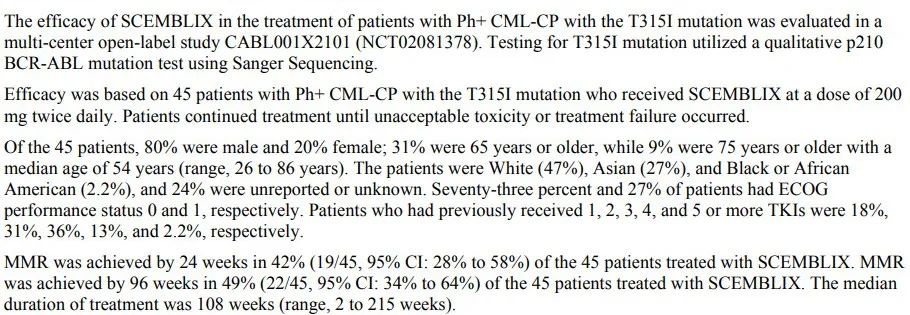
此前的BCR-ABL抑制剂,均靶向ATP结合位点;而Asciminib则靶向肉豆蔻酰口袋(specifically targeting theabl myristoyl pocket, STAMP),可将BCR-ABL1锁定为非活性构象,为一种变构抑制剂。

Asciminib(ABL001)研发背景

BCR/ABL是9号染色体的ABL基因与22号染色体的BCR基因融合形成的一种融合蛋白,被称为“费城染色体”,是个体化肿瘤治疗靶点的经典范例。BCR/ABL融合蛋白能够组成性激活,驱动CML细胞的恶性增殖,被证明为CML的主要发病机制。2001年,FDA批准ABL抑制剂伊马替尼上市,成为第一个小分子靶向药物,开启肿瘤靶向治疗的新时代。但ABL突变尤其是T315I位点突变耐药一直是尚未解决的重大临床问题。

选择性变构ABL抑制剂

由于Asciminib独特的作用机制区别于传统TKI,因此Asciminib对TKI耐药的肿瘤也有强效抑制活性,包括T315I、Y253H、E255K等突变体。尽管Asciminib在临床前的研究中就发现存在耐药性,但其与ATP竞争性TKI的耐药突变是正交的,两种抑制剂联用,耐药出现概率显著降低。
2020年8月26日,诺华宣布,在是一项多中心、开放标签、随机3期临床ASCEMBL研究中,asciminib(ABL001)与辉瑞bosutinib(博舒替尼,BOSULIF®)相比,在24周治疗慢性期费城染色体阳性慢性粒细胞白血病(Ph+CML-CP)患者的主要分子反应(MMR)率方面具有统计学显著优势,该3期临床研究ASCEMBL初步分析达到了主要终点。
据报道,TGRX-678是深圳市塔吉瑞生物医药有限公司研发的首个国产BCR-ABL1变构抑制剂,也是全球第二款BCR-ABL1变构抑制剂,目前已获得中国临床许可(受理号:CXHL2000158/CXHL2000159)。
有关CML与ABL抑制剂
慢性骨髓性白血病(chronic myelogenous (or myeloid) leukemia (CML))是一种造血干细胞克隆增生性疾病。慢性粒细胞白血病在所有年龄阶段都有发生,但在20~50岁人群中发病率较高。其年发病率为0.1~0.2%,男性发病率略高于女性,占成年白血病患者的15~20%。我国每年新增病例高达30000例。
慢性髓性白血病(CML)是单基因驱动的疾病,95%以上的患者均发生BCR-ALB基因融合。BCR-ABL融合是CML发病的主要分子机制,也是其有效治疗靶标。一代ABL抑制剂格列卫的上市给CML的临床治疗带来革命性进步,大幅提高了CML患者的存活时间,但很快出现的靶蛋白突变耐药限制了进一步的临床治疗效果。
二代ABL抑制剂能够克服大部分的突变耐药,但对T315I等突变无效;而T315I突变是最为常见的耐药类型之一,发生率约20%。已上市的二代ABL抑制剂包括2007年诺华开发尼洛替尼以及2012年百时美施贵宝开发的达沙替尼等。
2012年,三代ABL抑制剂普纳替尼上市,是目前仅有的可以治疗T315I突变耐药的药物,但该药尚未获批进入中国,同时该药存在严重不良反应及副作用,被美国FDA打上黑框警告,其临床使用受到严重限制。这意味着,对于现有ABL抑制剂耐受的CML患者而言,更安全、有效的治疗药物仍是尚未被满足的、急需的临床需求。
2020年6月,中国自主研发的三代ABL抑制剂HQP1351已经提交中国上市申请(NDA)。

已上市的三代ABL抑制剂

临床前及临床研发中的ABL抑制剂
推荐学习:
请注明:姓名+研究方向!


本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。




 个人中心
个人中心
 我是园区
我是园区




