
今年6月,《华尔街日报》一篇报道称,默沙东正考虑以约400亿美元的高价收购Seagen。该消息称,触发收购的一个重要因素是Seagen的多款抗体偶联药物(ADC)可以与默沙东的 PD-1 抑制剂 Keytruda (pembrolizumab)联用,以加强后者以Keytruda为龙头的抗癌药产品组合。
7月26日,安斯泰来和 Seagen 宣布,两家公司合作开发的靶向于Nectin-4 【脊髓灰质炎病毒样受体4 (pvrl-4) 编码蛋白】的抗体偶联药物(ADC) Padcev (enfortumab vedotin) 与Keytruda联用于治疗晚期尿路上皮癌的研究结果,其确认的客观缓解率 (ORR) 达到 64.5%。
消息发布后,Seagen 的股价在当天的盘前交易中上涨 2.5%。
很显然,正在进行中的Padcev与Keytruda联用的I/II 期临床研究(EV-103)的结果对默沙东的收购决策至关重要。
Nectin-4是一种不依赖 Ca2+ 的免疫球蛋白样蛋白,是Nectin家族NECTIN4编码的的I型跨膜蛋白,主要在胚胎和胎盘组织中表达,成年后其表达显著下降。近年来,人们发现针对Nectin-4 的药物在乳腺癌、肺癌、结直肠癌、胰腺癌、卵巢癌等多种恶性肿瘤细胞表面高度表达,并且在这些上皮恶性肿瘤的发生、侵袭和转移中起关键作用,是ADC一个新型的重要靶点。
作为首款靶向Nectin-4的ADC,Padcev于2019年12月通过加速审批获得FDA批准上市,用于之前接受过铂类为基础的化疗及PD-1/PD-L1抑制剂治疗的局部晚期或转移性尿路上皮癌的患者。一年半后,Padcev顺利获得FDA完全批准,并拓展适应症至曾接受过PD-1/PD-L1抑制剂治疗,但不适合接受顺铂治疗的局部晚期或转移性尿路上皮癌的患者。
去年,Padcev的销售额为2.2亿美元,若能将获批适应症提前到一线治疗,华尔街预测其销售额有望在2030年达到28亿美元,成为一款重磅炸弹级的产品。
尚需等待一线治疗完整结果
铂类化疗是局部晚期或转移性尿路上皮癌的标准一线治疗,联合PD-1/PD-L1抑制剂可获得良好的ORR。然而,由于多种不良反应如肾功能不全、神经病变、身体状况不佳等,大约有一半患者无法接受铂类化疗。
因此,Padcev若能将适应症拓展至不能接受铂类化疗患者的一线治疗,将大大提升药物的适应症人群。
2017年9月开始的EV-103研究(NCT03288545)是一项设计复杂的研究,在I期临床研究剂量爬坡后设置了针对尿路上皮癌的3组扩展研究(Cohort A 和B、Cohort D、E和F、Cohort G)和1组随机研究(Cohort K),以及针对另一种膀胱癌肌肉浸润性膀胱癌的3个Cohort(Cohort H、J、L)。
该临床试验针对尿路上皮癌的部分研究设计如下:
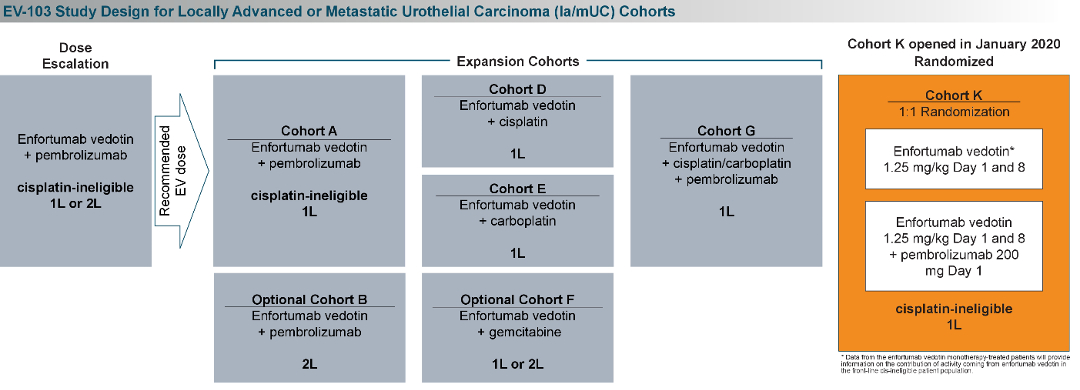
来源:ASCO 2020
而本次发布的是Cohort K的研究结果。该队列研究将Padcev单用及与 Keytruda联用,用于无法接受顺铂化疗的患者,比较两组的研究结果。
现在,Astellas 和 Seagen宣布,经独立数据监查委员会的独立审查,两药联用达到65%的ORR,中位缓解时间(mDoR)尚未达到。这一结果与2020年在ASCO-GU上公布的Cohort A结果相一致。Cohort A结果显示,Padcev与Keytruda联用,用于同样适应症患者的ORR为73%。
然而,两家公司并没有公布Padcev单独治疗组的ORR数据。此前,默沙东公司的Keynote-052研究结果显示,Keytruda用于无法接受顺铂患者的一线治疗,ORR为24%。
这样看来,似乎药物联用的疗效不错,Astellas 和 Seagen也表示将与FDA讨论这个结果。不过,新闻稿中未公布Padcev单药的ORR值还是让人费解,而之前发布的EV-201研究Cohort 2的数据显示,Padcev单药用于无法接受顺铂的患者的二线治疗,ORR能达到50.6%。
Keytruda单药一线治疗尿路上皮癌的适应症已经在美国获批,但与Lenvima联用的LEAP-011研究已经因结果不佳而停止。因此Cohort K的完整数据对于默沙东权衡收购Seagen的交易来说至关重要。
Evaluate Vantage总结了Padcev治疗尿路上皮癌的多个研究及结果:
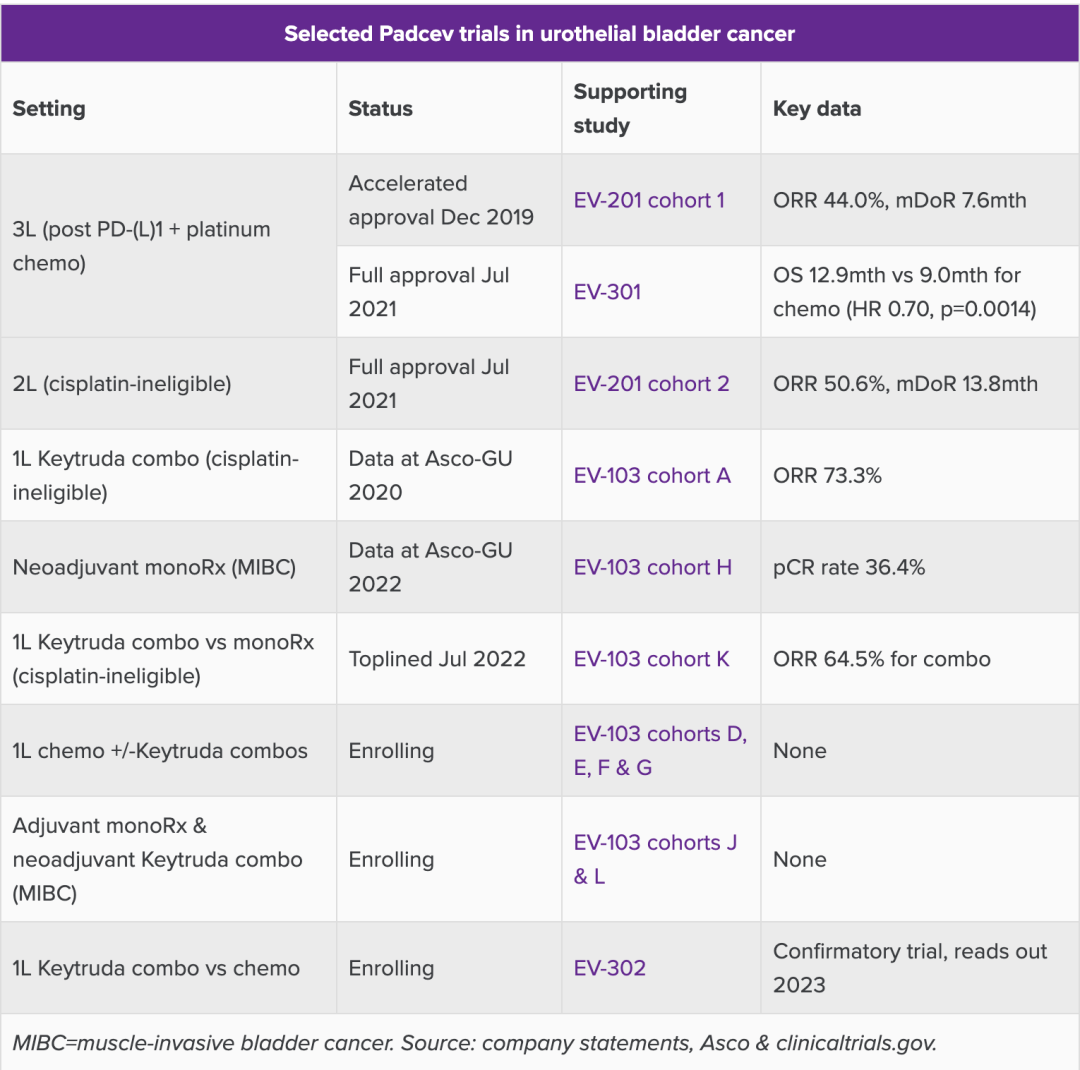
仅有少数玩家开发Nectin-4药物
不过,尽管Padcev已经取得商业化的初步成功,但目前正在开发的Nectin-4药物并不多,除Padcev外,仅有两款药物在早期临床阶段,另外还有3款已公开的临床前Nectin-4药物(见下图)。
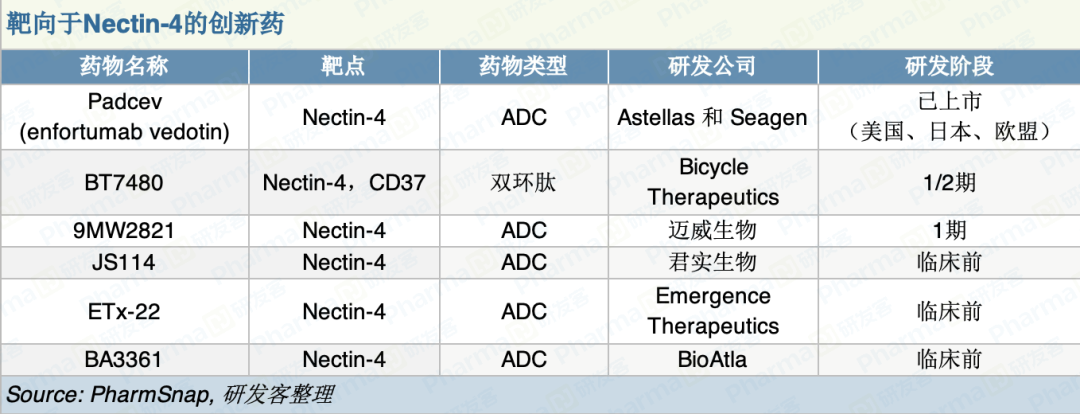
仅有的5款在研药物中,有2款来自中国公司。近日,迈威生物宣布,其自主研发的靶向Nectin-4的ADC创新药9MW2821的临床试验申请已获得了FDA的批准,即将开展针对实体瘤患者的I期临床研究。该款药物正在国内多家医院开展I期临床研究。
国外公司中,Bicycle Therapeutics的BT7480也进入了临床阶段,去年11月该公司宣布已经完成了I/II期临床研究的首例患者给药。该研究同样用于实体瘤患者。BT7480也是唯一一款非ADC的Nectin-4药物,是Bicycle利用双环肽技术开发而成,可以同时靶向于Nectin-4和CD137。肽类的分子量较小,能避免常见的肝脏和胃肠道毒性。
就目前而言,尽管在Nectin-4这个靶点上,我们已经有了一个已上市的药物Padcev,但相关的探索与研究尚处在早期阶段,还需要更多的研究数据来验证其临床疗效。
Astellas 和 Seagen当前围绕Padcev正开展20多项临床研究,其中包括7项III期临床试验,绝大多数是针对泌尿系统癌症。这些研究的数据不仅对Padcev的销售额提升,对后续其他Nectin-4产品开发都有非常重要的指导意义。让我们一起等待这些研究的最终结果发布。




 个人中心
个人中心
 我是园区
我是园区




