30 岁,担任华中科技大学的研究所所长和副院长;不到 40 岁,担任中科院生物物理研究所所长;不到 50 岁,又先后当选中科院院士和发展中国家科学院院士。而今年 4 月,52 岁的徐涛受聘为广州医科大学生物医学工程学院院长,掀开了职业生涯新的一页。
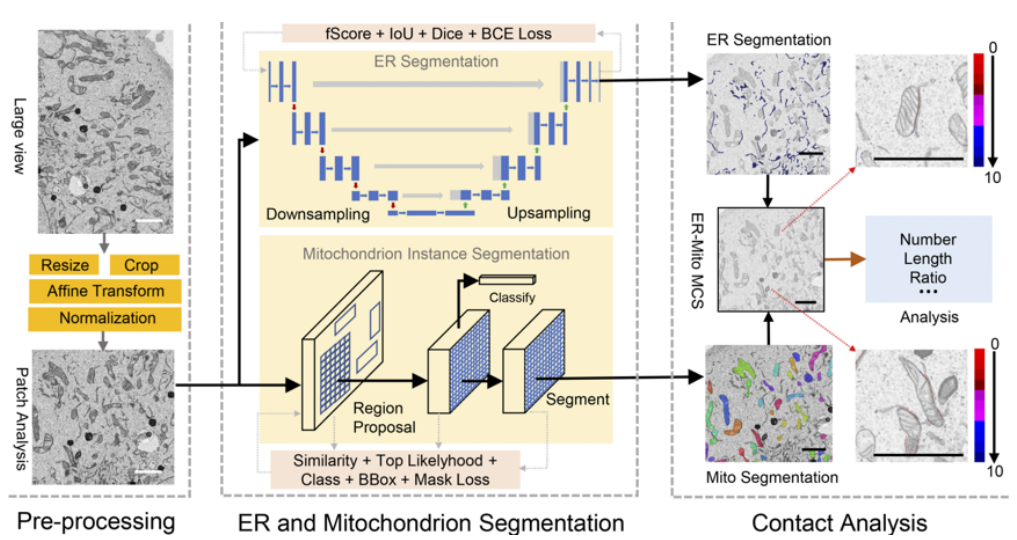
生于湖北宜昌的徐涛,是一名细胞生物物理学家。前不久,他和团队提出了一款基于深度学习的细胞器互作高通量分析系统 DeepContact,
成功填补了细胞器互作领域的空缺,并将成为加速细胞器互作研究的利器。
其表示,使用 DeepContact 进行二维电镜数据进行分析时,具备可容纳样本量大等优势,能支持细胞器互作网络的相关性基础研究,故能给细胞器互作的系统性研究提供一个强有力的工具。
另据悉,DeepContact 兼具组织电镜特异细胞类型分析能力,可扩展用于人体临床样本的超微医学病理学研究中,从而成为一个能给超微病理诊断提供更客观科学评价的工具。
此外,DeepContact 的源代码、细胞器预测模型、以及训练数据是开源的,细胞器预测分割模型也可植入到图像分析软件 Amira 中。
拥有这款商用软件的研究机构,都可通过其图形界面进行调用。同时,该团队也会不断优化程序的性能。
(来源:Journal of Cell Biology)
据介绍,细胞生物学研究的核心目标之一,在于理解细胞内部的复杂结构与细胞功能之间的关系。所有细胞的表面,都有一层由生物膜组成的屏障。
而从简单的原核细胞、到相对复杂的真核细胞的一个重要进化标志,就是细胞内部出现了生物膜结构,包括包裹遗传物质的细胞核、合成蛋白质和脂质的内质网、以及产生细胞所需能量的线粒体等。
这些相对独立的膜性结构,也被当作是维持实现细胞各种功能的一个个“小器官”,因此被称为“细胞器”。此前经典的细胞生物学研究,都是针对单个细胞器分别展开的。
有意思的是,近年来研究人员发现,细胞器之间存在一些有直接相互作用的接触位点,而细胞器的相互作用能介导其功能的协同效应,并能增加细胞器间信息互通的精准程度和效率。
因此,关于细胞器互作的相关研究,逐渐成为细胞生物学领域的前沿热点。举例来说,国家自然科学基金委敏锐捕捉到这一研究动向,设立了“细胞器互作”的重大研究计划,将国内顶尖的细胞生物学研究人员都聚焦于细胞器互作的团队攻关。
遗憾的是,一直以来,细胞器互作的程度的检测和计量都依靠低效的手动标注,一些互作的检测探针由于需要过表达,还得引入额外的干扰。
在这一背景下,徐涛课题组意识到:一个高通量、高精度和高速的细胞器互作计量工具,迫在眉睫、亟待研发。
他说:“为了实现这些设计要求,我们想到了人工智能。此前的一些研究表明,深度学习的方法可以用来识别亚细胞结构,尤其是内质网、线粒体和脂滴等形态特征鲜明的细胞器。”
基于此,该团队运用深度学习系统识别了同一张电子显微镜图像中的不同细胞器、并自动划定其边界,再根据这些信息快速系统地计算出细胞器互作的频率和程度等重要参数。
实践证明,这一方法既高效又准确,不依赖细胞器的特殊染色,还可广泛用于不同组织和细胞类型上。
徐涛
院士、中科院生物物理所研究员胡俊杰、以
及中科院计算所研究员肖立(现任职北京邮电大学人工智能学院)担任共同通讯作者,刘丽清和杨树鑫担任共同第一作者 [1]。
图 | 相关论文(来源:Journal of Cell Biology)
论文送审过程中,一位电镜专家认为:这项工作致力于解决一个领域里的重要问题,(电镜图像中的)细胞器识别是一项难度高、易出错的挑战,许多生物学家都急切希望看到这一环节的自动化提升。
另一位评审专家提出:此前的细胞器互作计量大部分是针对于三维电镜数据的,对电镜机时、计算机算力资源都有很高的要求,即使对较小细胞样品量的分析,也往往耗时极长。
DeepContact 的设计很好地解决了这些问题,凸显了二维电镜图像处理的优势,为细胞器互作研究提供了一个高效客观的高通量计量方法。此次研究也全方面地证实了该方法的精准度、高效性、及其广泛的应用场景。论文发表后,JCB 在杂志网站首页推荐了该工作。
(来源:Journal of Cell Biology)

DeepContact 的最核心算法:细胞器互作位点长度比率的计量方式
徐涛表示:“我的课题组长期从事细胞生物学研究,我本人也对学科中的新技术、新方法的开发尤为关注和重视,(同时)我们组在超高分辨率成像和光镜电镜融合等方面都有可喜的进展。”
在研究细胞生物课题的过程中,该团队意识到了细胞器互作自动化计量这一短板。而在细胞器互作专项的年度交流会上,也常有研究人员提到精准计量的诸多困难。
于是,他们萌发了借助多学科交叉来解决这一问题的想法。研究中,课题组首先讨论了取材的方式,由于细胞器直接接触位点往往在 30-50 纳米的范围,而即使最尖端的光学显微镜目前也很难清晰地分辨,因此他们将素材定焦于具有更高分辨率的电子显微镜成像。

图 | 从左至右:肖立、杨树鑫、刘丽清(来源:资料图)
该团队的博士后刘丽清长期从事基于电镜的细胞生物学研究,在各类型的电镜制样和成像中积累了丰富的经验和素材,因此所有电镜图像均由其采集。
接下来徐涛找到了肖立,后者对于生物医学图像的数字化处理有着浓厚兴趣,在细胞器分割识别方面也有一定基础和尝试。
最终,该项目的深度学习模型建立、计量程序开发和优化均由肖立团队完成,其团队的硕士生杨树鑫也是论文的并列第一作者。
然后,徐涛又联系了自己在生物物理所的同事胡俊杰。他说:“俊杰长期研究内质网的结构与功能,近年来对内质网介导的细胞器互作颇感兴趣,也参与承担了细胞器互作重大研究计划的项目,
他在本工作细胞场景的选择和互作动态的解析中提供了重要的参考。”
有了一支具有共同兴趣的多学科交叉的团队,研究效率也变得事半功倍。DeepContact 的原型很快被搭建起来。
第一作者刘丽清表示:“DeepContact 最核心的算法,是细胞器互作位点长度比率的计量方式,为此我们进行过多个阶段的设计和尝试。”
2021 年初,该团队建立了分割能力非常准确的深度学习模型,所有数据都已采集分析完成。但是,当时互作位点长度的计量,依旧在一个互作位点间距范围内进行体现(例如≤30nm)。
实际上,互作位点上的蛋白复合体的横向跨越长度,决定了细胞器的互作间距。因此,只限定一个范围做互作位点分析,必将会带来一定的局限性。
刘丽清继续说道:“关注到这个问题后,徐老师和胡老师提出了按照不同细胞器互作间距宽度来呈现互作长度比率的建议。”
2022 年春节期间,为了达到更全面、更精确的分析要求,肖立团队和刘丽清推翻了以往所有的高通量分析结果,并在两个月左右重新尝试建立了三个数学模型,最终确立了以细胞器互作位点宽度为基准、来进行细胞器互作比率计量的统计分析方式,实现了以不同颜色来区分互作位点宽度。
刘丽清总结称:“不同专业知识的沟通、每个成员想法的碰撞、几次全面推翻模型和从头分析,为 DeepContact 提取出了更科学、更有效的分析流程。这也使我坚信,要继续以精益求精的精神,践行以关键科学问题为导向的技术方法。”她表示。
而对于后续计划,作为共同一作的刘丽清表示,目前课题组已建立线粒体、内质网和脂滴的 DeepContact 分割模型,这些模型主要针对 ROTO 方法制样的高衬度电镜数据类型。
同时,所涵盖的细胞器类型、固定染色方案、组织、细胞类型、成像的电镜类型和图像分辨率都比较有限。因此,后续需要在应用过程中,逐渐对其进行扩展以适应更广泛的科研需求。
另据悉,DeepContact 边缘检测精度会受到化学电镜染色、成像分辨率等影响。针对以上问题,研究人员计划主动增加训练数据类型、逐步升级 DeepContact 算法,
借此去提高细胞器边缘检测的精度,让模型在不同成像条件下的域适应和泛化能力得到提升。
而且,生物医学电镜领域内的一些热门发展方向,也将提升 DeepContact 的基础算法,从而满足更多的统计分析需求。
“我本人已在近期入职位于怀柔科学城的国家级多模态跨尺度生物医学成像设施,将在徐院士带领下,和团队多方研究力量协作努力,大力推广 DeepContact 的应用。”刘丽清最后表示。

1.Liu, L., Yang, S., Liu, Y., Li, X., Hu, J., Xiao, L., & Xu, T. (2022). DeepContact: High-throughput quantification of membrane contact sites based on electron microscopy imaging. Journal of Cell Biology, 221(9).











 药选址
药选址











