艾伯维JAK抑制剂「乌帕替尼缓释片」有望近期在中国获批
收藏
关键词:
获批
资讯来源:医药观澜 + 订阅账号
发布时间:
2022-02-11
▎药明康德内容团队报道
2月10日,中国国家药监局(NMPA)官网药品注册进度查询可知,艾伯维(AbbVie)申请的乌帕替尼缓释片新药上市申请已进入:在审批,意味着这款产品有望近期在中国获批。根据中国国家药监局药品审评中心(CDE)优先审评公示,此次乌帕替尼缓释片有望在中国获批的适应症为:用于适合系统性治疗的成人和12岁及12岁以上青少年中重度特应性皮炎患者。
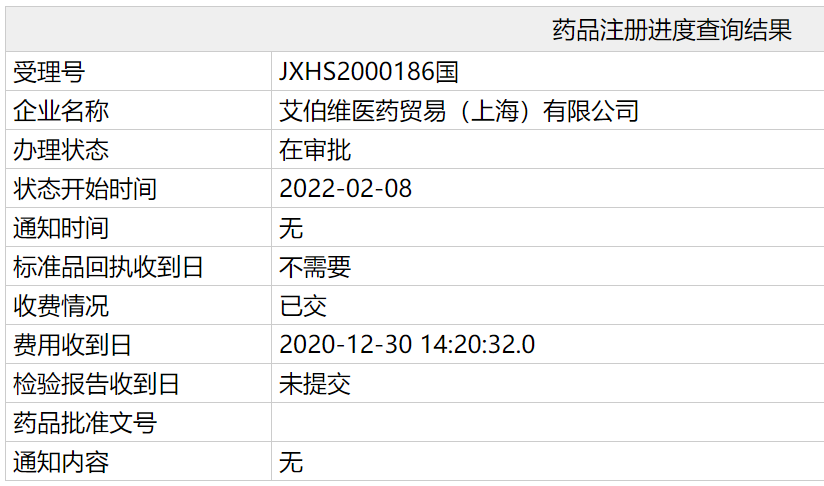
截图来源:NMPA官网
乌帕替尼由艾伯维科学家发现和开发,是一种每日口服一次、选择性和可逆性JAK1抑制剂。JAK家族是一类非受体酪氨酸激酶,包括JAK1、JAK2、JAK3、TYK2四种亚型,它们在多种I型和II型细胞因子受体的信号级联中具有重要的作用,由JAK介导的信号通路与细胞增殖、分化、凋亡以及炎症等过程有关。其中JAK1在免疫介导的疾病的病理生理过程中发挥重要作用,这使得JAK1抑制剂有潜力治疗多种疾病。
公开资料显示,乌帕替尼(upadacitinib,商品名:Rinvoq)最早于2019年8月被
上市,治疗对甲氨蝶呤反应不足或不耐受的中度至重度活动性风湿性关节炎成年患者。此后该药陆续获得FDA批准治疗成人和12岁及以上儿童及青少年的难治性、中度至重度特应性皮炎以及活动性银屑病关节炎。
在中国,艾伯维于2020年底递交了乌帕替尼的两项上市申请,分别对应30mg和15mg两种不同规格。该申请随后以“符合儿童生理特征的儿童用药品新品种、剂型和规格”为由被CDE纳入优先审评,拟定适应症为:用于适合系统性治疗的成人和12岁及12岁以上青少年中重度特应性皮炎患者。

据艾伯维早先新闻稿介绍,
FDA批准乌帕替尼的特应性皮炎适应症,是基于其在3期注册研究中所提供的有效性和安全性数据。
该项目评估了横跨3项研究的2500多例患者
(Measure Up 1、Measure Up 2和AD Up),约52%的患者既往接受过系统性特应性皮炎治疗
。
研究结果显示,乌帕替尼单药治疗和与外用糖皮质激素联合治疗在第16周均达到了所有主要和次要终点
。相较于安慰剂组,治疗组
一些患者达到了更高的皮损清除率
。
特应性皮炎是一种反复发作的炎症性皮肤病。目前,特应性皮炎的治疗现状不尽如人意,尤其是针对中重度特应性皮炎的治疗方法中,外用及系统治疗均存在一定的局限性和不良反应。随着对疾病发病机制的深入研究,以JAK抑制剂为代表的小分子靶向抑制剂逐渐用于临床,推动了这类疾病治疗模式的改变。
希望艾伯维乌帕替尼缓释片早日在中国获批,能让中国特应性皮炎患者增加新的治疗选择!
参考资料:
[1]NMPA官网药品注册进度查询. Retrieved Feb 10,2022, from http://sq.nmpa.gov.cn/datasearch_nmpa/schedule/search.jsp?
[2]美国FDA批准RINVOQ®(upadacitinib)用于治疗成人和12岁及以
上儿童及青少年的难治性、中度至重度特应性皮炎.Retrieved Jan 17 2022 , from https://mp.weixin.qq.com/s/0Z1sh2ezipuljymQD3yxBw
[3]
RINVOQ®(upadacitinib)获得美国FDA批准用于治疗活动性银屑病关节炎.Retrieved Dec 16,2021 ,
from https://mp.weixin.qq.com/s/ofMsIhKj6wecqCxq7QL6cA
本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。








 个人中心
个人中心
 我是园区
我是园区




