根据港交所最新披露,科济药业控股有限公司(CARsgen Therapeutics Holdings Limited)已递交IPO申请,联席保荐人为高盛和UBS。科济药业是一家在中国及美国运营的临床阶段的生物医药公司,专注于治疗实体瘤和血液恶性肿瘤的创新细胞疗法。根据招股书
,本次IPO募集资金将主要用于进一步开发其核心候选产品BCMA CAR-T(CT053),为其他管线候选产品的研发活动提供资金,培养全面的制造及商业化能力等。在医药观澜微信号回复“科济”可下载招股书PDF。

根据招股书,科济集团由董事会主席、执行董事、首席执行官兼首席科学官李宗海博士与执行董事兼首席运营官王华茂博士创立。自成立以来,该集团在中国获得了众多的医疗投资人的投资和支持,包括正心谷资本、拾玉资本、BVCF、高瓴资本、JT Investment Fund、礼来亚洲基金等。
根据招股书,目前该公司正在开发11款用于治疗实体瘤及血液恶性肿瘤的候选产品,其中6款正处于临床阶段,10款均为CAR-T细胞疗法。据介绍,其CAR-T候选产品循证新型肿瘤相关抗原,并经过精心设计和优化,以减少现有CAR-T疗法常见的副作用。此外,他们正在探究专有的同种异体CAR-T技术THANK-uCAR,旨在克服同种异体CAR-T细胞扩增及持久性效率不高的问题并形成可随时以较低成本使用的优质、普遍同种异体CAR-T细胞疗法。
CT053是一种采用全人抗体靶向B细胞成熟抗原(BCMA)的潜在“best-in-class”的自体 CAR-T候选产品,开发用于治疗复发难治多发性骨髓瘤(R/R MM)。此前,CT053已经获得美国FDA授予的
再生医学先进疗法(RMAT)资格和孤儿药资格
,欧洲药品管理局(EMA)授予的
优先药物资格(PRIME)和孤儿药资格,
并被中国国家药监局(NMPA)药品审评中心(CDE)纳入
突破性治疗品种
名单。
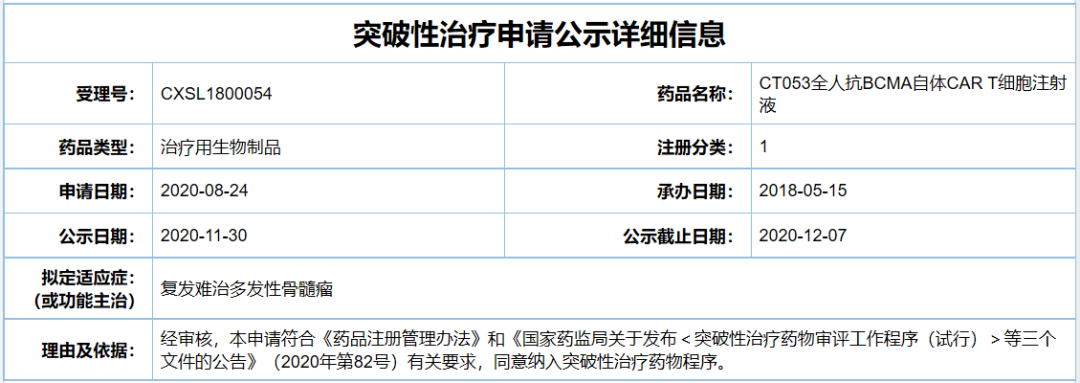
目前,CT053正在广泛开展治疗R/R MM的临床项目,包括若干由研究者发起的试验、中国的1/2期临床试验和北美的1b期临床试验。研究显示,CT053在中国和北美R/R MM患者中有一致的良好的耐受性,在经过多线治疗的患者中观察到显著且持久的临床疗效,细胞在体内扩增良好,且未检测到抗药抗体(ADA)。
根据招股书,CT053用于治疗既往至少接受三线疗法治疗MM患者的新药申请计划在2022年上半年向NMPA提交,并在2023年上半年向FDA提交生物制品许可申请(BLA)。同时,该产品的随机全球3期试验正在筹备中,以评估CT053作为R/R MM的早线治疗。
除了CT053外,科济药业的产品管线还包括5款处于临床阶段候选产品,以及5种处于临床前阶段的候选产品。

▲科济药业在研产品(图片来源:参考资料[1])
CT041
:一款人源化抗CLDN 18.2自体CAR-T细胞注射液,拟开发用于治疗CLDN18.2表达阳性、既往经系统治疗后出现进展或复发的晚期胃腺癌/食管胃结合部腺癌、胰腺癌等适应症。此前,该产品已获得FDA孤儿药资格,用于治疗胃腺癌和食管胃结合部腺癌。目前,该产品正在中国和美国开展临床试验,并表现出良好的治疗效果和耐受性。
CT011
:一种“first-in-class”、针对GPC3的自体CAR-T候选产品,开发用于治疗肝细胞癌(HCC)。根据招股书,CT011此前已获得NMPA的临床试验批准,是中国采用CAR-T细胞疗法治疗实体瘤的首个IND许可。目前,CT011已经在中国启动了一项1期临床试验,评估其在GPC3阳性晚期HCC患者中的安全性、细胞动力学和疗效。
CT032
:一种针对CD19的自体CAR-T候选产品,开发用于治疗B细胞非霍奇金淋巴瘤(NHL)。根据招股书,CT032结合了人源化的CD19特异性单链片段变体,与使用鼠抗CD19单链变体片段作为靶向基团的CD19特异性CAR-T产品相比,CT032的毒性有望会降低,免疫原性也会降低。目前,该产品正在中国进行一项开放标签、单臂的1/2期研究。
AB011
:一种经开发用于治疗CLDN18.2阳性实体瘤的靶向CLDN18.2的人源化单克隆抗体候选产品。在临床前研究中,AB011在体外对CLDN18.2阳性肿瘤细胞表现出很强的抗肿瘤活性,当与奥沙利铂和5-氟尿嘧啶联合使用时,在肿瘤小鼠模型中表现出强大的体内抗肿瘤活性。目前,AB011正在中国开展治疗CLDN18.2阳性实体瘤的1期临床研究。
CT017
:为下一代自体CAR-T候选产品,靶向GPC3并含有转录因子,该转录因子是诱导T细胞驻留在非淋巴组织中所必需的主要调节因数。临床前研究表明, CT017能够更好地在实体瘤等非淋巴组织中驻留和持续存在,因此显示出增强的抗实体瘤疗效。CT017目前正处于由研究者发起的试验阶段中,从而评估治疗中国GPC3阳性HCC患者的安全性及疗效。
此外,该公司正在投入大量资源开发新一代CAR-T技术,以解决CAR-T疗法治疗实体瘤的主要挑战。例如由于肿瘤微环境不利,CAR-T细胞在肿瘤肿块中的浸润、持久性或有效性有限。科济药业正在开发CycloCAR,这是一种共同表达细胞因子IL-7和趋化因子CCL21的新一代CAR-T技术,其有望产生更高的临床疗效,并降低对清淋化疗预处理的要求。
预祝科济药业的港交所上市申请顺利进行,希望在资本的助力下,该公司可以早日将这些在研疗法推向市场,造福广大患者。
尊敬的《医药观澜》微信公众号读者:
您好!非常感谢您长期以来的关注和支持。牛年开启,为了更全面地了解《医药观澜》微信号的读者群,从而为您提供更有针对性的内容,我们特邀请您在百忙之中回答这份调查问卷。此次问卷为不记名问卷调查,问卷内容不涉及任何个人信息等敏感信息,调查结果不对外公开,仅用于内部评估,并作为本年度内容推送的重要参考依据。谢谢您的配合与支持,我们将用心倾听您的声音。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。
注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
[1]科济药业招股说明书. Retrieved Feb 26, 2021, from https://www1.hkexnews.hk/app/sehk/2021/103228/documents/sehk21022601773_c.pdf
![]()






 个人中心
个人中心
 我是园区
我是园区




