您还不是认证园区!
赶快前去认证园区吧!
▲点击上方的蓝色“医谷”关注我们
“置顶公众号”获取最有价值行业趋势信息
医谷微信号:yigoonet
近日,CDE官网显示,上海信致医药科技有限公司(以下简称“信致医药”)自主研发的BBM-H901注射液获得药物临床试验批准,将正式启动注册临床试验,用于预防血友病B成年男性患者出血。这是国内首个获批进入注册临床试验的血友病AAV基因治疗药物,也是国内首个全身给药的罕见病基因疗法。
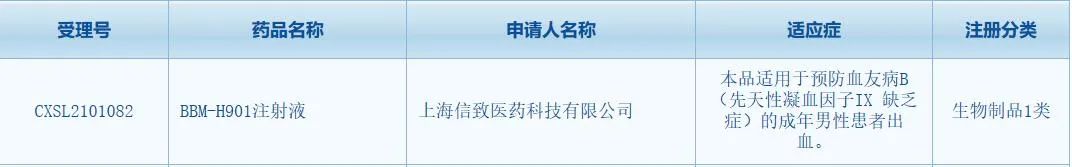
B型血友病由缺乏凝血因子IX导致,约占血友病人数的15%左右。BBM-H901通过AAV载体来递送患者所缺失的人凝血因子IX编码基因,从而提高并长期维持患者体内凝血因子水平,以期达到“一次给药、长期有效”的治疗及预防出血效果。
BBM-H901是国内最早开展临床试验的AAV基因治疗之一,从2019年就开始IIT临床研究(NCT04135300),临床研究数据显示BBM-H901注射液具有良好的安全性和有效性,患者体内凝血因子水平显著提高并长期稳定,且在临床期间未发现明显的不良反应。
2021年4月,BBM-H901被提交临床试验申请,日前获批进入临床试验阶段。
除了BBM-H901外,全球也有众多企业布局B型血友病基因疗法,包括辉瑞与Spark的SPK-9001,uniQure的AMT-060/061,Sangamo的SB-FIX,Freeline的FLT180a等。
目前前两家的疗法都已处在3期阶段,其中AMT-060/061的关键3期临床数据显示,给药后FIX替代疗法的年平均使用量下降了96%,而AMT-060临床试验则被叫停,原因是一位接受AMT-060治疗的病人患上了肝细胞癌,初步临床诊断认为该严重不良事件与AMT-060相关。
文 | 医谷





 个人中心
个人中心
 我是园区
我是园区




