
导读:嵌合抗原受体CAR-T细胞疗法发展迅速,并在癌症治疗中显示出巨大的潜力。然而,仍然存在几个局限性,最近,研究人员提出了一种优先的非病毒策略,以生产具有点突变校正和T细胞受体(TCR)元件精确插入的T细胞产物。因此,为了同时解决病毒使用和随机整合的缺点,研究人员通过CRISPR-Cas9开发了非病毒,基因特异性靶向CAR-T细胞,并证明了它们在治疗复发/难治性B细胞非霍奇金淋巴瘤患者中的高安全性和有效性。
华东师范大学、浙江大学医学院附属第一医院联合创建了一种二合一方法,通过CRISPR-Cas9生成非病毒,基因特异性靶向CAR-T细胞。该研究发布于《Nature》。这也是国内首个在《Nature》期刊发表的CAR-T研究成果!

https://www.nature.com/articles/s41586-022-05140-y
CAR-T细胞疗法的局限性
01
嵌合抗原受体CAR-T细胞疗法在治疗血液系统恶性肿瘤方面显示出巨大的潜力。然而,CAR-T细胞疗法目前有几个局限性。生产过程复杂、成本高、制备周期长,而且还存在安全隐患。CAR-T制备过程中使用的病毒载体的随机插入可能会提高潜在的致癌风险。此外,机体对病毒递送的DNA的特异性反应会阻碍CAR的表达,而且,病毒的制备本身会产生高成本。虽然有些策略,如使用转座子系统和mRNA转导,正在被利用来产生不含病毒的CAR-T细胞,由随机整合引起的最终产物的低同质性和CAR表达的中断成为了额外的问题。
非病毒,基因特异性靶向CAR-T细胞
02
最近,一些研究表明,通过使用腺相关病毒载体作为模板,基因组编辑技术可以应用于生成位点特异性的综合CAR-T细胞。此外,研究人员提出了一种优先的非病毒策略,以生产具有点突变校正和T细胞受体(TCR)元件精确插入的T细胞产物。因此,为了同时解决病毒使用和随机整合的缺点,研究人员成功开发了一种二合一方法,通过CRISPR-Cas9生成非病毒,基因特异性靶向CAR-T细胞。除此之外,研究人员还开发了一种具有PD1集成的创新型抗CD19 CAR-T细胞,该细胞在异种移植模型中显示出根除肿瘤细胞的卓越能力。
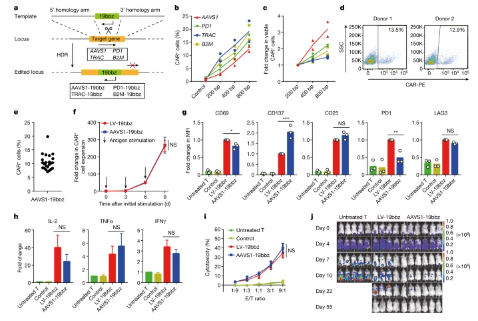
基因靶向修饰CAR-T疗法具有巨大潜力
03
非霍奇金淋巴瘤是一种原发于淋巴组织的血液系统恶性肿瘤,虽然患者在初次治疗后疾病得到缓解,但之后往往出现复发现象。尽管已有CAR-T产品获批用于复发难治性非霍奇金淋巴瘤的临床治疗,可是总体疗效依然有限。PD-1/PD-L1信号通路是抑制T细胞功能的重要免疫检查点,有不少研究报道了PD-1敲除可有效增强CAR-T细胞的功能。
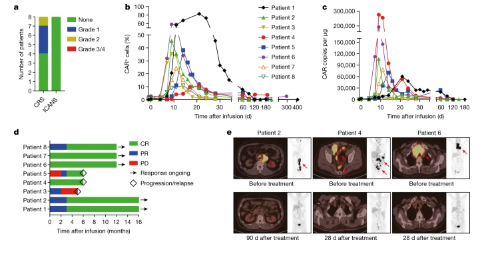
在复发/难治性侵袭性B细胞非霍奇金淋巴瘤的过继治疗中,研究人员观察到80名患者中完全缓解和持久反应的高率(87.5%),没有严重的不良事件。值得注意的是,这些增强的CAR-T细胞即使在低输注剂量和低百分比的CAR细胞下也是有效的。单细胞分析表明,电穿孔法使输液产物中记忆T细胞比例较高,PD1干扰增强了抗肿瘤免疫功能,进一步验证了非病毒、PD1整合CAR-T细胞的优势。研究人员在临床治疗中观察到了高比例的肿瘤完全缓解率,且未发现严重的毒副作用,该结果显示出这种CAR-T疗法具有出色的临床安全性和有效性。研究人员同时也证明了非病毒定点整合T细胞治疗在临床应用的可行性。这一技术创新为未来更多基因靶向修饰CAR-T疗法的发展奠定了坚实的基础,对领域发展具有重要的推动作用。
参考资料:https://www.nature.com/articles/s41586-022-05140-y
识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!
请注明:姓名+研究方向!


本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。




 个人中心
个人中心
 我是园区
我是园区




