▎药明康德内容团队编辑
Vertex Pharmaceuticals公司今日宣布,美国FDA已经授予在研疗法inaxaplin(VX-147)突破性疗法认定,用于治疗APOL1介导的局灶节段性肾小球硬化(FSGS)患者。同时,欧盟药品管理局(EMA)也授予这一在研疗法PRIME药品认定,用于治疗APOL1介导的慢性肾病(AMKD)。新闻稿指出,inaxaplin是首款针对AMKD潜在机制的在研疗法。

APOL1介导的肾脏疾病是一种由APOL1基因突变引起的慢性肾脏疾病。遗传性功能增益性(gain of function)APOL1基因突变产生的蛋白会导致足细胞损伤。这种损伤破坏了肾脏正常的过滤功能,导致蛋白尿和快速进展的肾脏疾病。进展性肾病可导致患者需要接受透析和肾移植的治疗,并可能造成死亡。局灶节段性肾小球硬化是APOL1介导的慢性肾病的一种类型。
Inaxaplin是一款APOL1抑制剂,突破性疗法认定和PRIME药品认定的授予是基于它在治疗FSGS患者的2期临床试验结果。该试验共入组16例患者,在13例可评估患者中,在标准治疗的基础上联用inaxaplin治疗13周后,患者的尿蛋白/肌酐比值(UPCR)获得具有临床意义和统计学显著性的降低,平均降低47.6%(95% CI:-60.0%,-31.3%)。并且,治疗早期就观察到患者蛋白尿减少,疗效在整个13周治疗期间持续。无论患者基线指标或背景治疗如何,均获得一致积极结果。
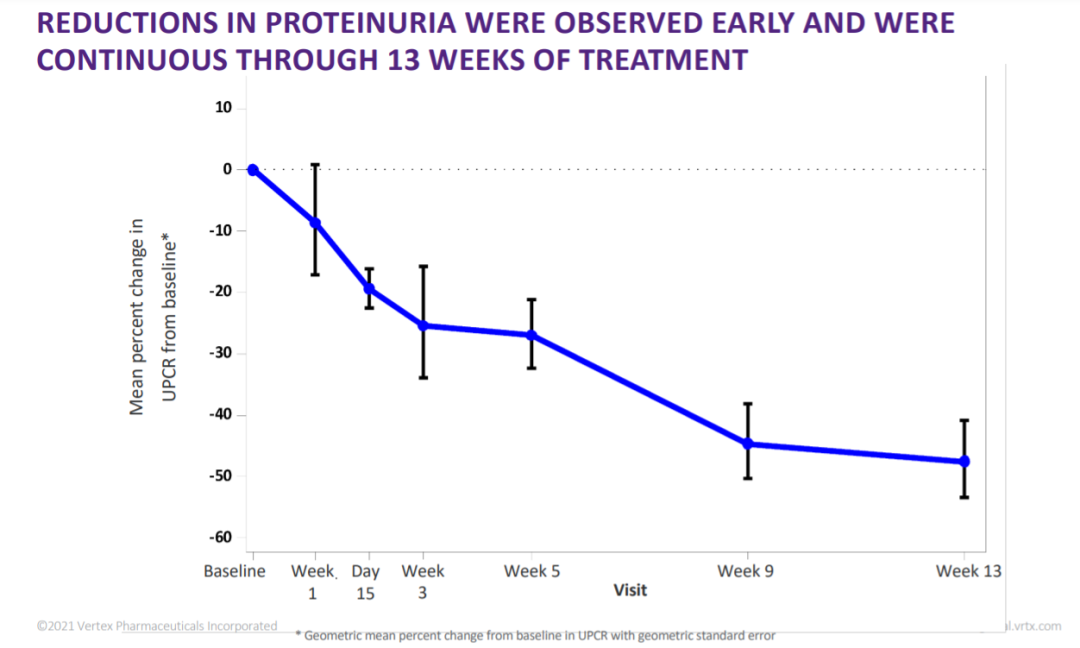
▲VX-147治疗早期就观察到蛋白尿指标下降,并且在13周疗程中持续下降(图片来源:参考资料[2])
目前,inaxaplin正在随机双盲,含安慰剂对照的2/3期适应性临床试验中接受评估。如果中期数据分析结果积极,可能作为Vertex寻求加速批准的基础,用于治疗AMKD患者。
参考资料:
[1] Vertex Announces Inaxaplin (VX-147) Granted Breakthrough Therapy Designation by U.S. FDA and Priority Medicines (PRIME) Designation by the EMA. Retrieved June 8, 2022, from https://www.businesswire.com/news/home/20220608005181/en
[2] Vertex Announces Positive Results From Phase 2 Study of VX-147 in APOL1-Mediated Focal Segmental Glomerulosclerosis. Retrieved December 1, 2021, from https://www.businesswire.com/news/home/20211201005492/en
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「药明康德」微信公众号回复“转载”,获取转载须知。








 个人中心
个人中心
 我是园区
我是园区




