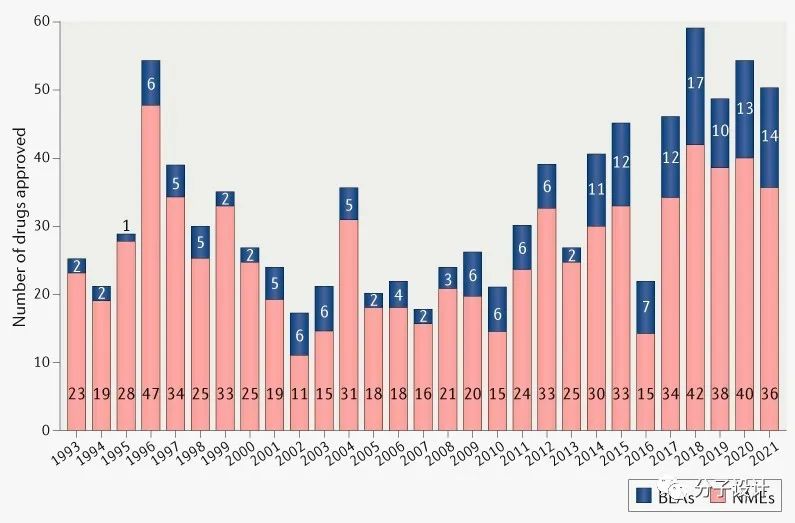
2021年,美国 FDA 药物评价和研究中心(Center for Drug Evaluation and Research, CDER)共批准了50种新药,其中新分子实体(New molecular entities, NME)36种,生物制剂许可申请(Biologics license applications, BLA)14种,总数基本与近5年的平均水平持平(51种)。
从药物的创新性来看,
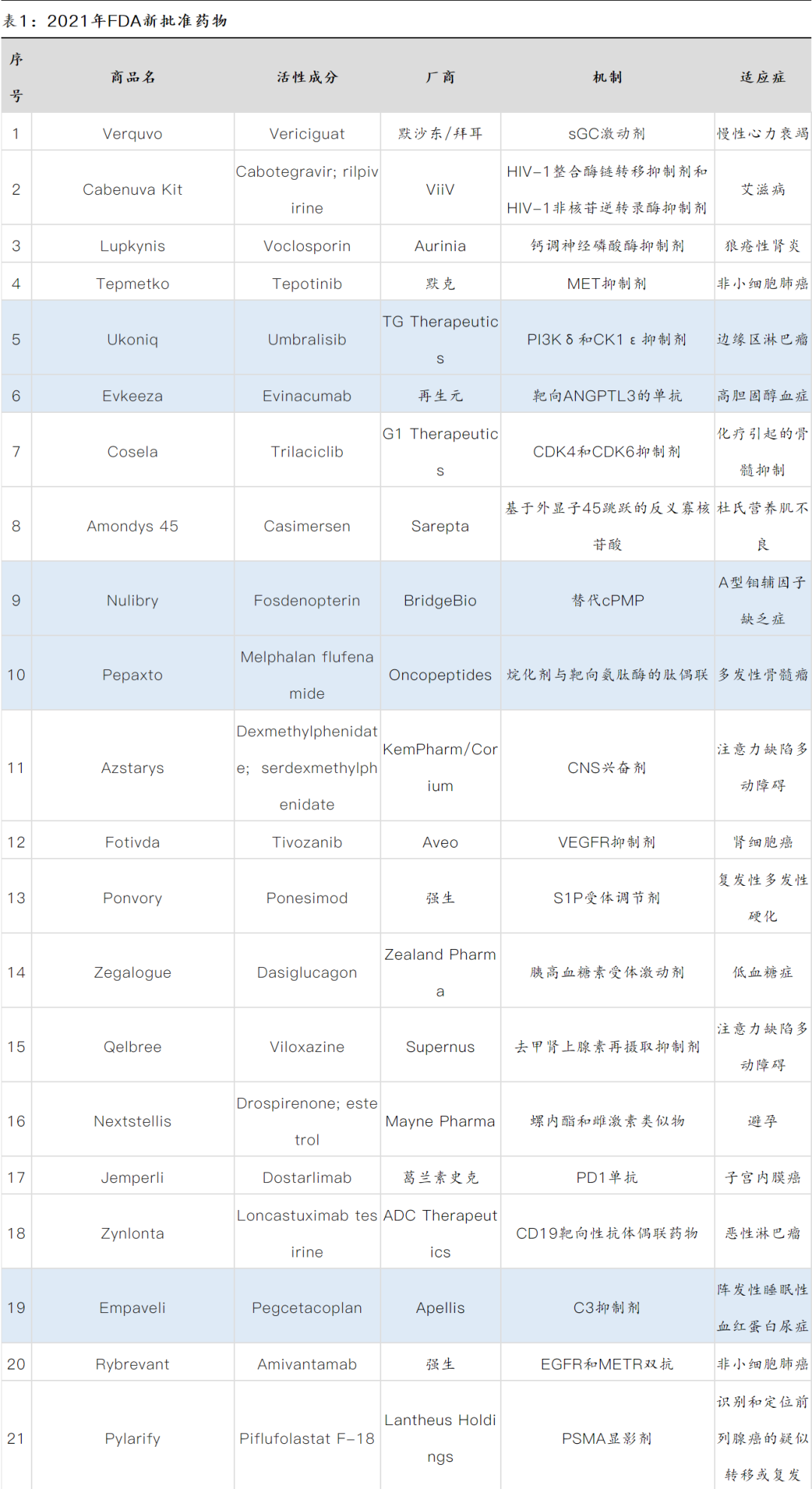
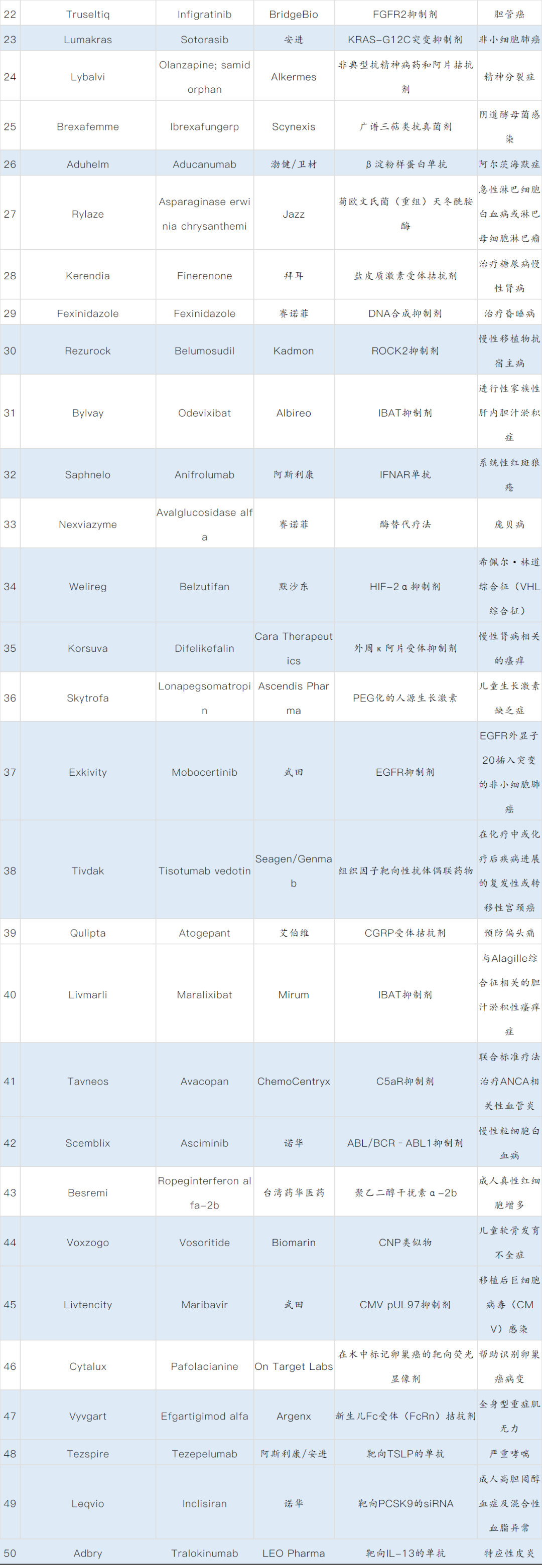
2021年共有21款新药属于First-in-class药物,占到获批总数的42%(
下表中蓝色标记为First-in-class药物)
,其中包括
Lumakras
:攻克了KRAS不可成药的难题,特异性靶向KRAS-G12C突变体的共价抑制剂,可将KRAS锁死在失活状态;
Cabenuv
a
:首款HIV长效注射疗法,每月只需进行一次治疗,一年给药仅12天;
Aduhelm
:首个治疗阿尔茨海默症病因的药物,它能够选择性地与患者大脑中的淀粉样蛋白沉积结合,借助免疫系统清楚沉积蛋白;
Welireg
:诺奖靶点的首个抗癌药物,可以选择性地阻断HIF-2α和HIF-1β相互作用,减少HIF-2α靶基因的转录和表达;
Rybrevant
:首款获批靶向不同肿瘤抗原的双抗药物,目前已被NMPA纳入突破性治疗品种,在中国开展多项临床试验;
Zynlonta
:首款靶向CD19的ADC,之前上市ADC药物的靶点包括CD33,CD30,CD22,CD79β,HER2,Nectin-4,Trop-2,BCMA;
Pepaxt
o
:首款抗癌肽-药物偶联物,借助多肽的亲脂性易于被肿瘤细胞摄取,多肽在细胞内被肽酶水解后,释放出亲水性的烷化剂;
Leqvio
:全球首款且唯一一款降低低密度脂蛋白的siRNA药物,该药在初始注射及第三个月注射治疗后,每年仅需两次治疗即可取得长效控制
。
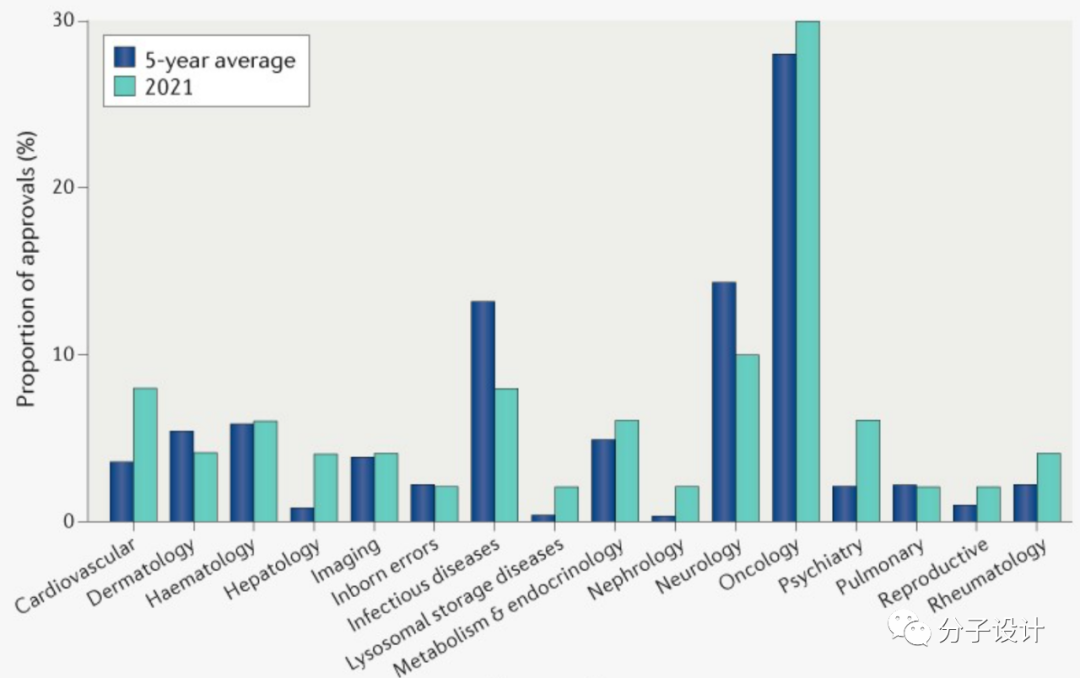
从获批的适应症来看,癌症药物仍然占据主导地位,占到新批准药物的30%(15项)
,而癌症药物批准的5年平均值为28%。
神经科药物连续第三年获得第二多的批准,2021年占到新批准的10%(5项)
。传染病和心血管疾病药物并列第三,各占到8%
(4项)
。
1. 癌症领域,
2021年最引人瞩目的进展大概是KRAS-G12C抑制剂的获批,遗憾的是JCI杂志刚刚报道了肿瘤对这款药物耐药性的出现。
另一个广受关注的靶点是HIF-2α,这个诺奖级靶点的首个抑制剂也于2021年获批。抗体药物依旧集中于PD1/PDL1、EGFR、CD19等炙手可热的靶点,当然还有BCMA,也是细胞疗法的主要靶点。
2. 阿尔兹海默症,渤健和卫材的β淀粉样蛋白抗体Aducanumab是今年FDA最具争议性的批准。渤健在2019年初对两项Ⅲ期试验的分析中没有发现活性证据,因而停止了开发。但该公司重新分析数据后,发现了一丝效果,又提交了批准。
2020年11月一个独立的FDA咨询小组以10票对0票反对了这项批准,然而FDA利用加速审批途径,根据其降低淀粉样蛋白水平的能力
(一个未经证实的替代终点)
为aducanumab开了绿灯。不过欧盟和日本对这款药物仍持谨慎态度。
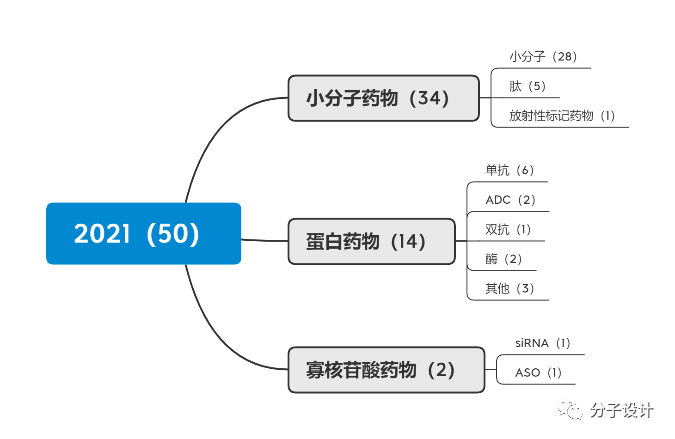
3. 从获批的药物类型来看,2021年生物药的品种更为丰富,包括2款酶学疗法、1款双抗、1款限制性肽(constrained peptide)。此外,2021年4月22日获批的PD-1抗体Jemperli是FDA批准的第100款抗体药(“小分子”包括所有长度不超过40个氨基酸的肽;小分子和寡核苷酸作为NMEs被批准,蛋白类药物作为BLAs被批准)。
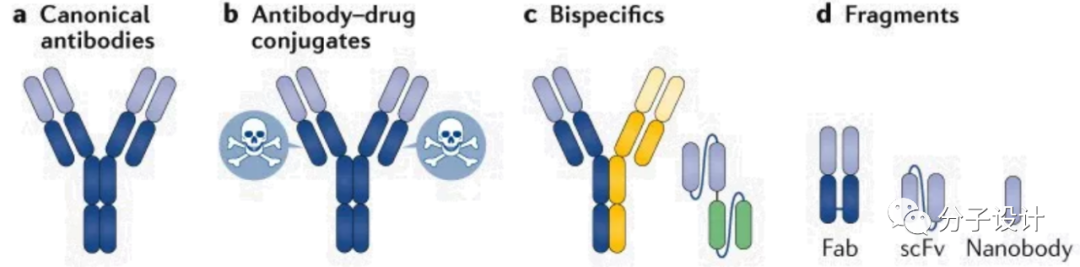
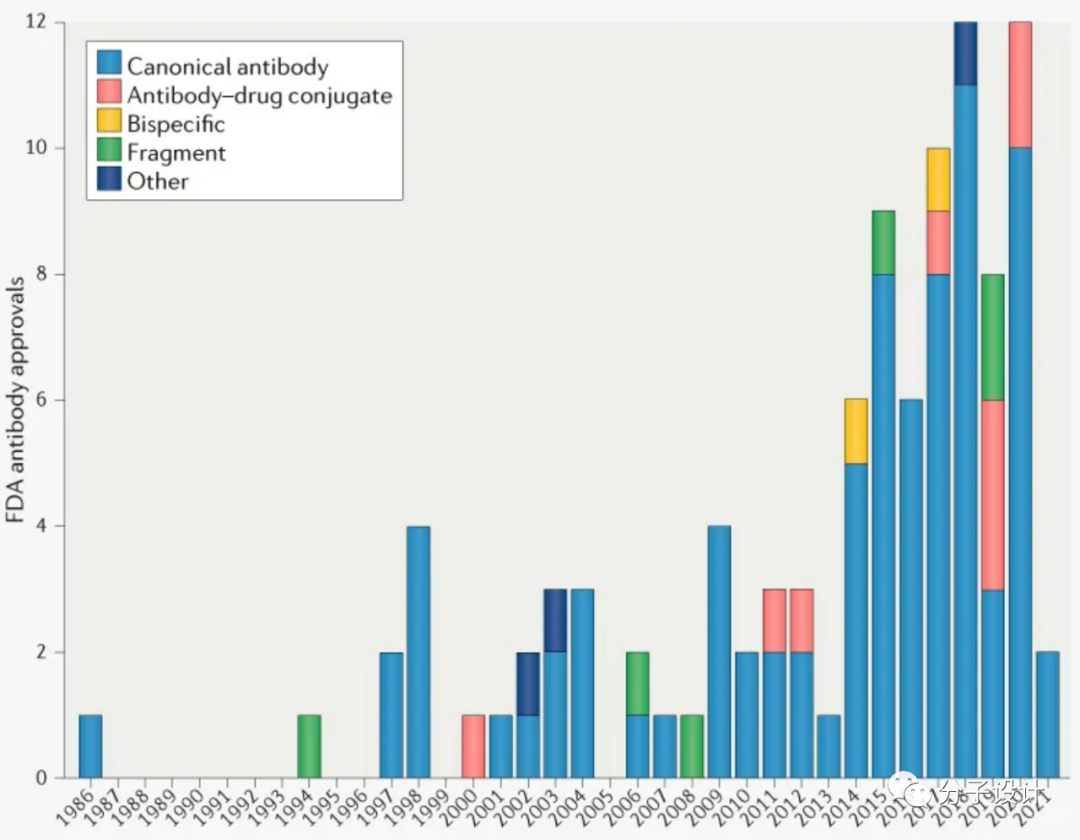
4. 抗体类药物厚积薄发,处于飞速发展时期。抗体药物的概念自1975年被提出来之后,直到1986年FDA才批准了第1个单抗药物。而在之后的20多年间,抗体类药物进入技术积累期,获批寥寥无几。2014年之后,抗体药物的研究开始大规模兑现。
FDA从第1个抗体药物到第50个用了29年,而从第50个到第100个仅用了6年。不过目前抗体类药物面临着适应症和靶标严重同质化的问题,癌症占到获批的41%,前10靶标占到获批的42%。
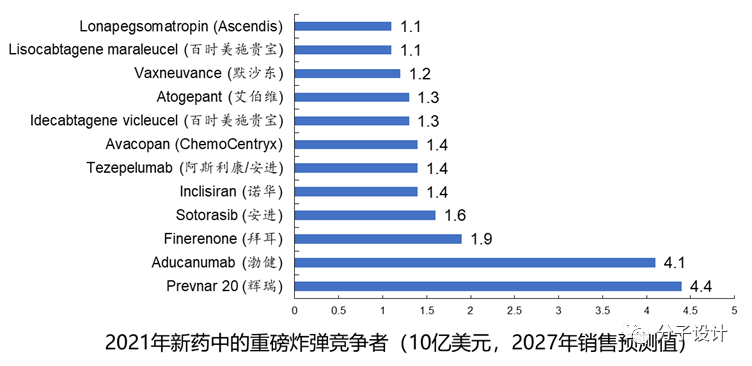
5. 从获批药物的销售潜力来看,2021年这批新药的市场前景并不乐观。据Clarivate Analytics的分析师评估,2027年销售额可超过20亿美元的新药仅有两款,其中辉瑞的Prevnar20是疫苗产品,药物中仅有渤健的Aducanumab具有相应的潜力。但鉴于这款阿尔茨海默症药物在上市中引发的巨大争议,41亿美元的销售预期仍有待考量。
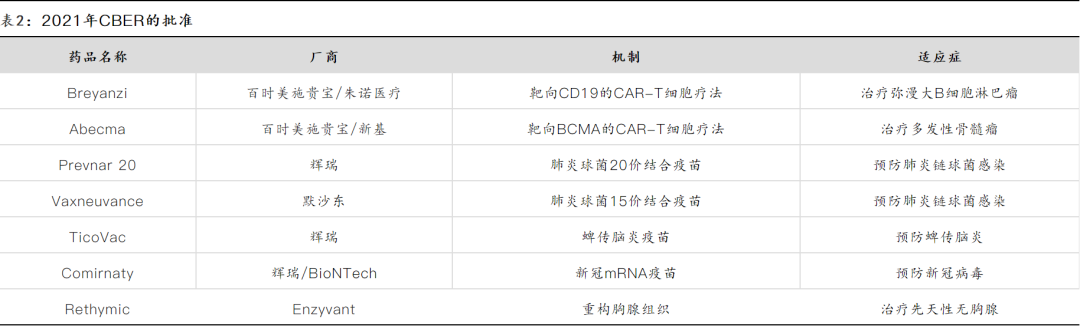
6. 2021年CBER
(生物制品评价与研究中心)
共批准了7款新产品,包括2款CAR-T细胞疗法,2款肺炎结合疫苗,1款新冠mRNA疫苗。辉瑞新冠疫苗2021年的全球销售额被预测为350亿美元,可能打破2019年阿达木单抗210亿美元的商业记录。

7. 2022年值得关注的新药包括2款治疗阿尔兹海默症的单抗,然而新的AD药物是否能够成功取决于FDA是否继续以加速审批进行支持。此外,百时美施贵宝为了应对来那度胺的专利悬崖压力,心肌病和银屑病的2款药物也有望在2022年获批。新机制方面,礼来治疗2型糖尿病的GIP/GLP-1双靶点激动剂以及Alnylam治疗hATTR的RNAi疗法备受市场关注。

参考文献:
Asher Mullard, 2021 FDA approvals. Nat Rev Drug Discov. 2022, doi: 10.1038/d41573-022-00001-9
















 个人中心
个人中心
 我是园区
我是园区




