▲点击上方的蓝色“医谷”关注我们

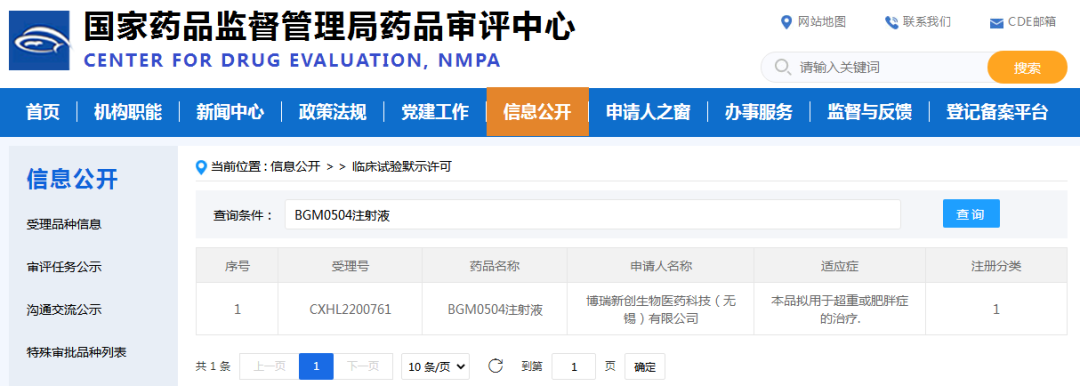
近日,据国家药监局药审中心官网信息显示,博瑞医药子公司博瑞新创生物申报的葡萄糖依赖性促胰岛素多肽(GIP)和胰高血糖素样肽-1(GLP-1)受体双重激动剂BGM0504注射液获批临床试验,拟开发适应症为用于超重或肥胖症的治疗,这也是继豪森药业HS-20094之后国产第2款获批减重适应症临床的GIPR/GLP-1R激动剂。
据了解,GIP是一种激素,可以补充GLP-1受体激动剂的作用,临床前模型已证明GIP可以减少食物摄入并增加能量消耗,从而使体重减轻,并且GIP与GLP-1受体激动剂联合使用时,可能会对血糖和体重产生更大的影响。
根据博瑞医药方面的介绍,BGM0504作为一款GLP-1和GIP受体双重激动剂,可激动GIP和GLP-1下游通路,产生控制血糖、减重和治疗NASH等生物学效应,展现多种代谢疾病治疗潜力。
目前,全球范围内共计有超20款GIPR/GLP-1R双重激动剂在研,其中进展最快的是礼来的tirzepatide(替尔泊肽),其于今年5月获得美国FDA批准,用于与控制饮食和锻炼联用改善成人2型糖尿病患者的血糖控制,商品名为Mounjaro,定价为974美元,根据礼来季度财报,Mounjaro上市四个月的全球销售业绩为1.87亿美元。
现阶段,tirzepatide还在进行减重适应症的开发,截止目前,其减重适应症尚未在任何国家和地区获得批准。不过,今年10月,礼来方面宣布,FDA已授予tirzepatide快速通道指定,用于治疗成人肥胖或超重以及体重相关的并发症,根据与FDA的讨论,礼来将滚动提交tirzepatide针对成人肥胖或超重的上市申请。
在中国,tirzepatide用以改善成人2型糖尿病患者血糖控制的上市申请已获得国家药监局受理,用于成人超重和肥胖者的药物干预治疗,降低其主要心血管事件的风险,减少2型糖尿病发生风险和改善肾脏结局的临床试验也已获得批准。
据咨询机构普华有策发布的研报,全球肥胖药物市场规模已从2016年的18亿美元增长到2020年的26亿美元,年复合增长率高达9.0%,并将于2030年超过115亿美元。中国肥胖药物市场规模则由2016年的2.6亿元急速增至2020年的19亿元,年复合增长率高达64.6%。同时,受肥胖人群增加,体重管理意识增强,新的减肥药上市等因素驱动,2025年中国肥胖药物市场规模将达到87亿元,并将继续保持高速增长,将于2030年接近150亿元。
文 | 医谷
推荐阅读
《首次实现药物减重超20%,礼来tirzepatide三期结果出炉》


寻求广告投放、会议合作、企业传播、人事招聘等欢迎联系400-689-7892。



 个人中心
个人中心
 我是园区
我是园区





