
点评 | 高路(海军军医大学)、袁佳(山东大学)
责编 | 兮
粘附类G蛋白偶联受体
(adhesion G protein-coupled receptors, aGPCRs)
是G蛋白偶联受体
(G protein-coupled receptors, GPCRs)
超家族中的第二大家族,有33个成员,分为9个亚家族。aGPCRs在许多重要生理过程中起到关键分子开关的作用,调控免疫反应、大脑发育、血管生成、骨骼生长、生殖及细胞命运决定等
【1】
。尽管aGPCRs调控多种生理功能,但大多数aGPCRs仍是孤儿受体,配体信息非常有限,限制了对其生物学效应的研究。作为粘附类受体G家族的成员之一,粘附类受体ADGRG2,
(又称GPR64或人附睾基因产物6)
,在男性生殖中发挥重要的调控作用。ADGRG2基因敲除的雄性小鼠精子数目减少,生殖力下降【2】,在人类中也发现ADGRG2的突变与男性不育密切相关【3】,因此ADGRG2被认为是治疗男性不育的潜在药物靶点。然而ADGRG2的内源性配体尚未发现,极大的限制了对其功能的深入研究和干预策略开发。
山东大学孙金鹏教授和于晓教授团队长期关注粘附类GPCR的配体发现、生理功能和信号转导机制研究。前期研究发现ADGRG2在附睾输出小管的非纤毛细胞顶膜与CFTR偶联形成信号复合体,调控氯离子电流以及输出小管的重吸收过程,对于精子运输和成熟至关重要
(eLife 2018 ;7:e33432)
。团队优化了ADGRG2本身的stachel序列,获得了高亲和力的ADGRG2激动剂,为ADGRG2的功能研究提供了有力工具。此外,团队和山东大学易凡教授合作,通过大规模筛选发现糖皮质激素可以激活粘附类受体G家族的另一成员GPR97
(ADGRG3)
发挥快速作用,并联合药物所徐华强教授和浙江大学张岩教授解析了糖皮质激素-GPR97复合物的冷冻电镜结构
(详见BioArt报道:Nature | 孙金鹏/张岩/徐华强合作揭示黏附类受体GPR97感知糖皮质激素并激活Go的结构基础,Nature, 2021, 589: 620-626,高被引论文)
,解开了几十年来学界中糖皮质激素快速作用的机制之谜。延续此工作,孙金鹏和于晓课题组鉴定出粘附类受体GPR126
(ADGRG6)
是孕酮和17-羟基孕酮的膜受体,阐明了孕酮和17羟基孕酮作用于GPR126调控乳腺癌发生发展的作用机制
(详见BioArtMED报道:PNAS | 孙金鹏/于晓/肖鹏团队揭示孕酮作用新机制,PNAS, 2022; 119 (15) e2117004119)
。通过系列研究揭示了识别固醇类激素的GPCR亚家族。
2022年8月18日,山东大学于晓、孙金鹏教授研究团队与南方科技大学刘忠民教授团队通力合作,在以前的工作基础之上,共同在Nat Chem Biol杂志上在线发表了文章
Structures of the ADGRG2-Gs complex in apo and ligand bound forms
。该研究
发现的类固醇激素配体脱氢表雄酮(DHEA)、硫酸脱氢表雄酮(DHEAS)是粘附类孤儿受体ADGRG2的内源性激动剂,而且类固醇激素去氧皮质酮DOC是ADGRG2的内源性拮抗剂。并解析了DHEA与其膜受体ADGRG2结合的复合物电镜结构。这项研究结果是识别类固醇激素的GPCR亚家族领域又一新进展,重塑了多年来人们对类固醇激素作用机制的认知。
脱氢表雄酮
(
DHEA
)
和硫酸脱氢表雄酮
(
DHEAS
)
是人循环系统中含量最丰富的激素,也是性类固醇雌激素和雄激素的前体。DHEA和DHEAS可以与核受体结合调节基因的转录,但多项研究表明它们除了激活核受体,还可以通过膜受体介导快速作用,比如DHEA可诱导小鼠胚胎新皮层神经元细胞内钙的快速增加;DHEA还可以与血管内皮细胞上的未知膜蛋白结合,激活MAPK通路诱导细胞增殖等;DHEAS则可快速诱导大鼠嗜碱性细胞白血病细胞释放媒介物β-己糖胺酶等。有些快速作用与胞内第二信使Ca2+、cAMP等密切相关,提示DHEA和DHEAS很可能具有GPCR膜受体。然而,该膜受体一直未能真正确证。
在本研究中,该团队解析了Apo状态下的ADGRG2-Gs复合物电镜结构,发现在受体7TM上端有一个开放的潜在配体结合口袋,通过对类固醇小分子库中进行系统性筛选,发现并鉴定出ADGRG2的激动剂DHEA、DHEAS和中性拮抗剂去氧皮质酮
(Deoxycorticosterone, DOC)
,这些配体特异性激活或阻断ADGRG2下游Gs信号通路
(图1)
。
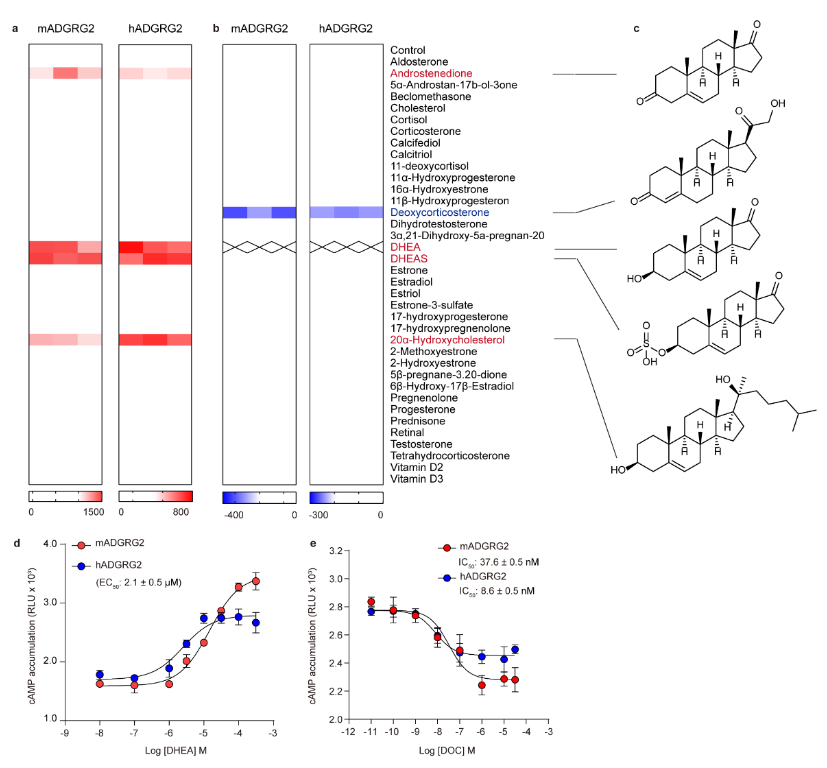
图1 ADGRG2的类固醇激素配体鉴定,DHEA与DHEAS为激动剂,DOC为拮抗剂
研究人员进一步通过单颗粒冷冻电镜技术解析了DHEA-ADGRG2-Gs高分辨率结构,详细阐释了DHEA与ADGRG2相互作用,激活该受体,并与G蛋白偶联的清晰过程。此外,通过分子动力学模拟方法预测了DOC-ADGRG2结合模式,揭示了类固醇激素中性拮抗剂阻断激动剂诱导的Gs信号的作用机制。
图2 ADGRG2的类固醇激素配体筛选及相互作用分子机制示意图
综上所述,
本研究中鉴定出粘附类受体ADGRG2的类固醇激素配体,实现了ADGRG脱孤,并详细阐释了ADGRG2识别不同类固醇激素的分子机制。这些新发现的ADGRG2配体为进一步研究该受体在生殖系统中的功能提供了有用工具,也为靶向ADGRG2治疗男性不育的药物设计奠定了理论和结构基础。
山东大学于晓教授,孙金鹏教授、易凡教授和南方科技大学刘忠民教授为该论文的共同通讯作者。山东大学博士研究生林慧和郭盛超,基础医学院杨照研究员、南方科技大学博士研究生卜瑞倩,以及清华大学袁道鹏博士该论文的共同第一作者。该工作的许多研究结果是和生殖领域多位知名专家,包括山东大学赵晗教授、四川大学徐文明教授、南通大学曾旭辉教授、和北京大学第三医院林浩成副研究员合作取得。
原文链接:
https://www.nature.com/articles/s41589-022-01084-6
近年来,人类的不孕不育率持续上升,不孕不育症已成为继癌症和心血管疾病之后第三大最常见的公共卫生问题,并且有可能随着人口老龄化和环境问题而日趋严重。将近7%的男性存在生育问题,精子发育缺陷,精子活力下降以及精卵结合障碍等,都会导致男性不育。然而,由于导致男性不育的作用机制较为复杂,长期以来缺乏有效的药物靶点和干预手段。GPCR是重要的药物靶点,目前上市临床药物有34%的直接作用靶点为GPCR。孙金鹏教授团队和他的合作团队长期从事膜受体GPCR的相关研究。他们前期已发现附睾中高表达的粘附类受体ADGRG2与男性生殖密切相关,并发现ADGRG2与囊性纤维化跨膜电导调节因子
(Cystic fibrosis transmembrane conductance regulator, CFTR)
偶联,调控男性输出小管中的氯离子电流和水盐代谢平衡,阐明了ADGRG2功能障碍导致男性不育的作用机制。然而由于ADGRG2是孤儿受体,内源性配体的缺失严重阻碍了ADGRG2在男性生殖的功能研究和靶向药物开发。
在本文中,孙金鹏教授及其合作团队通过高通量筛选成功实现了ADGRG2脱孤,发现了DHEA和DHEAS是ADGRG2的内源性激动剂,而DOC是ADGRG2的中性拮抗剂。利用单颗粒冷冻电镜技术解析了激动剂DHEA作用下ADGRG2与Gs蛋白三聚体复合物结构,进一步阐释了ADGRG2识别类固醇激素的分子机制,拓宽了类固醇激素的GPCR受体亚家族研究领域。值得注意的是,DHEA和DHEAS是能够调控生殖功能的重要类固醇激素,它能提高睾丸和附睾中雄激素的水平,也可以改善卵巢储备功能下降患者的卵巢环境,增加怀孕几率。ADGRG2作为DHEA和DHEAS的膜受体,与其调控男性生殖的重要功能相符,并且提示ADGRG2可能在女性生殖过程中也起到潜在的调控作用,值得进一步深入研究。另外基于DHEA-ADGRG-Gs复合物结构基础,可对DHEA和DHEAS进行结构改构和优化,有希望发展出靶向ADGRG2的高亲和力配体,为男性不育症的潜在治疗方案提供了新的思路和干预策略。从陈宜张院士提出甾体激素作用的非基因组机制学说至今已过去了三十余年,今年3月先生还在我室的一次学术交流中提到甾体激素膜受体鉴定发展的心愿。孙金鹏教授和于晓教授团队近年来在甾体激素GPCR受体领域的开创性工作,不仅是对陈先生学说有力的实验证明,更是对膜受体在不同系统作用的进一步拓展和完善。
近年来对粘附类GPCR的研究发现,该类受体广泛参与组织发育和器官生理活动,调控多种人类疾病,是极具前景的治疗靶点。ADGRG2
(又称为GPR64)
是直接参与生殖调控的重要粘附类受体,缺失ADGRG2导致男性输出小管内液体再吸收失调, 致使液体在附睾内淤积及精子停滞在输出小管内最终引发雄性不育。2018年,山东大学孙金鹏教授,于晓教授和易凡教授团队揭示了ADGRG2-Gq/β-arrestin-1/CFTR调控输出小管液体再吸收的分子机制,为ADGRG2参与的男性生殖疾病指明新的治疗策略。
近日,孙金鹏教授和于晓教授团队使用冷冻电镜深入阐明ADGRG2蛋白结构,并进一步发现脱氢表雄酮
(DHEA)
是ADGRG2的配体,这一结果令人惊喜,让我们对粘附类GPCR在生殖调控中的作用有了新的认识和期待。DHEA作为重要的性激素间接前体,调控成年男性50%的雄激素以及绝经前女性75%的雌激素生成。临床上使用DHEA改善生育力,特别是用于卵巢早衰以及辅助生殖治疗以维持和促进女性卵巢功能,尽管DHEA的过度使用也会引发一系列副作用。DHEA作为ADGRG2激动剂这一发现,有助于改善DHEA激活ADGRG2产生的不良反应,打开了探索粘附类GPCR蛋白在雌性生育力调控作用的新篇章。
接下来的工作依然极具挑战性,根据现有研究ADGRG2在卵巢中表达量较低,是否其在卵巢特定细胞群行使作用,如卵泡膜细胞,还需要进一步定位;其次,是否有其他粘附类GPCR与DHEA结合也值得关注;并且 DHEA在人类中的表达远超实验室动物,因此制备适当的动物生育力干涉模式亦是需要面对的难关;更重要的是,是否还有其他的粘附类GPCR蛋白参与生育力调控。
全球约有15%的夫妻面临不育问题,我国不育人口也逐年攀升,粘附类GPCR作为重要的药物靶点,在生殖疾病方面的研究依然非常有限。山径之蹊间,介然用之而成路,粘附类GPCR蛋白在生殖领域的进一步探索让人翘首以盼。
制版人:十一
1 Lala, T. & Hall, R. A. Adhesion G protein-coupled receptors: structure, signaling, physiology, and pathophysiology. Physiol Rev 102, 1587-1624, doi:10.1152/physrev.00027.2021 (2022).
2 Davies, B. et al. Targeted deletion of the epididymal receptor HE6 results in fluid dysregulation and male infertility. Mol Cell Biol 24, 8642-8648, doi:10.1128/MCB.24.19.8642-8648.2004 (2004).
3 Khan, M. J. et al. X-linked ADGRG2 mutation and obstructive azoospermia in a large Pakistani family. Sci Rep 8, 16280, doi:10.1038/s41598-018-34262-5 (2018).
【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。











 个人中心
个人中心
 我是园区
我是园区





