
随着新修订的《药品管理法》、《药品注册管理办法》和《药品记录和数据管理要求》等法规的实施,对药品研发企业或药品生产企业的研发部门的研发过程质量保证提出新的挑战。
因此为了帮助大家解决在建立研发质量管理体系过程中面临的困惑,特开设本次课程,本次培训支持企业全员考试,考试合格的同学将颁发电子版培训证书,欢迎相关人员咨询参加。
时间地点
培训地点:药视网 网络讲堂
组织单位
药视网
徐州易云企业服务有限公司
蒲公英、药聘网、药林网
1、制药企业和新药研究机构的研发人员、注册人员、检验人员;
2、药品生产企业研发技术与质量管理负责人、QA、QC;
3、新药研发CRO实验室人员;
4、各高等院校、科研院所、医疗机构等相关专业人员。
课程内容
一、药品研发风险识别和质量管理体系构建
二、研发质量管理文件体系
三、研发质量体系运行管理
四、研发注册现场检查
嘉宾介绍

培训模式
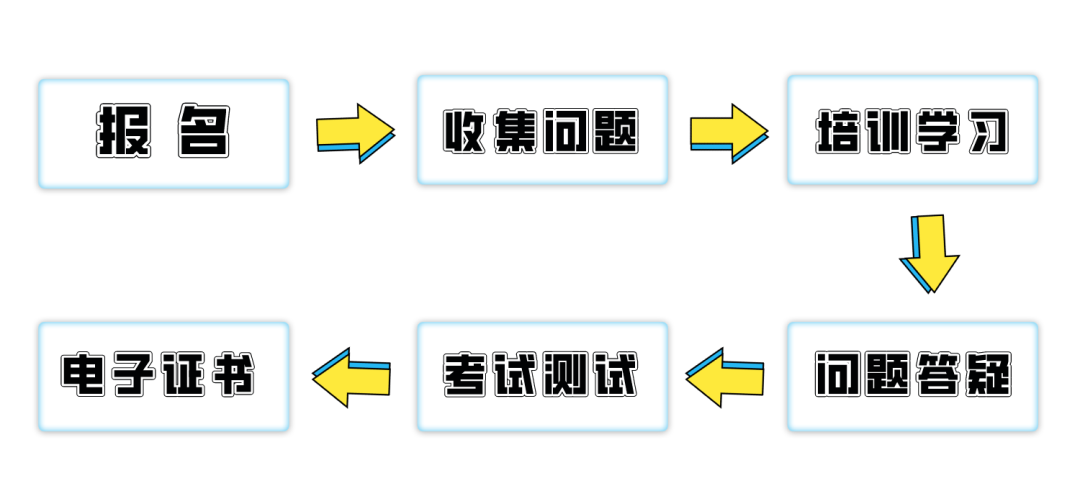
培训特点
1、更专业,更贴心
培训侧重答疑,在培训开始前请各参会企业务必向会务组提交在员工间收集的问题,会务组会和讲师接洽协商,将企业提供的问题融入到课程之中,并且会最大程度的延长答疑时间,以期帮助员工最大程度的解决日常工作中遇到的问题。
2、更方便,更高效
只需要一间会议室+一套投影设备,参会企业可以组织员工一起学习,培训过程中可以同公司同事边交流边学习,培训效果也会更好。
1家企业只需要买1个直播间账号,1个人线下培训的成本可以让n个人接受培训。
去外地参加培训,会有将近一半的时间浪费在路上,旅途的奔波也很辛苦,网络讲堂会使我们节省时间免受旅途奔波的辛苦。

部分企业网络学习展示



费用说明
1、A类票:3500元/端口(含药视网年度VIP/授课费/发票)
2、B类票:2800元/端口(含授课费/发票)
3、药视网年度VIP:500元/端口(含授课费/发票)
4、药视网企业VIP:提供一个免费端口
户名:徐州易云企业服务有限公司
开户行:中国工商银行徐州市淮海东路支行
账号:1106020409210313389
(付款请注明“研发质量”)

报名咨询
VIP权益
2、年度VIP有效期内可免费参与药视网线上直播答疑课(全年约5场)
3、年度VIP有效期内可优惠参与药视网举办的线下培训班(不低于8场)

详情咨询



 个人中心
个人中心
 我是园区
我是园区




