
● 从靶点上来看,TNF-α 仍然为第一大靶点,市场规模 352 亿美元。PD-1/PD-L1 紧随其后,市场规模为 332 亿美元,2022 年即将超越 TNF-α 登顶。VEGF 靶点排在第 3 位,市场规模为 182 亿美元,其中眼病(Eylea、Lucentis、Beovu、Vabysmo)即达到 130 亿美元。
● 新冠中和抗体列在第 4 位,试产规模 110 亿美元,其中再生元/罗氏中和抗体为 76 亿美元,礼来中和抗体为 22 亿美元。HER2 靶点接近百亿美元,Perjeta 和 DS-8201 成为新的增长点。Th17 通路已经诞生多个重磅炸弹,包括 IL-12/IL-23、IL-23、IL-17 等靶点,合计市场规模达到 215 亿美元。
第一代抗体药物已经进入生物类似药时代,抗体药物的生命周期相比小分子有所延长,但仍然挡不住原研药业绩快速下滑的趋势。
● PD-1/PD-L1 今年即将取代 TNF-α 成为抗体药最大的靶点,Th17、Th2 则成为自免领域最重要的增长点。一些老靶点则因为新药物形式焕发生机,如 CD20、HER2 等。一些罕见病抗体药快速增长,如 C5(PNH、NMOSD 等)、KLK(HAE)、IGF-1R(甲状腺眼病)。国产抗体药如何进军欧美市场,也是未来两年的重要看点,目前第一道关卡是监管政策,获批后还要面临潜在的 IP 挑战和市场竞争等。
● 新冠中和抗体方面,再生元/罗氏的中和抗体销售额高达 76 亿美元,礼来/君实的中和抗体销售额 22 亿美元。不过由于 Omicron 的流行,两者对其都失去活性,已经被 FDA 限制使用。
● 2021 全球抗体药物融资事件约 46 起,融资总额约 441 亿元(折合约 70 亿美元)。
● 其中,中国融资 32 起,总额约 346 亿元(54.85 亿美元),约占融资总额的 77%。融资轮次多集中在 A、B 轮及 IPO 环节。治疗领域以肿瘤、自身免疫性疾病为主。
从融资地区来看,中国为 2021 年抗体领域的主要融资市场,以 32 起融资事件居于首位;美国以 10 起居于其次,此外,瑞士、新加坡、英国均有企业涉及。
● 如今,在开发新抗体疗法以及现有分子现代化生产的过程中,降低患者和政府的药品成本(如何拓宽获得药品的渠道)成为了关键的动力。
● 降低成本包括提供强大的工艺制造过程,这些过程可以快速、可转移到世界各地的多个生产地点,并且生产工艺过程需要足够灵活,可接受并更新下一代技术和工艺过程,同时确保产品质量。
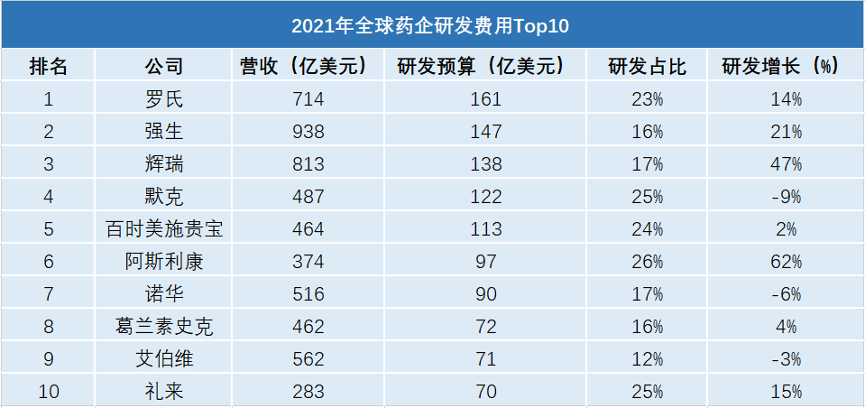
(数据来源:药融云数据库、公开资料)


随着抗体药研发投入的提升,获批数量显著增加,市场占有率不断攀升,已经成为生物药中增长最快的领域。同时随着对抗体药需求的提升,对于抗体技术和工艺也提出了新的要求和挑战。在各位制药同仁们的不断努力下,抗体技术和工艺在短短 10 年中不断改进,技术层面上从最初的不锈钢到现在的一次性。培养工艺从最初的批次、流加,发展到最新的灌流。
作为下一代细胞培养工艺,灌流模式的上游生物工艺为细胞和生物制剂的工业生产提供了广阔的前景。在灌流过程中,将新鲜培养基不断添加到生物反应器中,并将细胞保留在生物反应器中,同时收获已经用过的培养基。因此,细胞培养基的组成在此过程中可以保持相当的恒定。
这提供了几个优点,在灌流过程中,可以达到比在分批和补料分批过程中更高的细胞密度,从而提高体积生产效率。由于培养基成分会影响细胞代谢并因此影响产品特性,因此工艺条件越稳定,产品质量可能越一致,通过细胞保留装置保留细胞,同时不断收获培养液所产生的产品质量是较为稳定的。
除了用于生产分泌蛋白或病毒载体外,灌流还可用于一些生物过程的早期步骤,如生产高密度种子序列或在转染/感染细胞以生产病毒载体之前实现高细胞密度。在所有情况下,灌流生物处理都需要在生物反应器内或连接到生物反应器上的细胞保留装置。保留技术的选择取决于是培养贴壁细胞还是悬浮细胞、可溶性蛋白质、病毒或细胞本身是否是我们感兴趣的产物、产品是否需要连续收获、工艺流程是否需要可扩展和其他因素。
据估计,从 2020 年到 2030 年,全球连续生物工艺市场将以 23% 的复合年增长率扩大,价值达到 3.1 亿美元。
一次性生物加工设备在短短十年内就彻底主导了商业前生物制药生产。然而,即使有了这一突破,生物制药设施的性能和成本压力仍在继续增长。对更高生产力、更高效率和更低成本的需求正在不断推动上游改进。一些业内人士预测,灌流生物反应器技术可能是生物工艺的下一次革命。灌流可能会成为一种占主导地位的生物反应器技术,而分批补料系统作为一种久经考验的传统技术占据了地位。随着技术的发展,研究人员发现灌流可以提供许多成本和性能优势。此外,由于灌流过程比分批补料过程更接近稳态,它通常会产生更一致的产品——特别是对于对生物反应器内条件变化敏感的分子。
与分批进料系统不同,灌流系统不会积聚废物。表达的蛋白质被快速去除并可供纯化,对于易于不稳定的蛋白质而言,这是一个显着优势。灌流失败的批次成本也往往要低得多。如果发现污染,早期未受影响的收成仍可使用;如果污染发生得早,则浪费了相对少量的培养基和人力。相反,如果在分批补料过程中发生故障,则必须丢弃整批。一旦建立灌流生物反应器的生物处理在许多情况下可以更简单并且经历更少的故障。此外,在细胞与固体基质结合的灌流系统中,细胞生长更自然,并且创伤性混合搅动和剪切力更小。
BioFlo® 320 生物工艺控制器
BioFlo® 320 生物工艺控制器是 Eppendorf 作为生物工艺设备制造商迈向未来的一步。
新功能
新功能包括可高压灭菌和一次性使用容器的灵活性、智能传感器和用于多单元控制的IP网络通信,使其成为台式生物工艺市场中新的优质选择。
适用于微生物和细胞培养、从放大到缩小、分批、分批补料和连续过程,可以满足生物技术和制药行业所有领域不断变化的需求。它提供了灵活性、更好的控制和最大的功能,同时只占用了类似系统宝贵实验室空间的一小部分。
抗体生产工艺比较
我们使用 Eppendorf BioFlo® 320 进行实验控制,对比了多种抗体生产方法。(即分批法、流加法、灌流法)。同时我们比较了两种采用不同细胞截留方法的生物反应器的灌流工艺。第一个套组使用交替切向流 (ATF) 过滤装置, 利用中空纤维过滤器截留细胞。第二个套组使用填充床生物反 应器,在固体的支持基质上固定细胞并进行培养。此实验针对细胞生长情况、细胞存活率、代谢特征以及细胞表达 的产品总量,对这几种培养条件进行了比较。

(不同工艺的细胞密度峰值和抗体滴度对比,数据来源:《单克隆抗体生产培养方法对比》)
Eppendorf 具体实验方法及数据请下载白皮书:

增量改进
当前的灌流系统包含了数十年的增量改进:培养基、基因工程、膜和过滤器、氧合方法、泵、一次性设备和过程监控。这些已经解决了许多灌流之前的问题,包括高故障率。随着越来越多的供应商将此类系统提升到世界一流的当前良好制造规范 (CGMP) 制造规模和质量,以及从小规模制造开始采用更多的灌流系统,行业专业人士对灌流的态度可能会发生变化。最终,涉及更少公用设施和更少劳动力的更小、更便宜的灌流设施可能会取代用于商业产品制造的大规模补料分批生物反应器(固定不锈钢和一次性)。
请注明:姓名+研究方向!


本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。




 个人中心
个人中心
 我是园区
我是园区





