
前列腺癌(Prostate Cancer, PCa) 是全球男性最常见的恶性肿瘤之一。雄激素 (androgen) 和雄激素受体(androgen receptor, AR)在驱动前列腺癌发生发展中起着关键作用。早期前列腺癌患者可通过手术或放疗来消灭肿瘤细胞,而对于复发或者发生转移的晚期患者,雄激素剥夺治疗(androgen deprivation therapy, ADT)是最主要的治疗手段。接受ADT治疗的患者在早期缓解之后,会出现治疗抵抗并发展成为去势抵抗性前列腺癌(Castration-resistant prostate cancer, CRPC)。AR信号通路的激活仍然是CRPC发展的重要因素,靶向AR配体结合域(LBD)的拮抗剂(或叫antiandrogen, 抗雄激素)是目前治疗前列腺癌的重要手段。然而,临床上广泛使用的AR拮抗剂,如恩杂鲁胺等,都会不可避免地引起耐药。其中重要的耐药机制是LBD结构域发生了突变,或者表达缺失了LBD结构域的AR剪接体AR-V7。因此,研究前列腺癌细胞对AR拮抗剂的耐药机制并寻找新的靶向策略对于治疗晚期的前列腺癌患者具有重大的临床意义。
近年来,科研人员发现转录因子、共激活因子和RNA聚合酶II等可以通过自身的无序区域(Intrinsically disordered regions, IDRs)介导液-液相分离(Liquid-liquid phase separation, LLPS),形成液态转录凝集体参与下游基因的转录调控。因此,靶向转录因子的液-液相分离有望成为针对转录因子这类“难以靶向”的蛋白开发小分子药物的有效策略。越来越多研究表明,蛋白质的异常液-液相分离与包括肿瘤、代谢性疾病、神经退行性疾病等人类重大疾病的发生发展密切相关。然而,蛋白质的液-液相分离在耐药过程中的作用研究并不深入。阐明生物分子凝集体在疾病发生发展乃至耐药中的生物功能研究将为我们开发全新机制的小分子药物开辟崭新的方向。
2022年10月13日,中国科学院生物与化学交叉研究中心朱继东/朱光亚团队与上海奕拓医药合作在Nature Chemical Biology在线发表了题为Targeting androgen receptor phase separation to overcome antiandrogen resistance 的研究论文。该研究揭示了AR的液-液相分离在抗雄激素耐药机制中起到了关键的作用,并提出了通过靶向AR液-液相分离克服抗雄激素耐药的新策略。

在这项研究中,科研人员发现雄激素二氢睾丸酮(dihydrotestosterone, DHT)可以诱导AR入核发生液-液相分离并形成激活的转录凝集体(图1a)。OptoIDR实验表明AR的相分离能力是主要由NTD结构域驱动的。由于AR-V7具有完整的NTD和DBD结构域,AR-V7即使在雄激素不存在的条件下仍然可以进入细胞核,并形成转录凝聚体(图1b)。
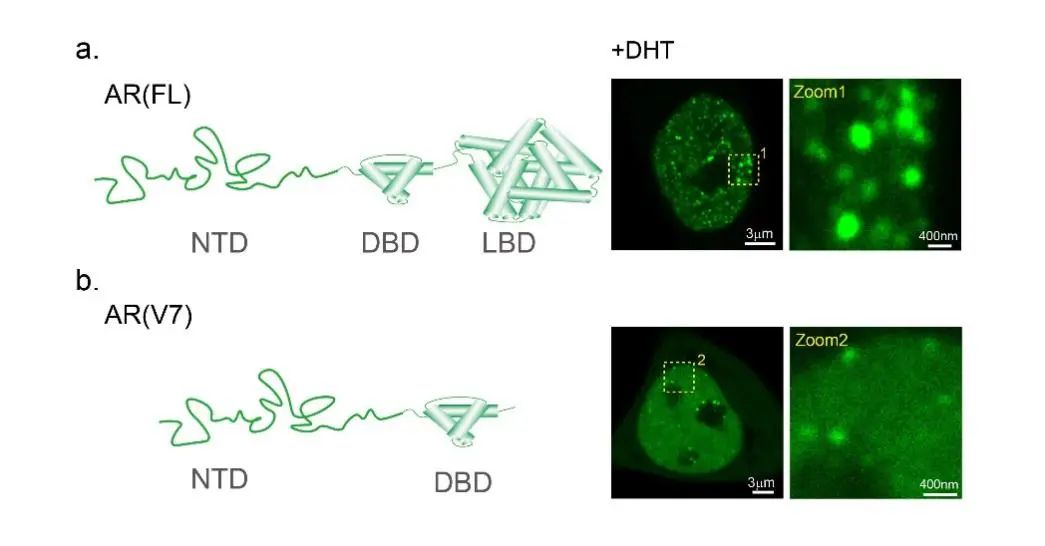
图1:AR和AR-V7的液-液相分离
AR的液-液相分离与AR拮抗剂的药效及耐药具有密切的关联性。例如,AR拮抗剂恩杂鲁胺 (Enzalutamide, Enza) 可以显著抑制AR在雄激素DHT刺激下产生的凝聚体。然而,在临床中当AR对恩杂鲁胺产生耐药突变AR (F877L/T878A) 后,恩杂鲁胺对AR (F877L/T878A) 的相分离抑制明显减弱。更有意思的是,恩杂鲁胺甚至可以诱导AR (F877L/T878A) 发生液-液相分离并激活AR转录活性,意味着当AR产生耐药突变后,恩杂鲁胺从AR拮抗剂转变为AR激动剂(图2)。
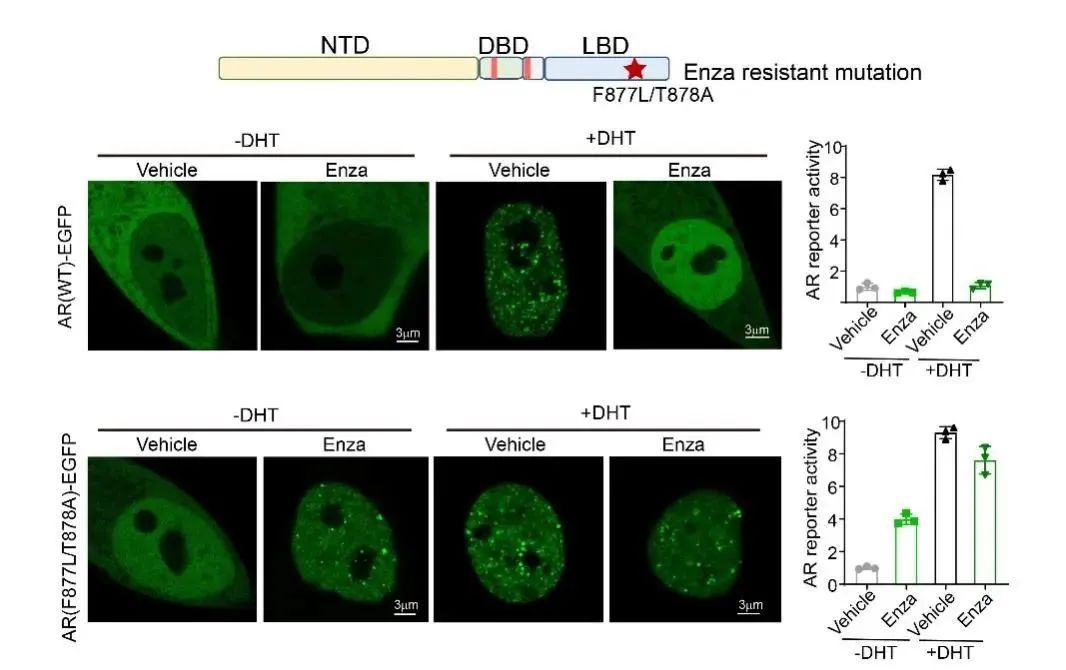
图2:恩杂鲁胺(Enza)对AR野生型和耐药突变型相分离和转录活性的影响
由于AR通过NTD介导的相分离来促进其转录活性,作者希望通过小分子靶向AR的液-液相分离来抑制AR的转录活性,并克服LBD的突变或缺失导致的AR拮抗剂药物的耐药问题(图3)。研究人员选择表达恩杂鲁胺耐药的AR (F877L/T878A) 细胞株作为AR液-液相分离的表型筛选体系,结合AR转录报告基因和细胞活性检测,进行了靶向AR相分离的化合物库筛选。作者发现了一个小分子化合物ET0516可以有效地抑制野生型AR和耐药突变AR的相分离形成。该化合物结合在AR的NTD结构域,可以特异性地降低AR转录活性并显著抑制前列腺癌细胞增殖及肿瘤的生长。
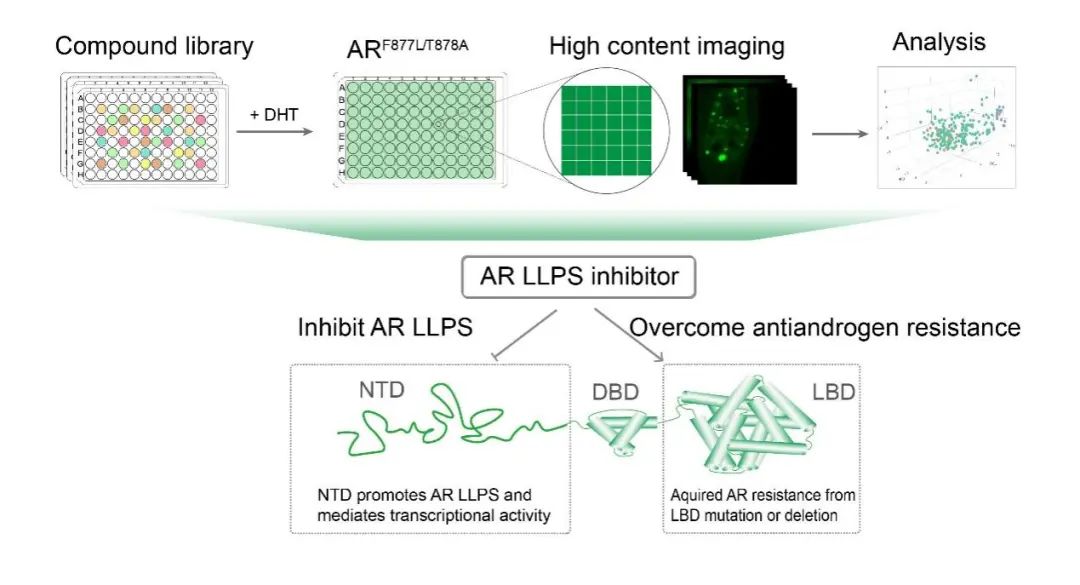
图3:AR液-液相分离小分子抑制剂的筛选
综上所述,作者揭示了液-液相分离对于AR转录机器形成和AR转录活性的重要作用。同时,液-液相分离在AR拮抗剂的耐药过程也起了关键的作用。在临床中发现的AR耐药突变在AR拮抗剂的存在下会发生化合物诱导的液-液相分离,使AR拮抗剂转变为AR激动剂。作者进一步通过化合物筛选,发现了AR 液-液相分离的小分子抑制剂可以有效抑制表达耐药突变AR或AR-V7的前列腺癌细胞生长。该工作为靶向蛋白液-液相分离来开发“难以成药”靶点的小分子药物奠定了坚实的基础。
朱光亚博士和上海奕拓医药朱继东博士为本文共同通讯作者,上海奕拓医药的谢菁菁博士和何浩博士为该论文共同第一作者。
制版人:十一




转载须知
【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。




 个人中心
个人中心
 我是园区
我是园区





