您还不是认证园区!
赶快前去认证园区吧!

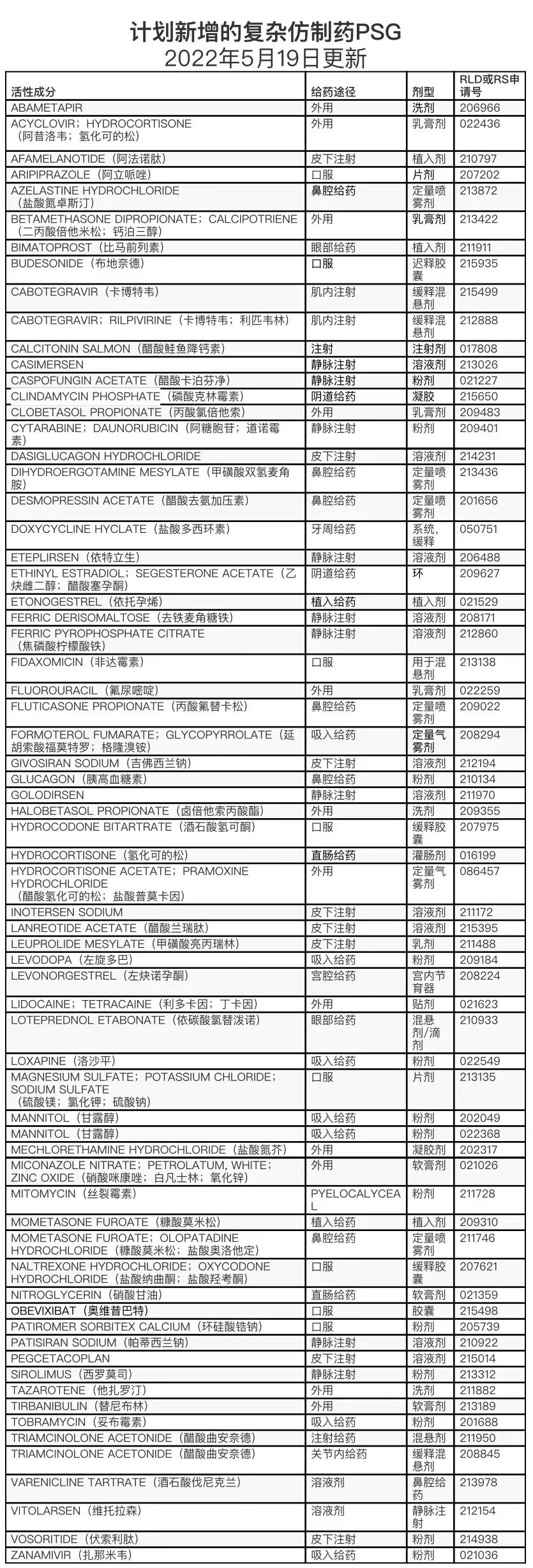
该页面展示了FDA计划发布的新增或修订的复杂仿制药特定产品指南(product-specific guidance,PSG),体现FDA目前对特定参考上市药物的仿制药产品开发的想法和期望,帮助仿制药企业确定最合适的方法,提供最有效的证据,以推动特定仿制药的审批。
-
复杂的活性成分(例如:肽、聚合物、活性药物成分的复杂混合物、天然来源成分) -
复杂制剂(例如:脂质体、胶体) -
复杂的给药途径(例如:配制成混悬液、乳剂或凝胶剂的局部作用药物,如皮肤病用药、复杂的眼科产品以及耳用剂型) -
复杂剂型(例如:透皮、定量吸入制剂、缓释注射剂) -
复杂的药械组合产品(例如:自动注射器、定量吸入器)等 -
其他可受益于早期科学参与、存在批准途径或替代方法的复杂性或不确定性的产品。
-
主要修订(Major revision):包括建议额外的生物等效性研究或证据要求,以支持FDA批准。 -
次要修订(Minor revision):除主要修订之外的其它修订,包括但不限于移除某些研究,为当前推荐的研究提供替代(简化)方法,添加有关新批准的RLD研究规格的信息,或提出其它建议,这些建议通常不会导致ANDA申请人开展额外的生物等效性研究或证据要求。 -
编辑性修订(Editorial revision):包括非实质性变更,例如更新外部参考,更正语法问题以及简化现有的格式。 次要修订是当前清单中最普遍的修订,计划修订清单的104份复杂仿制药PSG中有98份将会进行次要修订,另有80份将会进行编辑性修订,仅计划对3份PSG进行主要修订。
参考资料
https://www.fda.gov/drugs/guidances-drugs/product-specific-guidances-generic-drug-development
https://www.accessdata.fda.gov/scripts/cder/psg/index.cfm
作者:识林-晓林
长按下方二维码下载识林®App

识林®版权所有,未经许可不得转载



 个人中心
个人中心
 我是园区
我是园区




