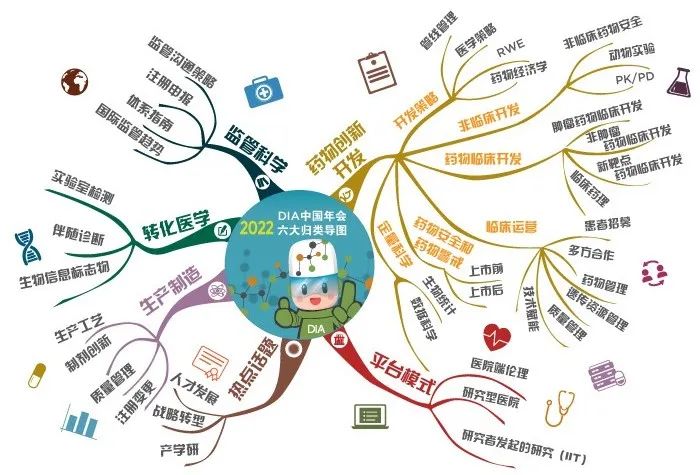
创新守护健康 合作引领未来——2022 DIA中国年会即将开幕 | 会讯
收藏
关键词:
合作
资讯来源:研发客 + 订阅账号
发布时间:
2022-07-08
ICH全体大会: ICH与各国药监、工业界等利益相关者合作的策略、意义,以及未来5-10年ICH的方向
Theresa MULLIN 博士
ICH管理委员会主席
美国FDA药品审评和研究中心(CDER)副主任,战略事务负责人
ICH M4Q(R2)专题:EWG对ICH M4Q 更新的期望
余煊强 博士
美国FDA CDER新产品办公室主任
全球新冠疫情下各国监管应对创新举措及教训 - FDA分享
Kevin BUGIN 博士
美国FDA新药办公室运营副主任
FDA仿制药办公室(OGD)全球事务计划和全球参与
Sarah IBRAHIM 博士
美国FDA CDER 仿制药办公室(OGD) 仿制药全球事务副主任
束映华 药学博士
美国FDA肿瘤卓越中心(OCE) 资深监管健康项目经理,ORBIS项目组成员
Jeffery SUMMER 博士
美国FDA CDER肿瘤疾病办公室转化科学副主任
Emer COOKE
欧盟药品监管局(EMA)局长
全球新冠疫情下各国监管应对创新举措及教训 - EMA分享
Alexis NOLTE
EMA人类医学办公室负责人
Junko SATO 博士
日本PMDA国际项目办公室主任
全球新冠疫情下各国监管应对创新举措及教训 - PMDA分享
Nobumasa NAKASHIMA 博士
日本PMDA国际项目执行副主任
日本的MAH监管经验 及
日本在COVID-19大流行期间的监管应对措施
Yuji MATSUKURA
日本MHLW国际药政事务办公室副主任
日本在COVID-19大流行期间的临床开发监管敏捷性措施
Daisuke KOGA
日本PMDA国际项目办公室计划管理部亚洲二部处长
更有诸多来自国内学术界的重磅演讲嘉宾就药物研发中的热点内容进行分享与讨论
部分已确认学术界演讲嘉宾
(以姓氏首字母排序)
组委会已正式推出酒店预定小程序,请微信扫描二维码进行预定
会议咨询:DIA 中国
Tel.: +86. 21. 8012 3167
Tel.: +86. 21. 8012 3190
Tel.: +86. 21. 8012 3166
Email: China@DIAglobal.org
大会日程:宁尔宁
Tel.: +86. 10. 5704 2655
Email: erning.ning@DIAglobal.org
大客户合作和团体报名(10人以上):
谢飞
Tel.: +86. 10. 5704 2652
Email: fei.xie@DIAglobal.org
展览、会议支持及广告预订:
中国食品药品国际交流中心
张莞宸
Tel.: +86 10 8221 2866*6007
Email: zhangwanchen@ccfdie.org
杨纪虎
Tel.: +86 10 8221 2866*6005
Email: yjh@ccfdie.org

DIA是一个全球化、跨学科的国际性学术组织,在中立的环境中,融合医药研发领域全行业的意见领袖,探讨当前研发的技术问题,提升专业能力,以及催化行业共识,在全球医药研发领域享有极高的声誉。
















 个人中心
个人中心
 我是园区
我是园区