他叫高洪岩,目前在麻省大学阿莫赫斯特分校读博,专业为电子计算机工程。他自认为从本科到现在“学习成绩平平”,期间经历了多次转专业:本科学习高分子化学,硕士研究无机纳米材料,博士则转到电子计算机。
不过高洪岩也表示:“让自己比较欣慰的是,我都能及时调整思路适应新课题,而且现在来看,多学科背景也给自己带来了科研上的启发。”
最近,其担任一作的新论文发表在 Science Advances 上。审稿人认为,
该工作填补了心肌细胞机电传感器领域的不足,是通过结合机械和电信号、去探索心肌细胞特性的一个令人兴奋的应用。
当下,尽管用于电生理测试的微电极器件、以及用于细胞机械力测试的叉指电极,已经全部实现商业化。但是,在同步测试心肌细胞机电信号时,这两种器件依然无法满足同步性、器件小型化和高通量性。
而此次成果为其提供了一个可行性方法,其能同时克服以上局限,并且具备一定的商用价值。
 制备小于细胞尺寸的 8x8 阵列生物芯片
一直以来,心血管疾病是造成人类死亡的主要疾病之一。多年来,人们主要借用体外细胞和组织模型,来研究该类疾病的病理特征。
以人类胚胎干细胞诱导分化的心脏组织,是心脏疾病研究、药物测试和再生医学有效的模型,其分化出来的心肌细胞的机电耦合信号,是反映相关心脏组织状态的重要指标。
凭依“兴奋-收缩耦合”的机制,心肌细胞的机电信号会错综复杂地联系在一起。所以,对于明确心肌细胞的生理机制和病理机制来说,同时测量两种信号可谓至关重要。
例如,细胞中“兴奋-收缩耦合”的减弱,或可导致心律失常。这时,通过跟踪细胞的电活动和机械活动,就能揭示上述机制的具体内容。
然而,现有监测方法主要依赖于:将两种信号测试方法结合起来。这会导致器件集成、或信号采集的无法同步,进一步限制了监测时间、空间分辨率和可扩展性。
比如,在传统的光学方法里,一般依靠荧光标记来指示生物电信号,以及借助显微镜形态的追踪,来检测生物力学行为。
但是,当使用传统方法时,时间分辨率和可访问性都会被降低,这让快速动力学在三维组织中的可扩展监测,会受到一定限制。而且,分子标记物也可能会损害细胞收缩性、或是诱导细胞的毒性。
另外,当同时监测机电信号时,商业微电极和叉指电极的结合,并不能突破器件的尺寸限制,这让器件面临着低通量的“掣肘”,进而致使空间分辨率过低。
制备小于细胞尺寸的 8x8 阵列生物芯片
一直以来,心血管疾病是造成人类死亡的主要疾病之一。多年来,人们主要借用体外细胞和组织模型,来研究该类疾病的病理特征。
以人类胚胎干细胞诱导分化的心脏组织,是心脏疾病研究、药物测试和再生医学有效的模型,其分化出来的心肌细胞的机电耦合信号,是反映相关心脏组织状态的重要指标。
凭依“兴奋-收缩耦合”的机制,心肌细胞的机电信号会错综复杂地联系在一起。所以,对于明确心肌细胞的生理机制和病理机制来说,同时测量两种信号可谓至关重要。
例如,细胞中“兴奋-收缩耦合”的减弱,或可导致心律失常。这时,通过跟踪细胞的电活动和机械活动,就能揭示上述机制的具体内容。
然而,现有监测方法主要依赖于:将两种信号测试方法结合起来。这会导致器件集成、或信号采集的无法同步,进一步限制了监测时间、空间分辨率和可扩展性。
比如,在传统的光学方法里,一般依靠荧光标记来指示生物电信号,以及借助显微镜形态的追踪,来检测生物力学行为。
但是,当使用传统方法时,时间分辨率和可访问性都会被降低,这让快速动力学在三维组织中的可扩展监测,会受到一定限制。而且,分子标记物也可能会损害细胞收缩性、或是诱导细胞的毒性。
另外,当同时监测机电信号时,商业微电极和叉指电极的结合,并不能突破器件的尺寸限制,这让器件面临着低通量的“掣肘”,进而致使空间分辨率过低。
 如何同步测量单细胞生物的“电-机械”活动?
基于此,开发一种能同步测量单细胞生物“电-机械”活动的器件,对于研究心肌细胞“兴奋-收缩耦合”过程、以及心肌组织在病理学中的应用来说,可谓十分重要。
作为一种生物体,三维生物丝具有多种功能。受此启发,高洪岩所在课题组提出并设计了一种三维纳米线晶体管器件(下称“纳米晶体管”)。
当把它用于同步监测单个心肌细胞的生物“电-机械”耦合信号时,以及解析细胞运动向量的应用时,该团队对其性能进行了验证。
结果发现,针对传统方法中的空分辨率低、不同步性、不具备扩展性等短板,纳米晶体管均能予以补齐。
在制备上,让单根硅纳米线通过定位机械组装,即可造出纳米晶体管。借助一系列微纳加工技术,该团队还制备出了小于细胞尺寸的 8x8 阵列生物芯片。
(1)悬浮纳米线的几何自由度,能将细胞机械运动、转化为纳米线中的机械变形或者应变。同时,可以通过硅纳米线的压阻效应,来监测这种变化。
如何同步测量单细胞生物的“电-机械”活动?
基于此,开发一种能同步测量单细胞生物“电-机械”活动的器件,对于研究心肌细胞“兴奋-收缩耦合”过程、以及心肌组织在病理学中的应用来说,可谓十分重要。
作为一种生物体,三维生物丝具有多种功能。受此启发,高洪岩所在课题组提出并设计了一种三维纳米线晶体管器件(下称“纳米晶体管”)。
当把它用于同步监测单个心肌细胞的生物“电-机械”耦合信号时,以及解析细胞运动向量的应用时,该团队对其性能进行了验证。
结果发现,针对传统方法中的空分辨率低、不同步性、不具备扩展性等短板,纳米晶体管均能予以补齐。
在制备上,让单根硅纳米线通过定位机械组装,即可造出纳米晶体管。借助一系列微纳加工技术,该团队还制备出了小于细胞尺寸的 8x8 阵列生物芯片。
(1)悬浮纳米线的几何自由度,能将细胞机械运动、转化为纳米线中的机械变形或者应变。同时,可以通过硅纳米线的压阻效应,来监测这种变化。
(2)此外,纳米晶体管还可通过场效应,来检测细胞的动作电位。
由于生物力学和生物电过程可被分为不同频域。所以,上述两个过程都可通过纳米线的电信号进行检测,并能在单个器件中予以区分。
而三维凸起结构的设计,则让细胞和器件之间的生物界面更加紧密,从而实现更稳定的信号采集。
值得一提的是,通过使用 30-50nm 的硅纳米线,课题组让晶体管的投影区域小于 0.4μm²,相比传统的微电极、以及压力传感器,这一面积小了几个数量级。
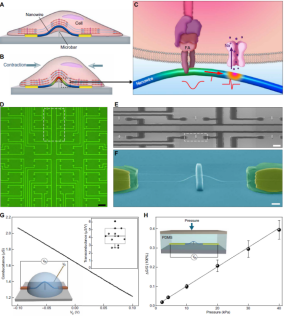
实验结果表明,硅纳米线对场电势监测的灵敏性,并未受到三维晶体管结构的影响。并且,当面临压缩和拉伸应变时,该器件均表现出良好的线性关系。这种性质,也让同时采集机械信号和电信号成为可能。
图 | 三维纳米线晶体管的结构和表征(来源:Gao H et al., Sci Adv, 2022)
而通过将人类胚胎干细胞分化的心肌细胞,培养在三维晶体管生物芯片上,高洪岩成功采集到多通道细胞机电耦合信号。
其还发现,该器件表现出良好的生物相容性,而心肌细胞也能在生物芯片上成活,并能维持规律的机械活动。
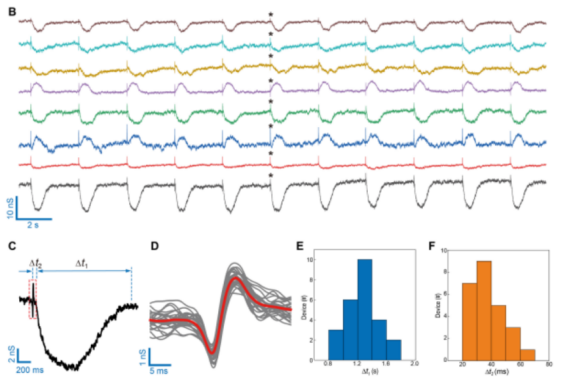
如下图,其展示了八个代表性的机电监测信号、信号的周期性、以及信号频率,与典型的人胚胎干细胞衍生的心肌细胞收缩频率一致。
但是,这与传统晶体管监测到的单一信号并不相同。在每个信号周期中,宽频峰之前的均有周期很短,同时尖峰的振幅较低。
不过,这一信号确实符合人胚胎干细胞、以及衍生心肌细胞的外动作电位的信号特征,而宽峰的来源也得到了数据验证。
图 | 八通道动作电位和机械信号监测(来源:Gao H et al., Sci Adv, 2022)
这些证据均表明,宽峰来源于心肌细胞的机械收缩舒张,同时也展示了该器件可同步测试单细胞机械和电信号的能力。
因此,动作电位和机械信号之间的时间延迟,能通过让对应动作电位、触发钙离子的形式,在肌浆网中释放。
与此同时,这一集成器件还实现了高通量特性,可同时获得多通道的“机械-电”耦合信号,从而监测单层心肌细胞信号的传输方向和传输速度。
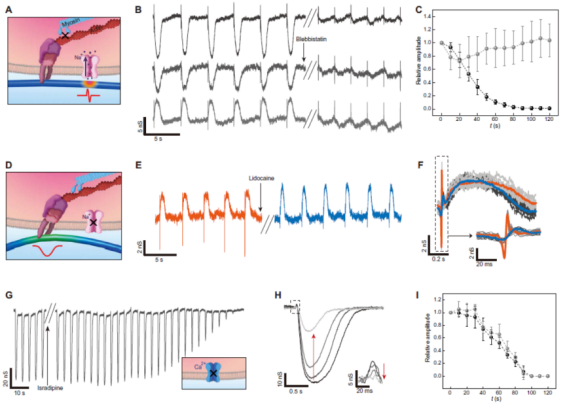
可以说,利用此次器件独有的多功能特性,高洪岩等人揭示了其在细胞药理和病理研究中的潜力。
图 | 传感器在药物检测方面应用(来源: Gao H et al., Sci Adv, 2022)
与传统监测心肌细胞跳动的器件不同的是,课题组还通过分析机械信号,以及结合模拟细胞-器件界面的机械耦合,赋予了器件解析细胞运动向量的能力。
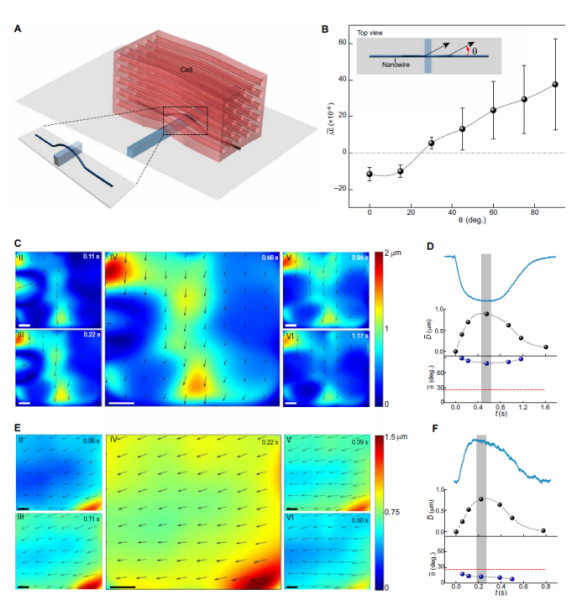
期间,该团队发现硅纳米线的电导变化,呈现出一定比例的分布。具体来说,通过建立硅纳米线和细胞界面的模型,以及对细胞相对纳米线轴向的运动进行模拟,结果发现当细胞运动方向与纳米线角度 θ 从 0
o
增大到 90o 时,纳米线的应变会从压缩转变为拉伸,平均转变角度大约为 25o。
针对细胞收缩周期中连续捕获的图像,研究人员对其进行向量分析,结果发现信号的振幅与细胞位移始终匹配。
而且,与细胞相对于纳米线轴向的运动方向来说,机械信号的符号也呈现出完全一致性,这说明该器件具备解析细胞运动向量的独特能力。
另外,通过模拟纳米线电导的变化,该团队计算出了如下数字:即单个细胞的收缩舒张力低于 160nN,这为研究细胞机械性质提供了借鉴信息。
综上,
本次器件能把两种功能集成在一个设备上,借此可以实现“等效缩放”,从而让生物电子器件对组织的侵害,可被最大限度地减少。
研究还表明,细胞电信号和机械响应均能揭示心脏组织中的基因表达。利用这一单细胞检测技术,能实现更广泛的表型-基因型的相关性,从而为研究心脏类疾病的病理和药理,提供更多的理论信息。
图 | 机械信号与细胞运动的相关性(来源:Gao H et al., Sci Adv, 2022)
图 | 相关论文(来源:Science Advances)
 迫于疫情,自行搭建细胞培养平台
据悉,该成果是一个多学科交叉的项目,其中涉及到纳米半导体器件的制备与加工、生物干细胞工程、生物电子界面模拟和影像分析等。
高洪岩表示:“在借助生物芯片培养心肌细胞的过程中,因为没有生物背景和相关经验,为此耽误了半年之久。当时正值疫情的严重期间,可利用的资源比较少。因为研究比较紧迫,我和导师商议之后决定自己搭建细胞培养平台。最终花费半年时间,终于得到了非常好的结果。”
但在目前,将微纳加工集成在刚性基底的制备方法,限制了该器件在器官、类器官组织中的应用。
因此,
如何将该器件集成到柔性器件里,从而实现更广泛的器官集成,是该团队的下一个研究目标。
迫于疫情,自行搭建细胞培养平台
据悉,该成果是一个多学科交叉的项目,其中涉及到纳米半导体器件的制备与加工、生物干细胞工程、生物电子界面模拟和影像分析等。
高洪岩表示:“在借助生物芯片培养心肌细胞的过程中,因为没有生物背景和相关经验,为此耽误了半年之久。当时正值疫情的严重期间,可利用的资源比较少。因为研究比较紧迫,我和导师商议之后决定自己搭建细胞培养平台。最终花费半年时间,终于得到了非常好的结果。”
但在目前,将微纳加工集成在刚性基底的制备方法,限制了该器件在器官、类器官组织中的应用。
因此,
如何将该器件集成到柔性器件里,从而实现更广泛的器官集成,是该团队的下一个研究目标。
参考资料:
1.Gao, H., Yang, F., Sattari, K., Du, X., Fu, T., Fu, S., ... & Yao, J. (2022). Bioinspired two-in-one nanotransistor sensor for the simultaneous measurements of electrical and mechanical cellular responses. Science Advances, 8(34), eabn2485.


 制备小于细胞尺寸的 8x8 阵列生物芯片
制备小于细胞尺寸的 8x8 阵列生物芯片
 如何同步测量单细胞生物的“电-机械”活动?
如何同步测量单细胞生物的“电-机械”活动?

 迫于疫情,自行搭建细胞培养平台
迫于疫情,自行搭建细胞培养平台





 个人中心
个人中心
 我是园区
我是园区




