CSCO 2020│郭军教授、何志嵩教授解读POLARIS-03研究——晚期尿路上皮癌二线治疗的新突破
收藏
关键词:
治疗新突破癌
资讯来源:医脉通肿瘤科 + 订阅账号
所属行业:化学原料药 + 订阅行业
发布时间:
2020-09-25
2020年9月19日~26日,由中国临床肿瘤学会(CSCO)、北京市希思科临床肿瘤学研究基金会和国家癌症中心主办的第23届全国临床肿瘤学大会暨2020年CSCO学术年会盛大召开。本届年会共收稿1211篇,口头报告91篇,壁报交流307篇,普通摘要813篇。经过层层筛选,特瑞普利单抗注射液(重组人源化抗PD-1单克隆抗体注射液,JS001)在标准治疗失败后的局部进展或转移性膀胱尿路上皮癌患者中的有效性和安全性的开放、多中心、单臂、II期临床研究(POLARIS-03)荣获本届CSCO年会优秀论文二等奖。在CSCO年会优秀论文交流专题上,北京大学肿瘤医院郭军教授对该研究进行了专题介绍,北京大学第一医院何志嵩教授对此也做了精彩点评,小编特汇总如下,以飨读者。

中国标准治疗失败后的晚期尿路上皮癌患者的治疗选择有限
尿路上皮癌是主要的泌尿系统肿瘤之一,主要发布部位为膀胱,国内肾盂、输尿管来源并不少见,一旦转移,预后差。根据Globocan2018年全球数据,膀胱癌新发患者占癌症新发病例第10位,占癌症死亡病例第13位。我国膀胱癌每年新发病例8.2万,占全球15.0%,死亡病例3.82万,占全球19.1%。
既往晚期尿路上皮癌的一线治疗主要以化疗为主,但对于经标准化疗方案失败的患者,其二线治疗方案选择有限。近年来,免疫治疗、靶向治疗、抗体偶联药物纷纷在晚期尿路上皮癌的治疗上取得突破, 国外已经有5款PD-1/PD-L1陆续获得FDA批准用于晚期尿路上皮癌的二线治疗。国内基于II期BGB-A317-204临床研究,替雷利珠单抗已于2020年4月获批用于治疗接受含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性PD-L1高表达的尿路上皮癌患者。但国内标准治疗失败后的晚期尿路上皮癌患者的治疗选择仍然有限。
特瑞普利单抗(Triprilimab,JS001)是一种以PD-1为靶点的新型人源化单克隆抗体,已于2018年12月获批用于治疗既往标准治疗失败后的局部进展或转移性黑色素瘤。特瑞普利单抗用于晚期泌尿肿瘤的I期临床研究显示,在尿路上皮癌患者中,研究者评估的客观缓解率(ORR)为25%,疾病控制率(DCR)为67.5%,与药物相关的不良事件大多为1/2级,耐受性良好。
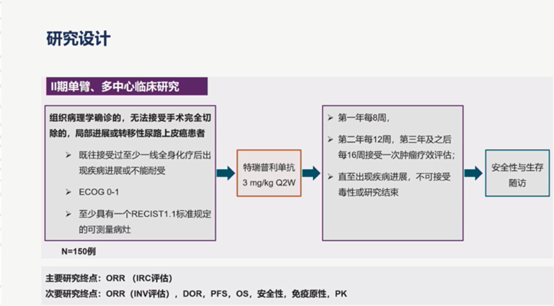
POLARIS-03是一项II期、单臂、多中心研究,旨在评估特瑞普利单抗用于标准治疗失败后的局部进展或转移性膀胱尿路上皮癌患者的有效性和安全性,研究设计如图1。主要终点为由独立审评委员会(Independent Review Committee, IRC)评估的ORR,次要终点为由研究者(INV)评估的ORR、缓解持续时间(DoR)、无进展生存期(PFS)、总生存期(OS)和安全性等。
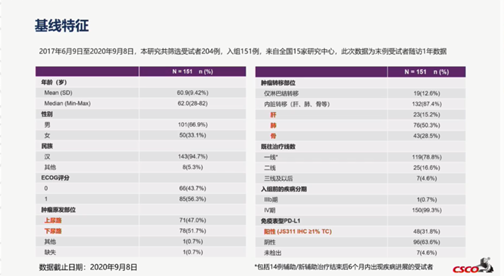
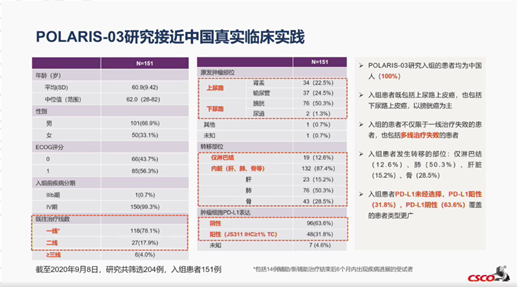
2017年6月9日-2020年9月8日,研究共入组了全国15家研究中心151例患者,其中肝转移患者占15.2%,肺转移患者占50.3%,肝、肺转移患者相对而言治疗难度较大。此外,POLARIS-03研究是首个在中国标准治疗失败的晚期尿路上皮癌非选择人群中开展的关键临床研究,其PD-L1阳性患者仅占31.8%。
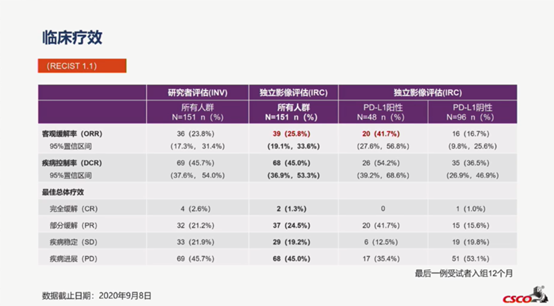
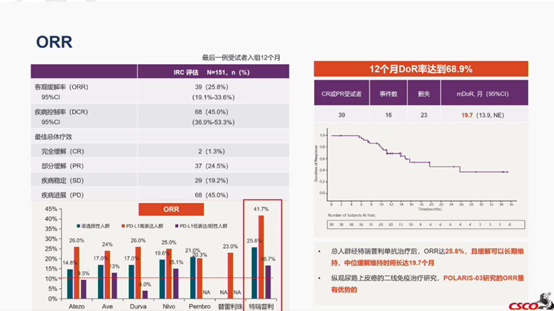
研究结果显示,IRC评估的ORR为25.8%。亚组分析显示,PD-L1阳性患者的ORR高达41.7%,PD-L1阳性人群及仅淋巴结转移人群获益更显著。中位起效时间1.8个月,中位DOR为19.7个月,12个月的DoR率达到68.9%。
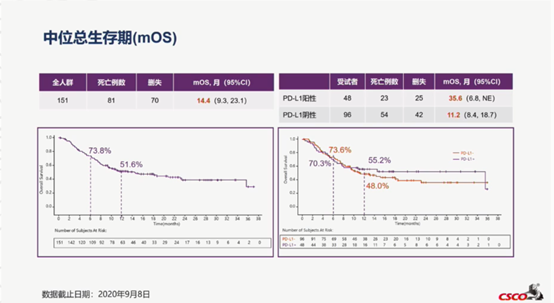
整体人群中位PFS(mPFS)为2.3个月,PD-L1阳性患者mPFS为3.7个月。整体人群中位OS(mOS)为14.4个月,PD-L1阳性患者mOS为35.6个月。
安全性方面,治疗期间出现的不良事件与目前获批该适应症的同类药物报道的安全性一致,未观察到新的安全性信号。
该研究表明,特瑞普利单抗在系统治疗失败的晚期尿路上皮癌患者总体人群及各亚组中均显示了明确的抗肿瘤活性及持续的有效性。特瑞普利单抗单药治疗将为中国标准治疗失败的晚期尿路上皮癌患者提供一种新的治疗选择。

近年来,免疫治疗、靶向药物、抗体偶联药物纷纷在晚期尿路上皮癌的系统治疗中取得突破性进展,特别是以PD-1/PD-L1单抗为代表的免疫治疗已经成为该领域的研究热点。POLARIS-03研究是首个在中国标准治疗失败的晚期尿路上皮癌非选择人群中开展免疫治疗探索的临床研究。
在研究设计方面,该研究接近中国真实临床实践,其入组患者既包括上尿路上皮癌,也包括下尿路上皮癌;入组的患者不仅限于一线治疗失败的患者,也包括多线治疗失败的患者;入组患者PD-L1未经选择,覆盖了更广泛的患者类型。
在研究结果方面,总人群经特瑞普利单抗单药治疗后,ORR达25.8%,且缓解可以长期维持,中位缓解维持时间长达19.7个月。与既往尿路上皮癌二线免疫治疗的相关研究相比,POLARIS-03研究的总人群ORR具有优势, 在OS方面仅次于Durva,且特瑞普利单抗单药治疗PD-L1高表达患者的ORR最高,达41.7%。
总体而言,POLARIS-03研究证实了特瑞普利单抗用于转移性尿路上皮癌患者二线全人群的疗效和安全性,给患者提供了更多的治疗选择。此外,POLARIS-03研究的总人群ORR与获批的阿替利珠单抗和帕博利珠单抗一线方案ORR相当,因此,特瑞普利单抗在不适合顺铂的局部晚期或转移性膀胱癌患者一线治疗中也具有前景,值得展望。







 个人中心
个人中心
 我是园区
我是园区




