深圳先进院孵化,生物计算初创专注GPCR新药研发,预计明年递交首个FIC管线IND丨专访阿尔法分子
收藏
关键词:
生物专访药研发药研发新药
资讯来源:DeepTech深科技 + 订阅账号
发布时间:
2022-05-17
以 AlphaFold2、RoseTTAFold 等为代表的蛋白质结构预测工具为结构生物学研究和新药研发提供了新思路。然而,这些工具主要以大分子结构为主,对膜蛋白的结构预测只占整个数据的 4% 左右,且对于膜蛋白结构的预测精度也有待验证。
在此背景下,对膜蛋白结构预测和模拟也就十分迫切和重要。其中,G 蛋白偶联受体(GPCR)是膜蛋白家族庞大的成员,也是最重要的明星药物靶点,当前大约有 40% 的上市药物以 GPCR 为靶点。
近日,在 GPCR-DOCK 2021 大赛中,国内生物制药初创阿尔法分子及其学术团队表现亮眼,在 GPCR 相关靶点和结合模式预测中斩获全球第三名。据悉,在大赛中,
该团队的预测结果不仅正确复现了 GPCR 折叠模型,还获得了精准的药物分子结合模型,捕获到药物分子所有的关键性相互作用。
GPCR-DOCK 大赛
由国际著名结构生物学家 Raymond C.Stevens 等在国际上发起,截至目前,大赛已于 2008 年、2010 年、2012 年、2021 年分别举办。在本次 GPCR-DOCK 2021 大赛中,来自全球不同国家的 45 个团队针对 5 个参赛靶点合计提交了超 800 个模型。
在此之际,生辉独家专访了中国科学院深圳先进技术研究院(以下简称为 “先进院”)研究员、阿尔法分子创始人袁曙光博士,和他聊了聊阿尔法分子的发展概况以及他对整个生物计算领域的见解。
“本次大赛,从更客观的角度评价了阿尔法分子的底层科学,也是对阿尔法分子 GPCR 药物开发技术的第三方验证。” 袁曙光说。
袁曙光曾在瑞士科学院院瑞士科学院院、洛桑联邦理工学院教授 Horst Vogel 实验室从事博士后研究,他现在是中国科学院深圳先进技术研究院计算机辅助药物设计研究中心的研究员。2020 年,他与 Horst Vogel 联合创办阿尔法分子,
该公司由深圳先进院孵化而来,专注于利用 AI、生物芯片等新技术开发与 GPCR 信号通路相关的新药。
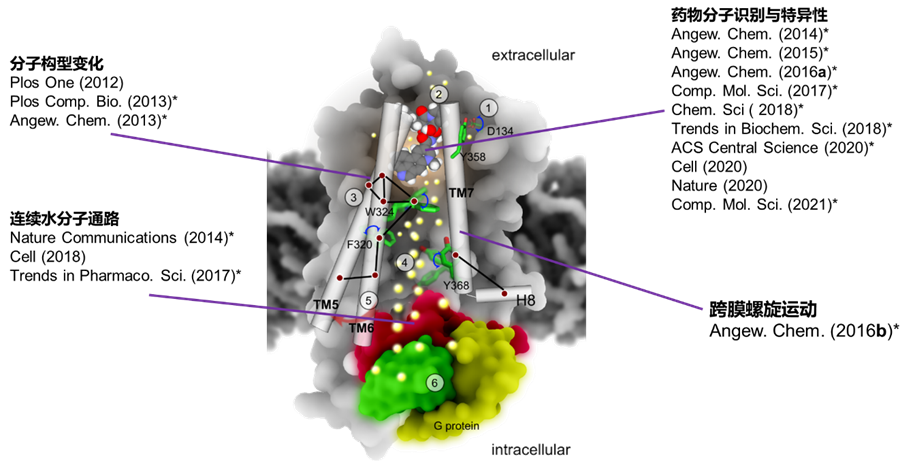
▲图 | 袁曙光团队近年在 GPCR 领域的深入研究工作(来源:受访者提供)
2021 年,阿尔法分子获得一品红药业天使轮融资。目前,该公司正在进行 A 轮融资,用以 IND 准备工作以及扩建场地等。
 深圳先进院孵化,瞄准 GPCR 新药研发
长久以来,袁曙光一直从事针对 GPCR 靶点的基础研究和转化工作,包括深入探究 GPCR 分子机制、药理学机制,GPCR 等膜蛋白的药物筛选。读博期间,袁曙光作为第一作者兼通讯作者提出 GPCR 连续水分子通路激活理论,据悉,该理论后续也成为了 GPCR 分子机制研究的核心理论之一。
他还在瑞士第四大制药公司 Actelion(现已被强生收购)以及Idorisa 从事 GPCR 药物开发工作,尤其是针对 GPCR 靶点的药物筛选和设计。曾通过生物计算方式开发的两款 GPCR 新药已相继进入临床研究阶段。
(来源:Nature Communications)
“我们团队在针对 GPCR 的理论、分子机制研究、生物技术创新以及新药研发上具有深厚的积淀。在学术上取得成就的同时,我们也希望能够向产业转化迈进一步,发挥研究成果更大的价值。
2019 年,与先进院沟通之后,我们团队决定回到国内将多年的基础研究和技术创新落地转化。”袁曙光说。
深圳先进院
在产业转化上经验丰富,目前在低成本健康、高端医学影像、机器人、电动汽车等领域极开展科技成果转移转化工作,转移转化的专利数已超三百件。截止 2021 年底,深圳先进院授权 4903 件专利、建立企业联合实验室 180 家、累计孵化企业 1346 家,其中包括
联影医疗
、DNA 数据存储公司
中科碳元
等。
深圳先进院孵化,瞄准 GPCR 新药研发
长久以来,袁曙光一直从事针对 GPCR 靶点的基础研究和转化工作,包括深入探究 GPCR 分子机制、药理学机制,GPCR 等膜蛋白的药物筛选。读博期间,袁曙光作为第一作者兼通讯作者提出 GPCR 连续水分子通路激活理论,据悉,该理论后续也成为了 GPCR 分子机制研究的核心理论之一。
他还在瑞士第四大制药公司 Actelion(现已被强生收购)以及Idorisa 从事 GPCR 药物开发工作,尤其是针对 GPCR 靶点的药物筛选和设计。曾通过生物计算方式开发的两款 GPCR 新药已相继进入临床研究阶段。
(来源:Nature Communications)
“我们团队在针对 GPCR 的理论、分子机制研究、生物技术创新以及新药研发上具有深厚的积淀。在学术上取得成就的同时,我们也希望能够向产业转化迈进一步,发挥研究成果更大的价值。
2019 年,与先进院沟通之后,我们团队决定回到国内将多年的基础研究和技术创新落地转化。”袁曙光说。
深圳先进院
在产业转化上经验丰富,目前在低成本健康、高端医学影像、机器人、电动汽车等领域极开展科技成果转移转化工作,转移转化的专利数已超三百件。截止 2021 年底,深圳先进院授权 4903 件专利、建立企业联合实验室 180 家、累计孵化企业 1346 家,其中包括
联影医疗
、DNA 数据存储公司
中科碳元
等。
加入深圳先进院后,袁曙光团队与先进院成立联合实验室,共同推进研究和转化工作。2020 年,由先进院孵化,阿尔法分子正式落地深圳,并于同年完成种子轮融资。成立后的公司,定位是一家以管线开发为主的生物制药公司,专注于开发针对 GPCR 膜蛋白靶点以及相关信号通路的 FIC 管线。
 已开发 4 条 FIC 自研管线,预计明年首条管线递交 IND
据袁曙光透露,作为一家生物制药初创公司,阿尔法分子当前的重点是将在研管线推进临床,后续再与 Bigpharma 合作推进药物的临床开发和未来的商业化。
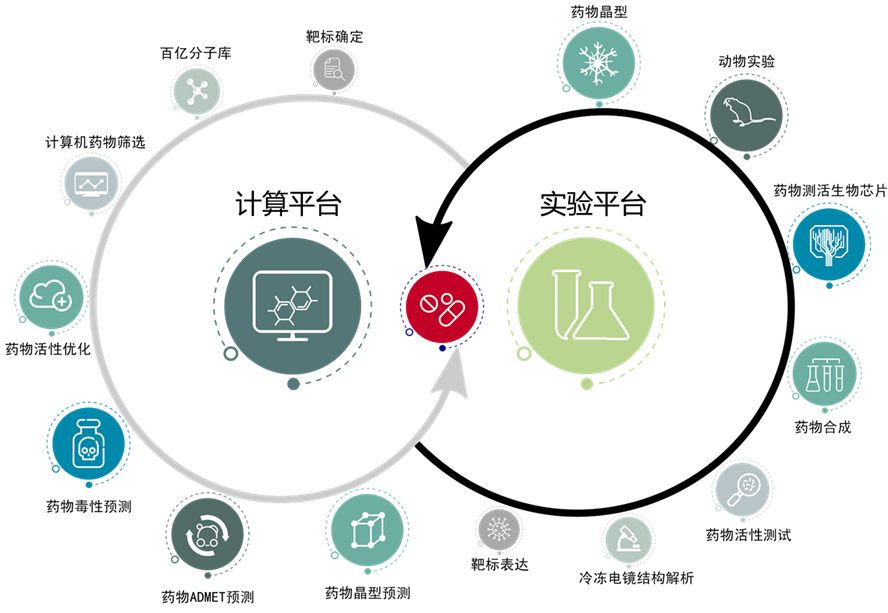
该公司开发管线的基础主要建立在公司现有的两大技术平台上,一是智能新药研发平台即计算平台,二是生物芯片技术平台即干实验平台。
袁曙光解释道,阿尔法分子的智能新药研发平台涵盖临床前新药研发的各个环节,通过计算方法精确预测 GPCR 等膜蛋白靶点的三维结构,对百亿级药物分子进行高效筛选,设计药物分子,以及分析药物分子与 GPCR 靶点结构的相互作用模式。
完成药物分子设计后,则需要通过实验验证,包括利用生物芯片技术预测 GPCR 活性、成药性以及毒性等等;其中,还会应用冷冻电镜技术,通过实验的方法解析膜蛋白的三维结构。
“去年年初,我们针对 GPCR 等膜蛋白、离子通道取得了一项重要的成果 —— 原生态细胞膜技术,可以在
真实
的细胞膜环境中解析膜蛋白的三维结构。
多种技术结合起来,能够帮助我们高效进行药物筛选和优化药物活性。
” 袁曙光介绍道。
据悉,GPCR 新药研发具有一定的技术壁垒,成功开发出新药并非易事。能否制备具备真实生理功能的样本、GPCR 自身表达和测活体系建立,以及如何区分 GPCR 激活哪些下游通道等都是有待解决的难题,这需要长期的底层技术和产业化经验的积累。
袁曙光告诉生辉,基于这些专有的技术平台,阿尔法分子开发了 4 条极具差异化的 FIC 管线,适应症集中在代谢和精神类疾病领域,包括糖尿病、帕金森病、阿尔茨海默病、抑郁症等神经退行性疾病。根据管线开发进度,
预计在 2023 年可以拿到在研管线的首个 IND 批件。
“未来 3-5 年内,预计会有 2-3 条 FIC 管线会进入临床研究阶段,第 5 个年头可能会开始为产品上市做准备。” 袁曙光总结道。
已开发 4 条 FIC 自研管线,预计明年首条管线递交 IND
据袁曙光透露,作为一家生物制药初创公司,阿尔法分子当前的重点是将在研管线推进临床,后续再与 Bigpharma 合作推进药物的临床开发和未来的商业化。
该公司开发管线的基础主要建立在公司现有的两大技术平台上,一是智能新药研发平台即计算平台,二是生物芯片技术平台即干实验平台。
袁曙光解释道,阿尔法分子的智能新药研发平台涵盖临床前新药研发的各个环节,通过计算方法精确预测 GPCR 等膜蛋白靶点的三维结构,对百亿级药物分子进行高效筛选,设计药物分子,以及分析药物分子与 GPCR 靶点结构的相互作用模式。
完成药物分子设计后,则需要通过实验验证,包括利用生物芯片技术预测 GPCR 活性、成药性以及毒性等等;其中,还会应用冷冻电镜技术,通过实验的方法解析膜蛋白的三维结构。
“去年年初,我们针对 GPCR 等膜蛋白、离子通道取得了一项重要的成果 —— 原生态细胞膜技术,可以在
真实
的细胞膜环境中解析膜蛋白的三维结构。
多种技术结合起来,能够帮助我们高效进行药物筛选和优化药物活性。
” 袁曙光介绍道。
据悉,GPCR 新药研发具有一定的技术壁垒,成功开发出新药并非易事。能否制备具备真实生理功能的样本、GPCR 自身表达和测活体系建立,以及如何区分 GPCR 激活哪些下游通道等都是有待解决的难题,这需要长期的底层技术和产业化经验的积累。
袁曙光告诉生辉,基于这些专有的技术平台,阿尔法分子开发了 4 条极具差异化的 FIC 管线,适应症集中在代谢和精神类疾病领域,包括糖尿病、帕金森病、阿尔茨海默病、抑郁症等神经退行性疾病。根据管线开发进度,
预计在 2023 年可以拿到在研管线的首个 IND 批件。
“未来 3-5 年内,预计会有 2-3 条 FIC 管线会进入临床研究阶段,第 5 个年头可能会开始为产品上市做准备。” 袁曙光总结道。
 “新药研发单靠 AI 远远不够”
制药大厂频频与 AI 制药公司牵手的背后,一定程度上是对 AI 在制药领域价值的认可。
袁曙光强调,国内外 AI 制药领域发展势头良好,相关公司日益增多,合作以及里程碑事件也在不断刷新。但是,其实到现在为止,我们还没有看到真正跑出原创新药的 AI 制药公司。
“
其实要真正开发出原创新药,单靠 AI 技术还远远不够。新药研发是多种技术的结合,需要多种硬核的生物技术与传统制药的方式相结合,
比如说干实验技术、冷冻电镜技术、X-Ray 晶体衍射技术以及生物芯片技术等等。
我认为,开发原创新药的基础在于需要将生物计算和多种生物技术手段有机整合在一起,形成一个完整的药物研发流程闭环。
” 袁曙光说。
他继续补充道,客观来讲,在整个药物研发管线这流程和周期里面,AI 会在某些比较小的环节中发挥一定的作用。不过,AI 的贡献有多大也需要时间的验证和后续更多的数据佐证。
“新药研发单靠 AI 远远不够”
制药大厂频频与 AI 制药公司牵手的背后,一定程度上是对 AI 在制药领域价值的认可。
袁曙光强调,国内外 AI 制药领域发展势头良好,相关公司日益增多,合作以及里程碑事件也在不断刷新。但是,其实到现在为止,我们还没有看到真正跑出原创新药的 AI 制药公司。
“
其实要真正开发出原创新药,单靠 AI 技术还远远不够。新药研发是多种技术的结合,需要多种硬核的生物技术与传统制药的方式相结合,
比如说干实验技术、冷冻电镜技术、X-Ray 晶体衍射技术以及生物芯片技术等等。
我认为,开发原创新药的基础在于需要将生物计算和多种生物技术手段有机整合在一起,形成一个完整的药物研发流程闭环。
” 袁曙光说。
他继续补充道,客观来讲,在整个药物研发管线这流程和周期里面,AI 会在某些比较小的环节中发挥一定的作用。不过,AI 的贡献有多大也需要时间的验证和后续更多的数据佐证。



 深圳先进院孵化,瞄准 GPCR 新药研发
深圳先进院孵化,瞄准 GPCR 新药研发

 已开发 4 条 FIC 自研管线,预计明年首条管线递交 IND
已开发 4 条 FIC 自研管线,预计明年首条管线递交 IND
 “新药研发单靠 AI 远远不够”
“新药研发单靠 AI 远远不够”




 药选址
药选址



 深圳先进院孵化,瞄准 GPCR 新药研发
深圳先进院孵化,瞄准 GPCR 新药研发

 已开发 4 条 FIC 自研管线,预计明年首条管线递交 IND
已开发 4 条 FIC 自研管线,预计明年首条管线递交 IND

 “新药研发单靠 AI 远远不够”
“新药研发单靠 AI 远远不够”



