2021年7月9日/医麦客新闻 eMedClub PR News/--7月7日,一家临床阶段的生物技术公司Coya Therapeutics, Inc.宣布,美国食品和药品监督管理局(FDA)授予ALS001孤儿药指定,这是一种自体、扩增的Treg细胞疗法,主要用于治疗肌萎缩侧索硬化症(ALS)。
Coya Therapeutics首席执行官Howard Berman博士说:“ALS001孤儿药的指定说明了ALS患者存在大量的医疗需求,虽然目前这些患者没有有效的治疗方法,但是ALS001在早期的临床数据中表明,该药物能够对神经起到保护作用,起到减缓和阻止ALS的进展。ALS001正在进行的2a期的试验,预计将在2021年夏末提供相关的临床数据。期待与FDA的合作,尽可能高效和快速地将ALS001带给患者。”

TAI™平台的Treg疗法
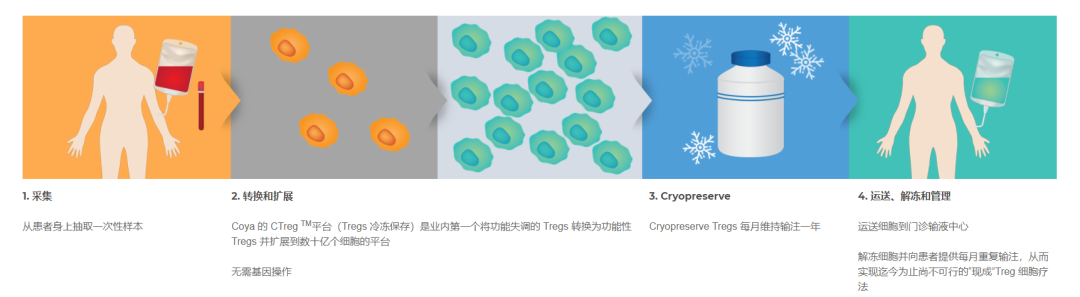
▲ 专有技术平台和可扩展制造流程(图片来源:Coya官网)
采集:从患者身上抽取一次性样本进行分离处理;
转换和扩展:Coya公司的CTreg TM平台(Tregs冷冻保存)是业内第一个将功能失调的Tregs转换为功能性Tregs,转化为具有高度功能性和神经保护作用的细胞,并扩展到数十亿个细胞,之后用于静脉回输。Coya公司平台扩增的Treg表现出基于蛋白质组学表型特征,可由重复物质组成,证实了它们的高度免疫调节和免疫抑制活性。
冷藏保存:低温保存Tregs一年,每月进行维持注射。
运送、解冻和管理:运送细胞到门诊输液中心,解冻细胞后向患者提供每月重复输注。
参考资料:
1.https://www.coyatherapeutics.com/patient-resources.html
2.https://www.biospace.com/article/releases/coya-therapeutics-receives-orphan-drug-designation-from-the-fda-for-als001-an-autologous-treg-cell-therapy-for-the-treatment-of-als/


 点击“阅读原文”,立即报名!
点击“阅读原文”,立即报名!



 个人中心
个人中心
 我是园区
我是园区




