▎药明康德内容团队报道
8月30日,赛诺菲(Sanofi)和Sobi公司发布新闻稿称,美国FDA已接受efanesoctocog alfa(BIVV001)治疗血友病A的生物制品许可申请(BLA),并授予其优先审评资格。
PDUFA日期定于2023年2月28日。
公开资料显示,efanesoctocog alfa是一款由赛诺菲和Sobi公司合作开发和商业化的长效血友病A疗法,
设计用于以一周一次的频率对血友病A患者进行预防性治疗。
密歇根大学Steve Pipe教授表示:“凝血因子疗法仍然是血友病治疗的基石,但这一领域需要创新,以应对与出血保护和繁琐治疗方案相关的挑战。如果获得批准,efanesoctocog alfa
可以在一周的大部分时间内提供接近正常的FVIII因子活性水平
,可能提供新的保护水平。这种治疗获益将代表血友病A患者未满足医疗需求的重要进展,并可能改变预防性治疗前景。”
血友病A是由于缺乏FVIII而导致的一种罕见遗传性出血性疾病。凝血因子的缺乏使患者凝血酶生成不足,导致凝血障碍。血友病A以反复出血及其相关并发症为主要临床表现,其中约80%为关节出血,其并发症主要是慢性出血性关节病变,且可导致严重的关节畸形。目前,血友病A的主要治疗手段是定期输注FVIII,通常患者需要每周接受3~4次FVIII输注,频繁输注给患者的生活带来极大不便。
天然FVIII在血液中的半衰期只有12个小时左右,因为在血液中,它与血管性血友病因子(VWF)结合形成复合体。VWF与FVIII的结合虽然提高了FVIII在血液中的稳定性,但是VWF本身被降解的速度也为FVIII在血液中的滞留时间设置了一个上限,因为当VWF被降解时,与它结合的FVIII也同时被降解。因此,VWF因子被认为是限制
FVIII半衰
期的主要因素。
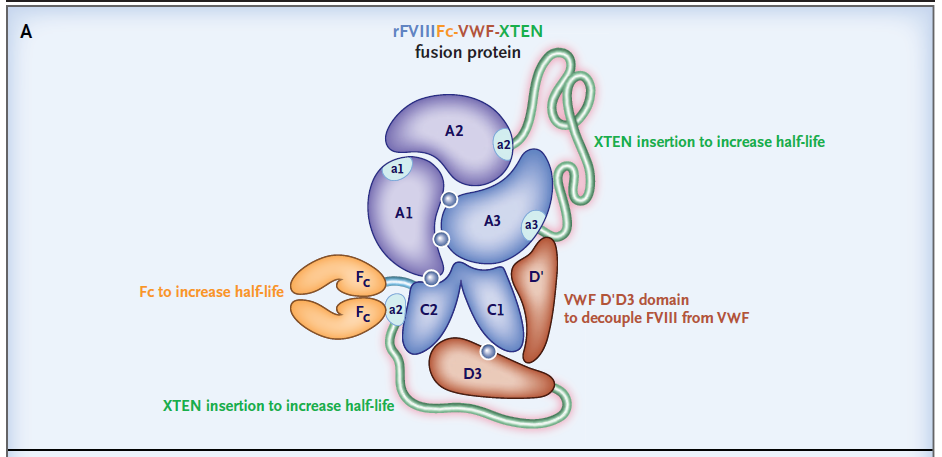
▲Efanesoctocog alfa结构示意图(图片来源:参考资料[3])
Efanesoctocog alfa是设计用于以一周一次的频率对血友病A患者进行预防性治疗的药品。它将FVIII、VWF部分区域、XTEN多肽与新式的Fc融合蛋白结合成复合体,从而延长药品存在血液循环内的时间。这将有望突破VWF设定的半衰期上限,使患者通过一周一次治疗在一周大部分时间中维持接近正常的FVIII活性。此前,efanesoctocog alfa已获得FDA授予治疗血友病A的突破性疗法认定、孤儿药资格和快速通道资格。
此次efanesoctocog alfa的生物制品许可申请得到了关键性3期研究XTEND-1的数据支持。该试验在159名12岁以上的严重血友病A患者中展开,他们此前接受FVIII替代疗法。试验结果显示,每周接受一次efanesoctocog alfa预防性治疗的患者中,52周内中位年出血率(ABR)为0,平均ABR为0.71。在安全性方面,候选药耐受性良好,没有发现针对FVIII的抑制物出现,最常见的治疗中出现的不良事件为头痛、关节痛、跌倒和背痛。XTEND-1试验结果表明,efanesoctocog alfa每周一次预防性治疗,可以显著降低严重血友病A患者中的年出血率,同时它还在预防出血方面表现出相比传统疗法的优效性。
图片来源:123RF
赛诺菲全球开发负责人兼首席医学官Dietmar Berger博士表示,关键性3期研究XTEND-1的结果表明,efanesoctocog alfa能够降低年出血率,具有潜在最佳疗效。他们期待在审评过程中与FDA密切合作,目标是将这种新型疗法带给血友病A患者群体。
在中国,efanesoctocog alfa曾被中国国家药品监督管理局药品审评中心(CDE)纳入
,
拟用于血友病A的成人和儿童患者
。根据中国药物临床试验登记与信息公示平台信息,目前该产品正在进行一项国际多中心(含中国)3期研究(XTEND-ed),以期在既往接受过治疗的重度血友病A患者中,评估候选药的长期安全性和有效性。
[1] Press Release: FDA grants priority review to efanesoctocog alfa for people with hemophilia A. Retrieved Aug 30 , 2022. From https://www.globenewswire.com/news-release/2022/08/30/2506359/0/en/Press-Release-FDA-grants-priority-review-to-efanesoctocog-alfa-for-people-with-hemophilia-A.html
[2] Efanesoctocog alfa met primary and key secondary endpoints in pivotal study in hemophilia A, demonstrating superiority to prior factor prophylaxis treatment. Retrieved March 9, 2022, from https://www.globenewswire.com/news-release/2022/03/09/2399557/0/en/Efanesoctocog-alfa-met-primary-and-key-secondary-endpoints-in-pivotal-study-in-hemophilia-A-demonstrating-superiority-to-prior-factor-prophylaxis-treatment.html
[3] Konkle et al., (2020). BIVV001 Fusion Protein as Factor VIII Replacement Therapy for Hemophilia A. NEJM, DOI: 10.1056/NEJMoa2002699
本文来自药明康德内容团队,欢迎个人转发至朋友圈。转发授权请在「医药观澜」微信公众号留言联系我们。其他合作需求,请联系wuxi_media@wuxiapptec.com。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。








 个人中心
个人中心
 我是园区
我是园区




