▎药明康德内容团队报道
港交所网站最新公示,赛生药业(SciClone Pharmaceuticals)IPO申请已通过港交所聆讯。赛生药业于2020年9月根据《上市规则》第8.12条规定在港交所递交IPO申请,联席保荐人为中金公司、摩根士丹利和瑞士信贷(香港)。根据聆讯后资料集(在医药观澜微信号回复“赛生”可下载PDF),此次港交所IPO募集资金将主要用于收购或授权引入新候选药,以及推动临床阶段候选药开发和商业化等。
值得一提的是,该公司用于治疗口念珠菌病的咪康唑颊含片诺弥可已于上个月在中国获批上市。此外,该公司正在准备就1.2亿美元引进的CD47靶向疗法,与中国国家药监局药品审评中心(CDE)举行新药申请前会议,以获得监管机构批准。

赛生药业专注于存在重大未满足需求的治疗领域,主要包括肿瘤及重症感染。该公司总裁、首席执行官为赵宏先生。招股书显示,该公司历史可追溯至1990年,由Thomas E. Moore先生及Nelson M. Schneider先生于美国成立SciClone US,并于1992年在纳斯达克上市。2017年,在GL资本牵头,鼎晖投资、上达资本、安瀚有限公司及Boying Investments的参与下,该公司完成私有化退市,并进行一系列重组。
目前,赛生药业已建立丰富的在研产品管线。其核心产品日达仙(胸腺法新)已在多个国家获得批准并被写入诊疗指南,可用于治疗肝炎,某些类型的癌症和作为疫苗佐剂使用。此外,该公司通过与诺华(Novartis)、辉瑞(Pfizer)、百特(Baxter)等大型医药公司合作,帮助其产品在中国商业化并推向市场。
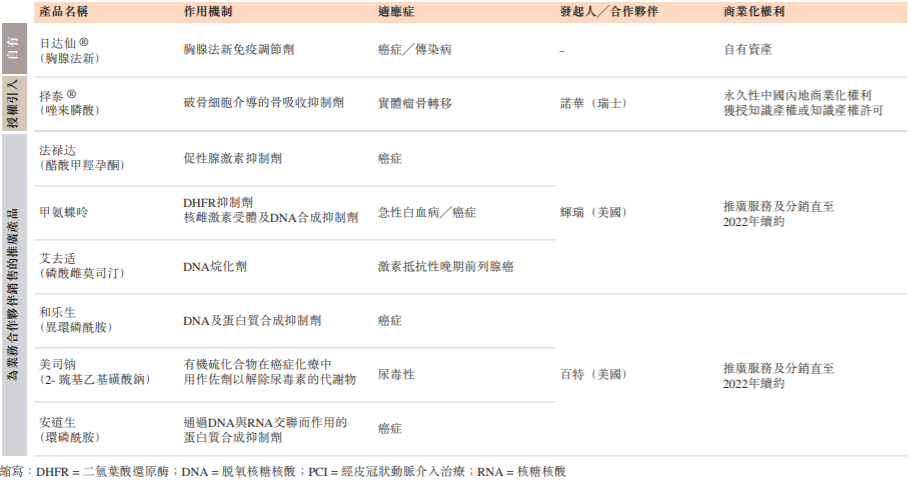
▲赛生药业
已上市产品
(截图来源:参考资料[1])
近年来,赛生药业完成了多项合作。其中,该公司于
2020年7月
初与EpicentRx公司宣布就肿瘤免疫疗法RRx-001达成大中华区的独家授权许可协议,涉及金额高达1.2亿美元。这是一款靶向CD47-SIRPα的小分子免疫疗法,目前正在进行针对小细胞肺癌(SCLC)适应症的3期临床试验,同时赛生药业正在准备与CDE举行新药申请前会议,以获得中国监管机构的批准。
另一款于2020年引进的精准肿瘤药物来自Tarveda Therapeutics。
2020年3月
,赛生药业与Tarveda公司签署一项许可协议,并获得后者微型药物偶联物PEN-866在大中华地区共同开发和商业化的权益,涉及金额总额高达7500万美元。
PEN-866是由热休克蛋白(HSP90)受体与SN-38(一种有效的抗癌有效载荷)相连而成
,可以与HSP90高亲和性结合,进而释放SN-38起到靶向杀伤肿瘤的作用。
此外,赛生药业还在2020年12月与Y-mAbs Therapeutics就Danyelza(naxitamab-gqgk) 和omburtamab两款产品达成独家授权许可协议。Danyelza已于2020年11月获FDA批准, 用于与粒细胞-巨噬细胞集落刺激因子(GM-CSF)联合治疗对既往治疗表现出部分缓解、轻微缓解或疾病稳定的复发/难治性高危神经母细胞瘤儿童(1岁及以上)和成人患者。Y-mAbs Therapeutics 拟于2021年初向FDA递交omburtamab的首个生物制品许可申请(BLA)申请,用于治疗中枢神经系统/软脑膜转移的神经母细胞瘤。
聆讯后资料显示,赛生药业已有多款产品目前正处于临床开发阶段。其中,用于治疗口咽念珠菌病
的诺弥可已在中国获批,另外还有4
款产品已进入后期临床。
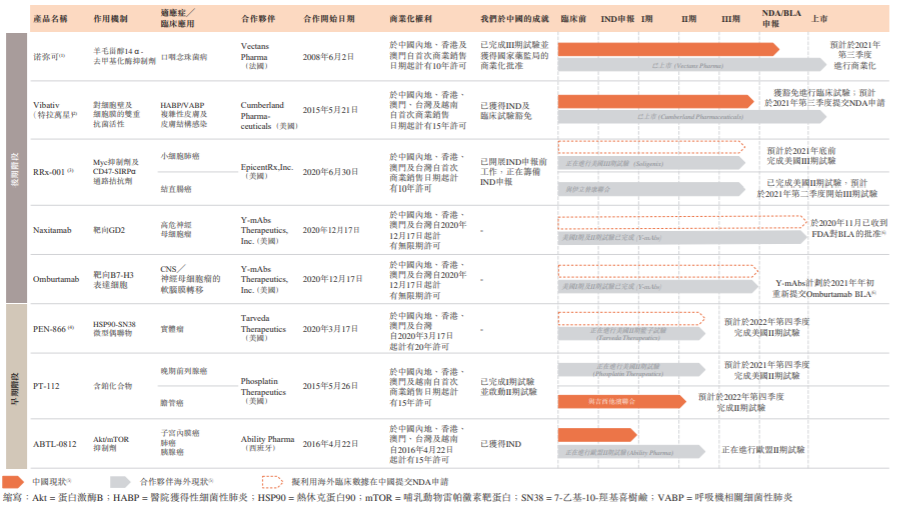
▲
赛生药业在研产品
(截图来源:参考资料[1])
诺弥可:
一种用于治疗口咽念珠菌病(OPC)的咪康唑颊含片
,对OPC中观察到的最常见念珠菌具有广谱抗真菌活性,包括光滑念珠菌、克鲁氏梭菌和热带念珠菌。该产品已于今年1月在中国获批上市,用于治疗口念珠菌病。
Vibativ
:注射脂糖肽类抗生素
,作用于由金黄色葡萄球菌药物敏感隔离(包括甲氧西林敏感及耐药隔离),及复杂性皮肤和皮肤结构感染(CSSSI)引起的感染或呼吸机相关细菌性肺炎。目前,该产品已进展至3期临床。
Naxitamab
:抗GD2抗体,通过靶向GD2(一种神经母细胞瘤细胞表面的肿瘤抗原)起效。根据公开资料,naxitamab因其适度的毒性、较短的输注时间及门诊可管理而优于其他基于抗体的GD2靶向疗法。Naxitamab已在美国完成1期及2期试验,并于2020年11月收到FDA对该药的BLA批淮。赛生药业计划利用海外临床数据在中国提交naxitamab的NDA申请。
Omburtamab:抗B7-H3抗体,靶向人体实体瘤(包括胚瘤、恶性上皮肿瘤、肉瘤及脑癌)内的B7-H3表达细胞,并与B7-H3分子上的FG环依赖构象(一个对其生物学功能至关重要的区域)结合。赛生药业计划利用海外临床数据在中国提交omburtamab的NDA申请。
PT-112:一种创新型铂类小分子药物
,通过细胞凋亡、免疫特性及高耐受性来抗肿瘤效果。该产品设计初衷是为了减少传统铂类药化疗中的毒性及耐药性。目前正在中国和美国进行1/2期临床研究。
ABTL-0812
:一种小分子癌症药物,通过激活PPAR受体和Trib3基因,从而抑制Akt/mTOR途径。这种途径在大多数人类癌症中被过度激活,支持肿瘤生长。在晚期癌症患者的1期临床试验中,ABTL-0812已显示出疗效好、毒性低、耐受性高的特点。
根据聆讯后资料,本次募集资金(净额)的主要用途有:
约30%将用于投资中国或其他全球市场的潜在药物收购目标,并为新候选药物的授权引入提供资金;
约26%将用于临床阶段候选产品的开发及商业化提供资金,包括为RRx-001、naxitamab、omburtamab、PEN-866、PT-112、 ABTL-0812等产品的计划临床试验、注册备案筹备及潜在商业发布(包括销售及营销)提供资金;
约6%将用于拨付上市产品组合作其他临床应用的持续临床研究。
祝贺赛生药业通过港交所聆讯(在医药观澜微信号回复“赛生”可下载PDF),希望该公司港股IPO进展顺利,早日在资本的助力下为患者带来更多创新疗法。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。
欢迎扫码关注“
医药观澜
”微信公众号,了解更多中国医药创新动态。

注:本文旨在介绍医药健康研究进展,不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
[1]赛生药业港交所IPO聆讯后资料. Retrieved Jan 31,2021, from https://www1.hkexnews.hk/app/sehk/2020/102582/documents/sehk21020100007_c.pdf
[2]Tarveda Therapeutics and SciClone Pharmaceuticals International Establish Licensing Agreement for PEN-866 in Greater China. Retrieved Mar 19 2020 from https://www.tarvedatx.com/3-19-20-tarveda-therapeutics-and-sciclone-pharmaceuticals-international-establish-licensing-agreement-for-pen-866-in-greater-china
[3]EpicentRx Inc.与SciClone Pharmaceuticals就RRx-001达成大中华区产品许可协议 Retrieved July 1,2020, from http://www.sciclone.com/Modules/newsDetail.aspx?id=101









 个人中心
个人中心
 我是园区
我是园区




