Anavex Life Sciences Corp.(AVXL)报告,SIGMAR1 mRNA表达所建立的反应预测生物标志物与原发性和继发临床疗效终点的反应有显著相关。这是一个概念随机、双盲证明,安慰剂对照II期试验:随机132例帕金森病痴呆(PDD)患者(1:1:1)与目标剂量30mg, 50mg ANAVEX®2-73或安慰剂。

ANAVEX®2-73激活sigma-1受体(SIGMAR1)。数据表明,SIGMAR1的激活可恢复体内完整housekeeping功能,对恢复神经细胞稳态和促进神经可塑性至关重要。最近独立研究发现对SIGMAR1激活作为慢性中枢神经系统代偿机制的有益作用的认识疾病。
帕金森病(PD)是一种慢性中枢神经系统疾病,是阿尔茨海默病后第二大年龄相关疾病。研究首次证明药物特异性生物标志物与帕金森病的临床疗效终点相关。
ANAVEX®2-73治疗可显著提高SIGMAR1(p=0.035)mRNA表达,SIGMAR1是ANAVEX靶向受体的ANAVEX®2-73,与主要认知疗效终点、CDR系统注意力连续性(CoA)(p=0.029)和CDR系统注意力能力(PoA)(p=0.015)和继发性帕金森病疗效终点运动障碍协会统一帕金森病分级量表(MDS-UPDRS)相关,MDS-UPDRSPart III (p = 0.024)和MDS-UPDRS Total (p = 0.038)。
PD相关评分
ANAVEX®2-73高剂量显示MDS-UPDRS总分与安慰剂(ITT人群)相比,有统计学显著改善(p=0.034)。从基线到试验结束14周,高剂量组MDS-UPDRS总得分提高了-10.98分,安慰剂组病情恶化3.53分,调整后平均差-14.51分(p=0.034)。与14周内的相对改善18.9%相对应。远远超过临界值-7.1。作为参考,文献中观察到的帕金森病患者MDS-UPDRS总得分的恶化在每年3.99至7.45分之间。
ANAVEX®2-73不仅能减缓中度帕金森病患者的运动和非运动症状的进展。还导致临床有意义的改善,根据帕金森病症状严重程度的全球综合评分、MDS-UPDRS总分高于治疗标准,包括多巴胺能疗法、左旋多巴和其他抗PD药物,治疗14周后,表明ANAVEX®2-73具有减缓和逆转帕金森病进展症状的能力,这是一种迫切的医疗需求。
睡眠是一个主观性和客观上跟踪变量,包括睡眠连续性或睡眠障碍症状的发生率。ANAVEX®2-73不影响睡眠,对REM睡眠行为障碍有积极影响。
痴呆相关得分
先前报告的与老年痴呆症相关的认知结果测量结果显示,在ANAVEX®2-73高剂量和安慰剂之间CDR系统幕式记忆的显著改善为+42.22,剂量依赖(p=0.003)。CDR系统幕式记忆与ADASCog评分(r=0.7)高度相关(70%)。高剂量组患者计算的相应ADASCog平均值与基线评分的变化为-1.9(改善),从基线到14周平均改善8%。ANAVEX®2-73组和安慰剂组在14周基线变化时,相应ADASCog评分(p=0.015)提高了4.0分。
ANAVEX®2-73目前正在晚期安慰剂对照ANAVEX中进行试验®2-732b/3期临床阿尔茨海默病研究,最近完成了注册,并使用与上述已完成的帕金森病痴呆(ANAVEX)相同的给药方案®2-73-PDD-001)具有区分患者选择标准的研究。
下一步
MichaelJ. Fox Foundation (MJFF) 最近授予Anavex一项研究补助金,用于ANAVEX®2-73帕金森病成像临床试验,该赠款为建立Anavex®2-73的临床前研究提供了充分的资金。
此次生物标志物相关的概念II期的有效性数据(ANAVEX®2-73-PDD-001)帕金森病痴呆患者的研究数据,将提交美国食品药品监督管理局(FDA)寻求监管指导。
AnavexLife Science的管线包括口服小分子药物Anavex®2-73治疗阿尔茨海默病、帕金森病和Rett综合征和ANAVEX®3-71治疗额颞部痴呆。
关于帕金森病(PD)
帕金森病是一种慢性进展性神经疾病,其特征是众所周知的运动症状包括颤抖、四肢僵硬、动作迟缓、姿势和平衡困难,以及非运动症状。它是美国第二常见的神经疾病,大约有100万人,全世界有1000多万人患有这种疾病。帕金森病在60岁以上的人中更为常见,随着人口平均年龄的增加,帕金森病的患病率预计将显著增加。目前帕金森病的治疗方法仅能有效地控制疾病症状,主要通过使用左旋多巴和多巴胺激动剂。随着疾病的进展和多巴胺能神经元的持续丢失,这些药物最终在治疗症状方面的效果会降低。
帕金森病痴呆(PDD)
据估计,多达80%的帕金森病患者最终会患帕金森病痴呆。帕金森病引起的大脑变化始于一个在运动中起关键作用的区域。随着帕金森氏症的大脑逐渐扩散,开始影响心理功能,包括记忆和注意力,判断能力,以及逻辑能力。
ANAVEX®2-73-PDD-001临床研究(NCT03774459)
ANAVEX®2-73-PDD-001是一项国际性、双盲、多中心、安慰剂对照的概念II期临床研究,随机132例帕金森病痴呆(PDD)患者(PDD)与目标剂量30mg,50mgANAVEX®2-73(1:1:1)或安慰剂。在14周的研究期间,评估了相关的反应、SIGMAR1、安全性和认知效能、MDS-UPDRS、活动图和睡眠功能的生物标志物。
研究纳入要求根据运动障碍协会临床诊断标准(MovementDisorder Society Task Force clinical diagnostic criteria)以及蒙特利尔认知评估(MoCA)评分13-23,诊断符合英国帕金森病学会脑库诊断标准和可能PD痴呆(PDD)的诊断标准。用NGS分析血液标本中DNA和RNA。
研究对象被允许服用稳定的抗帕金森病药物方案(包括levodopa,dopamine agonists, MAO-B inhibitors, 或 entacapone)。以及Cholinesterase抑制剂,rivastigmine, donepezil 和galantamine(Exelon®,Aricept® 或Reminyl®)治疗。
研究发现ANAVEX®2-73口服剂量50mg,每日一次,耐受性良好。结果显示,认知药物研究(CDR)计算机评估系统分析具有临床意义、剂量依赖性和统计学显著性的改善。本研究了确认ANAVEX®2-73通过SIGMAR1激活起作用,并证明精准靶向治疗的可能性。
完成ANAVEX®2-73-PDD-001试验之后,参与者将参加一项为期48周的自愿开放标签扩展研究,ANAVEX®2-73-PDD-EP-001,继续评估肠道微生物群的安全性、长期疗效和变化
AnavexLife Sciences Corp
AnavexLife Sciences Corp.是一家生物制药公司,致力于开发用于治疗神经退行性疾病和神经发育性疾病(包括阿尔茨海默病、帕金森病、Rett综合征和其他中枢神经系统(CNS)疾病)的差异化疗法,疼痛和各种癌症。Anavex的主要候选药物Anavex®2-73(blarcamesine),成功完成了阿尔茨海默病的IIa期临床试验,最近完成了帕金森病痴呆症的II期概念验证研究和Rett综合征成年患者的II期研究。ANAVEX®2-73是一种口服候选药物,通过靶向sigma-1和muscarinic受体恢复细胞内稳态。临床前研究表明,它有可能阻止和/或逆转阿尔茨海默病的进程。在动物模型中也表现出抗惊厥、抗遗忘、神经保护和抗抑郁的特性,表明其治疗其他中枢神经系统疾病(包括癫痫)的潜力。Anavex®2-73靶向sigma-1和毒蕈碱受体,在转基因(3xTg-AD)小鼠中显示出针对阿尔茨海默病主要特征的疾病修饰活性,包括认知缺陷、淀粉样蛋白和tau病理学。在临床前试验中,ANAVEX®3-71对线粒体功能障碍和神经炎症具有有益作用。
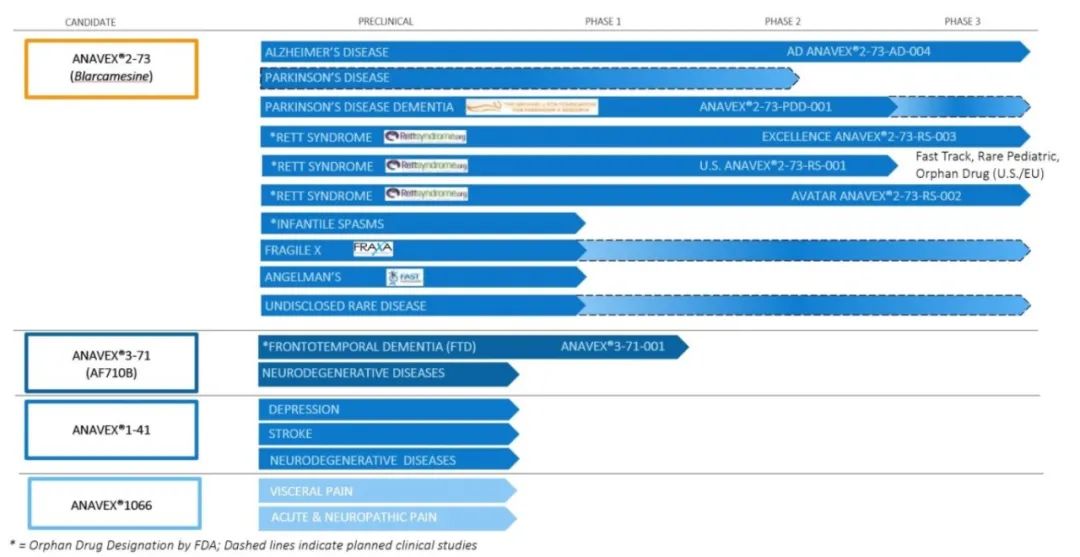
公司管线:



 个人中心
个人中心
 我是园区
我是园区




