「 本文共:17条资讯,阅读时长约:3分钟 」




1.再鼎引进复方抗生素报产。国家药监局受理再鼎医药从Entasis公司(已被Innoviva收购)引进的舒巴坦钠-度洛巴坦钠(SUL-DUR)的新药上市申请,用于治疗鲍曼不动杆菌(包括多重耐药和耐碳青霉烯类菌株)引起的感染。在III期ATTACK研究中,与多黏菌素相比,SUL-DUR治疗使碳青霉烯耐药ABC感染患者的28天全因死亡率更低(19%vs32.3%)。在美国,FDA已将SUL-DUR的上市申请纳入优先审评,PDUFA日期为明年5月29日。
2.度普利尤单抗新适应症拟纳入优先审评。赛诺菲和再生元联合开发的IL-4/IL-13单抗度普利尤单抗注射液获CDE拟纳入优先审评,用于治疗成人结节性痒疹。度普利尤单抗能选择性抑制IL-4/IL-13介导的关键信号,阻断Th2型炎症通路,减轻Th2型炎症的病理性反应,从而治疗Th2型炎症相关疾病。此前,该疗法已在中国获批用于中重度特应性皮炎适应症。
3.联拓引进心肌病创新药拟纳入优先审评。联拓生物从百时美施贵宝引进的心肌肌球蛋白别构抑制剂mavacamten胶囊获CDE拟纳入优先审评,拟用于治疗症状性梗阻性肥厚型心肌病(oHCM)。此前,该新药已被CDE纳入突破性治疗品种。mavacamten能将整体肌球蛋白群转变到节能、可募集的超松弛状态,旨在减少患者的心脏过度收缩症状。2022年4月,mavacamten已获FDA批准上市,为首款心肌肌球蛋白别构可逆性抑制剂。
4.北京中因眼科基因疗法上I/II期临床。中因科技基因替代治疗药物ZVS101e注射液在治疗结晶样视网膜变性(BCD)的I/II期临床完成首例受试者入组及给药。ZVS101e旨在通过rAAV病毒将正常的CYP4V2基因拷贝携带到患者视网膜细胞中,补充视网膜细胞中正常CYP4V2基因的表达量,恢复视网膜细胞功能。此前,该产品已获FDA授予孤儿药资格。
5.和誉抗耐药FGFR抑制剂国内获批临床。和誉医药自主研发的新一代抗FGFR耐药突变抑制剂ABSK121获国家药监局临床试验默示许可,拟开展针对晚期实体瘤的首次人体Ⅰ期临床试验。在多个临床前模型中,ABSK121显示出良好的抗肿瘤功效,并在FGFR耐药突变肿瘤模型中也具有较好的药效。2022年11月,该新药已获FDA批准开展临床研究。
6.康诺亚Claudin 18.2-ADC授权阿斯利康。康诺亚与乐普生物共同宣布与阿斯利康就潜在“first-in-class”的Claudin 18.2靶向ADC药物CMG901达成全球独家授权协议。CMG901由康诺亚和乐普生物的合资公司KYM Biosciences Inc.开发,针对晚期实体瘤的治疗。根据协议,KYM将获得6300万美元的预付款和超过11亿美元的研发和销售等里程碑后期付款,以及产品的销售分成。阿斯利康将获得CMG901研究、开发、注册、生产和商业化的独家全球许可。
7.华东医药引进GLP-1R/GIPR双靶点降糖药。华东医药旗下中美华东宣布与日本SCOHIA PHARMA公司就后者临床早期GLP-1R/GIPR双靶点降糖疗法SCO-094项目扩大战略合作。2021年6月1日,中美华东已获SCO-094在中国、韩国、澳大利亚等25个亚太国家和地区(不含日本)的独家开发、生产及商业化权益。根据新的合作协议,中美华东将获得SCO-094及其衍生产品在全球(包括日本)的独家开发、生产及商业化权益。


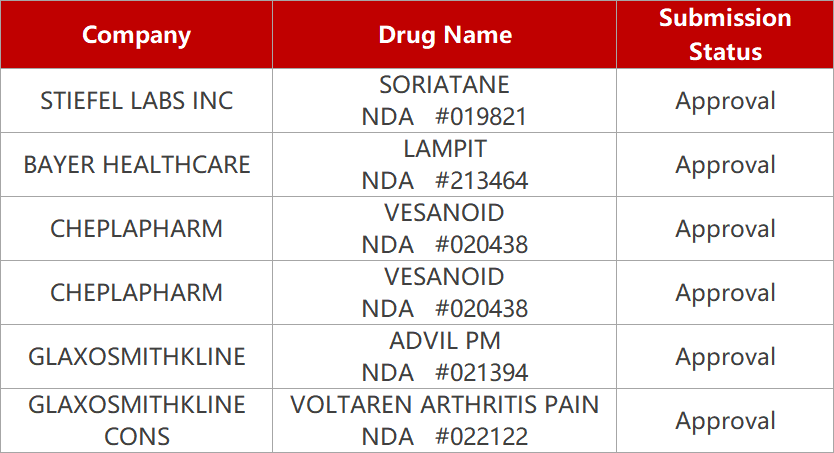
1.Alnylam公司RNAi疗法在美报sNDA。Alnylam公司RNAi疗法patisiran(商品名:Onpattro)的补充新药申请(sNDA)获FDA受理,用于治疗伴有心肌病的转甲状腺素蛋白介导的淀粉样变性(ATTR-CM)。PDUFA日期为2023年10月8日。patisiran通过靶向并沉默TTR的mRNA,从而阻止野生型和突变TTR蛋白的产生,旨在解决心衰根本原因。在Ⅲ期临床中,patisiran治疗组患者的6分钟行走检测结果较基线的变化显著优于对照组。
2.新型老花眼滴眼液在美报NDA。FDA受理Orasis公司低剂量毛果芸香碱(0.4%)滴眼液CSF-1用于治疗老花眼的新药上市申请(NDA),PDUFA日期为2023年10月22日。在两项III期研究(NEAR-1和NEAR-2)中,CSF-1治疗第8天时显著提高视力表多读三行的患者比例;接受第一剂和第二剂治疗后1小时内,患者多读三行的比例由40%提高至50%(p<0.0001);而且CSF-1可在20分钟起效,疗效可持续达8小时。
3.BMS重磅PD-1单抗长期疗效数据积极。百时美施贵宝PD-1抑制剂Opdivo(纳武利尤单抗)用于辅助治疗术后高危肌层浸润性尿路上皮癌的Ⅲ期试验最新数据积极。中位随访为36.1个月时,Opdivo治疗组无疾病生存期(DFS)较安慰剂组显著改善(中位DFS:22.0个月vs10.9个月),疾病复发或死亡风险降低29%;在PD-L1表达≥1%的患者中,两组中位DFS分别为52.6个月和8.4个月,疾病复发或死亡风险降低48%。药物的安全性与已知研究一致。
4.辉瑞CD3/BCMA双抗获FDA优先审评。辉瑞CD3/BCMA双特异性抗体elranatamab的生物制品许可申请(BLA)获FDA优先审评资格,用于治疗复发/难治性多发性骨髓瘤患者。一项Ⅱ期MagnetisMM-3临床数据显示,在中位随访10.4个月时,接受elranatamab作为首次BCMA靶向治疗的患者达到61%的客观缓解率以及55%的非常好的部分缓解率。此前,该新药已获FDA突破性疗法认定。欧洲药品管理局(EMA)日前也已受理了elranatamab的上市许可申请(MAA)。
5.默沙东/Moderna癌症疫苗获FDA突破性疗法认定。Moderna与默沙东联合开发的个性化mRNA肿瘤疫苗mRNA-4157/V940获FDA突破性疗法认定,联合PD-1单抗Keytruda辅助治疗完全切除后的高危黑色素瘤患者。在IIb期研究KEYNOTE-942中,联合辅助治疗较Keytruda显著改善患者的无复发生存期,使复发或死亡的风险降低44%(HR=0.56 [95% CI,0.31-1.08];单侧p值=0.0266)。
6.全球首款TCR疗法首年业绩出炉。Immunocore公司公布该公司战略布局和全球首款TCR疗法Kimmtrak上市首年销售业绩。该产品Q4净销售额约为5000万美元,在2022年全年销售额约为1.4亿美元(9.6亿人民币)。2022年1月,Kimmtrak获得FDA的全球首批,用于治疗HLA-A*02:01阳性、不可切除性或转移性葡萄膜黑色素瘤。Kimmtrak在临床中可降低患者的死亡风险49%(HR=0.51,p<0.0001),中位OS约22个月。


1.2022年上海总和生育率为0.7。20日,上海市卫健委在官网发布《上海市2022年度人口监测统计数据》。数据显示,上海全市总和生育率为0.7,平均初育年龄为30.36岁,平均生育年龄为31.18岁。与上海相比,2021年,新加坡的总和生育率为1.12,东京的总和生育率为1.09,首尔的总和生育率为0.63。目前学界普遍认为,要达到正常的“人口更替”水平、保持上下两代之间人口的基本平稳,总和生育率至少要达到2.1。
2.玻利维亚确诊超8900例登革热病例。当地时间2月22日,玻利维亚卫生部通报称,截至当天,该国累计登革热确诊病例达8909例,其中死亡29例。近六成的死亡患者为未成年儿童。目前,玻利维亚中部的圣克鲁斯省疫情最为严重,确诊病例数量超过8800例,死亡25例。当地媒体报道称,这是近十年来该国遭遇的最严重的登革热疫情。
3.第三名艾滋病患者被治愈。来自英国《自然·医学》月刊的一篇最新研究论文显示,一名获称“杜塞尔多夫病人”的艾滋病患者约10年前接受干细胞移植,停止抗艾药物4年后体内未再检测到活跃的艾滋病病毒,从而成为继“柏林病人”和“伦敦病人”后第三名被治愈的艾滋病患者。新研究进一步证明,针对CCR5受体的基因编辑疗法可能成为治愈艾滋病的关键。


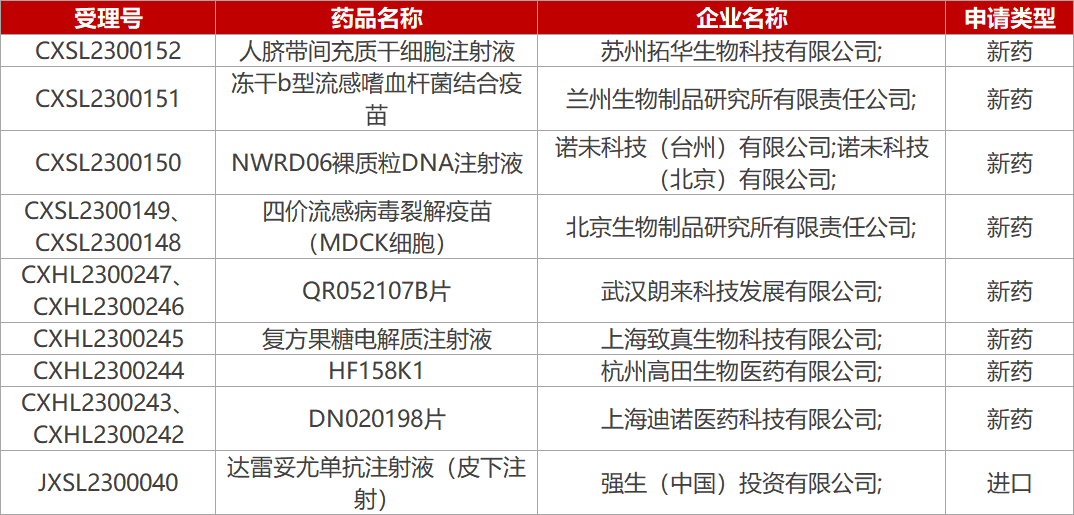
1. CDE新药受理情况(02月23日)


上个交易日 A 股医药板块 -0.73%
涨幅前三 跌幅前三
N 峆一 +52.46% 特宝生物 -6.18%
奥 赛 康 +8.44% 特一药业 -4.66%
诚意药业+3.65% 川宁生物 -4.59%
【甘李药业】甘精胰岛素注射液上市许可申请获得美国FDA正式受理。
【翰宇药业】全资子公司翰宇武汉醋酸加尼瑞克原料药及卡贝缩宫素原料药获得上市申请批准通知书。
【中关村】下属公司华素生物科技(北京)取得重组新型冠状病毒S蛋白三聚体及其制备方法与应用发明专利证书。
- The End -




 个人中心
个人中心
 我是园区
我是园区




