▎药明康德内容团队编辑
Intra-Cellular Therapies公司日前宣布其药品Caplyta(lumateperone)作为单药治疗具有混合特征的重度抑郁症(MDD)与双相抑郁症(bipolar depression)患者重度抑郁发作的3期临床试验积极顶线结果。分析显示,试验达成主要终点,在第6周时,Caplyta组患者的抑郁症状具有统计学和临床意义的改善。

双相情感障碍(bipolar disorders)和MDD是高发的严重精神疾病。双相抑郁症是双相情感障碍最常见的临床表现。与躁狂相(manic phase)相比,双相情感障碍患者通常停留在抑郁相(depressive phase)的时间更长。当患者的重度抑郁发作时,约三分之一的双相情感障碍或MDD患者表现为混合特征。混合特征定义为患者在抑郁发作期间同时出现阈下躁狂症状,或患者在躁狂发作期间同时出现阈下抑郁症状。具混合特征的抑郁症患者其疾病严重程度、自杀意念、自杀率、复发率与合并症产生的机率更高。与无混合特征的抑郁患者相比,这类患者更难以治疗。
Caplyta(42 mg)是一种口服、每日一次的非典型抗精神病药,获批用于治疗成人1型或2型双相情感障碍(双相抑郁)相关的精神分裂症和抑郁发作,作为单药治疗和锂剂或丙戊酸盐的辅助治疗。虽然Caplyta的作用机制尚不清楚,但其疗效可通过中枢5-羟色胺5-HT2A受体的拮抗活性和中枢多巴胺D2受体的突触后拮抗活性联合介导。Caplyta正被研究用于治疗重度抑郁症,以及其他神经精神和神经系统疾病。

此次所公布的403试验是一项全球性、随机双盲、安慰剂为对照的3期试验,旨在评估Caplyta单药治疗MDD或1、2型双相障碍相关重度抑郁发作患者的疗效和安全性,这些患者符合精神障碍诊断与统计手册第5版(DSM-5)的混合特征标准。此外,患者的Montgomery Asberg抑郁评定量表(MADRS)总分≥24,总体印象-严重程度量表(CGI-S)总分≥4,杨氏躁狂评定量表(YMRS)评分为4-16。
分析显示,在第43天,接受42 mg Caplyta治疗的每个病患群体,其在主要终点(MADRS评分)皆具统计学显著的改善,包括:
与安慰剂组相比,接受Caplyta治疗的具混合特征MDD和双相抑郁症患者,其MADRS总分降低5.7分(p<0.0001)。
与安慰剂组相比,接受Caplyta治疗的具混合特征MDD患者,其MADRS总分降低5.9分(p<0.0001)。
与安慰剂组相比,接受Caplyta治疗的具混合特征双相抑郁症患者,其MADRS总分降低5.7分(p<0.0001)。
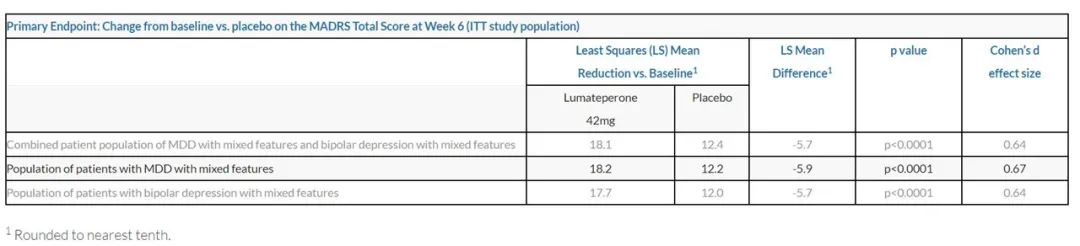
▲Caplyta试验结果摘要(图片来源:参考资料[1])
此外,在第43天,接受Caplyta治疗的每个病患群体也在关键次要终点CGI-S评分上,与安慰剂组相比呈现显著统计学差异性。在试验中Caplyta展现良好安全性和耐受性特征,此与既往试验结果一致。
“我们对这项在具混合特征MDD和双相抑郁症,难以治疗病患群中所得到非常成功试验结果感到相当满意,”Intra-Cellular Therapies公司董事长兼首席执行官Sharon Mates博士说道,“这项试验在这些患者群体中提供了概念性证明,并进一步验证Caplyta在治疗情绪障碍疾病方面的广泛潜力。我们期待与美国FDA讨论这些结果以确定该项目的下一步。”
大家都在看



▲如您有任何业务需求,请长按扫描上方二维码,或点击文末“阅读原文/Read more”,即可访问业务对接平台,填写业务需求信息

▲欲了解更多前沿技术在生物医药产业中的应用,请长按扫描上方二维码,即可访问“药明直播间”,观看相关话题的直播讨论与精彩回放
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。


分享,点赞,在看,聚焦全球生物医药健康创新



 个人中心
个人中心
 我是园区
我是园区




