拜耳Copanlisib注射用冻干制剂纳入优先审评程序
收藏
关键词:
注射优先审评拜耳制剂
资讯来源:生物探索 + 订阅账号
所属行业:小分子靶向药 + 订阅行业
发布时间:
2021-04-15
根据国家药品监督管理局最新公示,拜耳旗下PI3K抑制剂
Copanlisib
注射用冻干制剂已于4月14日纳入优先审评品种名单,拟定适应症为
既往至少接受过两种系统性治疗的复发或难治性滤泡性淋巴瘤(FL)成人患者
。
滤泡性淋巴瘤是来源于滤泡生发中心的成熟b细胞淋巴瘤,也是最常见的非霍奇金淋巴瘤之一,恶性度较低,化疗和放疗对这一疾病具有较好的治疗效果。不过,患者的病情在出现缓解后,经常会复发,因此罹患滤泡性淋巴瘤的病人终生都需要接受定期的检查和监测,否则这类疾病便可能转变为恶性淋巴瘤,危及生命。
Copanlisib是一种通过静脉注射的磷脂酰肌醇-3-激酶(PI3K)抑制剂,对于在恶性B细胞中表达的PI3K-α和PI3K-δ两种亚型都具有抑制活性,可通过细胞凋亡和抑制恶性B细胞的增殖来诱导肿瘤细胞死亡。
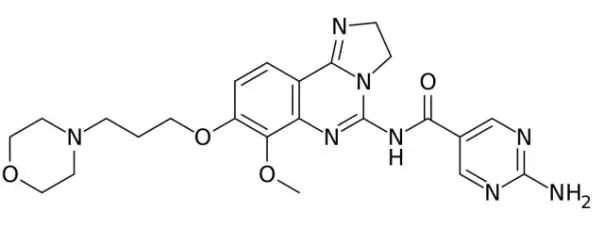
Copanlisib分子结构式(图片来源:维基百科)
2017年9月,Copanlisib获得美国食品药品监督管理局批准,用于治疗罹患复发性滤泡性淋巴瘤,且已经接受了至少两次系统疗法的成人患者。该适应症的加速批准基于一项开放标签、单臂II期CHRONOS-1研究结果,接受Copanlisib治疗的患者总体缓解率(ORR)为59%,其中CR率为14%。2年随访后更新的最新结果显示,FL人群的ORR为59%,其中CR率为20%。
在最近开幕的2021AACR虚拟会议上,拜耳(Bayer)公布了Copanlisib与Rituximab联合使用治疗复发性惰性非霍奇金淋巴瘤(iNHL)的III期临床试验结果。经过联合治疗,iNHL患者的疾病进展和死亡风险降低了48%,中位生存期由13.8个月提高至21.5个月。
除了拜耳的Copanlisib已申报上市外,国内外还有多款PI3K抑制剂处于不同临床试验阶段,其中诺华的Alpelisib、Buparlisib,罗氏的Taselisib 、GDC-0077均处于III期临床阶段,正大天晴、信达、和记黄埔、石药等中国本土企业的产品目前处于I/II期临床阶段。
参考资料:
[1]CDE官网
[2]https://mp.weixin.qq.com/s/9iu5eFeE_j5_eABdjnYPvQ
免疫疗法 | 生物仿制药 | 疫苗 | 耐药性 | 药物靶点 | 健康生活 | 药企新闻 | 药物盘点 | 制药技术 | 药物副作用
白血病
| 肺癌
| 胃癌
| 结直肠癌
| 肝癌
| 乳腺癌
| 胰腺癌
| 心血管疾病
| 神经退行性疾病
| 肠道微生物
体外诊断
| 医疗器械
| 生物纳米
| 3D打印
| 基因检测
| 单细胞测序
| 基因编辑
| 辅助生殖
| 人工智能
| 精准医学
抗癌药
| 4+7带量采购
| 耗材
| 备案制
| 注册人制度
| 健康中国
| 新版基药目录
| AI医疗器械
| 远程医疗
| 同股不同权
IPO
| 融资
| 合作
| 基金
| 港交所
| 科创板
| 创业板
| 研发投入
| 收购
| 市场&消费




 药选址
药选址



