
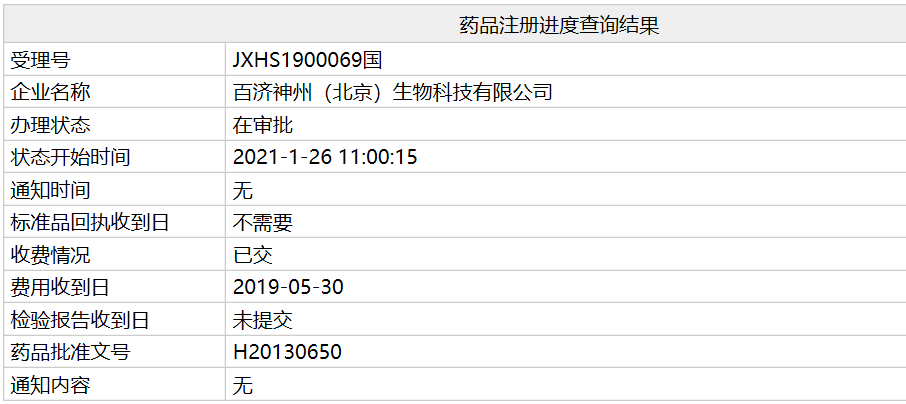
2月1日,国家药监局官网显示,百济神州/新基按新注册分类5.1类申报的注射用紫杉醇(白蛋白结合型)上市申请(受理号:JXHS1900069 )已处于“在审批”阶段,有望于近期获得NMPA批准上市。经查证,此次获批的是新适应症,注射用紫杉醇(纳米蛋白颗粒结合型)联合吉西他滨用于一线治疗转移性胰腺癌(mPC)。此前,该品种曾获NMPA批准用于治疗转移性或复发性乳腺癌。
白蛋白紫杉醇由美国Abraxis BioScience公司开发,是一种紫杉醇与白蛋白结合的全新制剂,克服了普通紫杉醇水溶性差、效率低和副作用大等缺点,于2005年1月被FDA批准上市治疗乳腺癌(商品名Abraxane),随后又获批治疗肺癌、胰腺癌。2010年新基以29亿美元首付款收购Abraxis,将Abraxane收入囊中。2019年11月BMS完成对新基的收购工作,现在Abraxane属于BMS(百时美施贵宝)。
中国于2008年批准新基Abraxane进口药品,2018年,Abraxane的全球销售额是10.62亿美元。百济神州于2017年7月获得Abraxane的中国市场权益,根据协议,目前BMS负责按照法规要求进行生产、注册和进口许可证的维护,以及为中国市场提供成品制剂。
注射用紫杉醇(白蛋白结合型)为第二批集采品种,国内此前中标企业为新基(1150元/支)、石药(747元/支)和恒瑞(780元/支)3家企业。2020年3月,新基Abraxane生产设施因不符合我国GMP要求,被药监局暂停进口、销售和使用,百济神州Abraxane集采中标资格也随之取消。
3月27日,上海药品阳光采购平台公布《关于确定部分地区注射用紫杉醇(白蛋白结合型)替补供应企业的通知》。石药和恒瑞分走了百济此前中选地区,采购周期为2年,首年约定采购量比例为70%。
对于质量不合格事件,百济已于3月25日发布公告做了解释,并表示BMS已向国家药品监督管理局递交更换生产厂的补充申请,从其另一家工厂为中国供货。该申请目前正在审评中。
截止目前该品种共有恒瑞、石药、齐鲁、科伦4家国产厂家过评,海正、扬子江处于一致性评价申报阶段。科伦目前在国内的最新招标价为690元/支,齐鲁为698元/支。

点亮“在看”,好文相伴



 个人中心
个人中心
 我是园区
我是园区




