▎药明康德内容团队报道
12月22日,中国国家药品监督管理局药品审评中心(CDE)网站最新公示,阿斯利康(AstraZeneca)在中国申报的奥拉帕利(olaparib)拟纳入优先审评,拟开发适应症为:转移性去势抵抗性前列腺癌。另有两款生物新药benralizumab和tezepelumab获得临床试验默示许可。其中奥拉帕利是一款“first-in-class”PARP抑制剂;
benralizumab是一款IL-5Rα抑制剂
;
tezepelumab是一款潜在“first-in-class”TSLP抑制剂。
拟开发适应症:特定转移性去势抵抗性前列腺癌成人患者的单药治疗
奥拉帕利是阿斯利康和默沙东(MSD)联合开发的一款“first-in-class”PARP抑制剂,也是首个获批的PARP抑制剂。
该药靶向DNA损伤修复反应(DDR)通路,利用“合成致死“原理,在杀伤癌细胞的同时,不影响健康细胞。该药于2014年12月首次在美国获批上市,用于治疗携带BRCA种系基因突变的晚期卵巢癌患者。
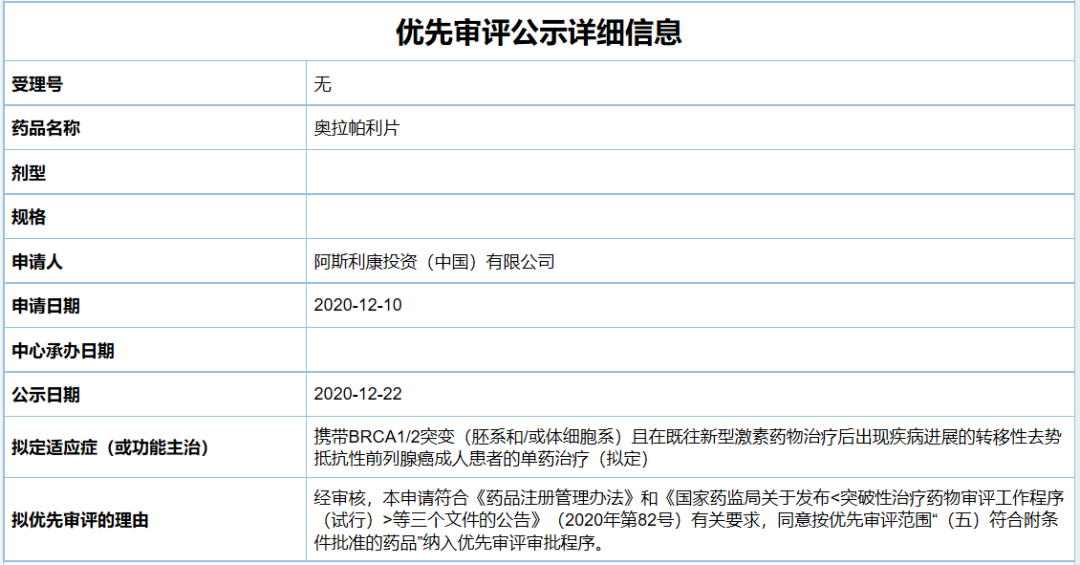
此次奥拉帕利在中国拟纳入优先审评,拟开发适应症为:携带BRCA1/2突变(胚系和/或体细胞系)且在既往新型激素药物治疗后出现疾病进展的转移性去势抵抗性前列腺癌(mCRPC)成人患者的单药治疗(拟定) 。
根据一项名为
PROfound的3期临床试验结果,在携带
BRCA1/2
或
ATM基因
突变(HRR基因突变亚群)的mCRPC患者中,
奥拉帕利
与
阿比特龙或恩杂鲁胺
相比,使患者的总生存期(OS)得到显著的改善,达到了该试验的关键性次要终点。此前公布的试验结果显示,在携带
BRCA1/2
或
ATM
突变的mCRPC患者中,与
阿比特龙或恩杂鲁胺
相比,
奥拉帕利
的治疗使患者的放射学无进展生存期(rPFS)显著延长,达到了试验的主要终点。
在中国,奥拉帕利(中国商品名:利普卓)于2018年8月首次获批,是首个在中国获批上市的卵巢癌靶向新药。2019年11月,奥拉帕利再次获得NMPA批准,用于携带BRCA基因突变的晚期卵巢癌患者的一线维持治疗,这些患者在接受铂基化疗之后获得缓解。
Benralizumab(Fasenra)是阿斯利康开发的一款与嗜酸性粒细胞表面表达的IL-5Rα相结合的单克隆抗体。
通过与IL-5Rα相结合,它能够募集天然杀伤细胞,通过诱发嗜酸性粒细胞的细胞凋亡过程来迅速清除这些细胞。研究表明,选择性抗嗜酸性粒细胞的作用可以减少COPD患者的急性加重率,这种作用在血嗜酸粒细胞基数高的患者中似乎更明显。
此前,benralizumab已于2017年11月被美国FDA批准用于12岁及以上具有嗜酸性表型的重度哮喘患者的附加维持治疗。此外,它还先后在2018年和2019年被FDA分别授予了治疗嗜酸性肉芽肿性多血管炎(EGPA)的孤儿药资格和治疗高嗜酸性粒细胞综合征(HES)的孤儿药资格。
此次benralizumab注射液在中国获批临床,拟开发适应症为慢性阻塞性肺疾病。
慢阻肺是一种进行性疾病,可引起肺部气流阻塞,导致呼吸困难。它影响全球大约3.84亿人,是全球第三大死亡原因。改善肺功能,减少急性加重和管理日常症状是慢阻肺管理中的重要治疗目标。
根据一项名为WINDWARD项目的临床结果,接受8周benralizumab给药方案的重度哮喘患者,肺功能明显改善,1秒用力呼气容积(FEV1)比安慰剂组提高159ml,并且在给药4周后就看到差异,提示起效早。研究表明,benralizumab具有强大的临床表现,包括在第一次给药后显示的改善肺功能的能力,减少甚至停止使用口服类固醇的潜力,以及8周给药的便捷性。
公开资料显示,tezepelumab是安进(Amgen)公司和阿斯利康联合开发的胸腺基质淋巴细胞生成素(TSLP)抑制剂,为一款潜在的“first-in-class”新药,曾获美国FDA突破性疗法认定。TSLP是一种上皮细胞因子,它是包括哮喘在内的各种疾病中多种炎症途径的上游调节子,对气道炎症的发生和持续进行至关重要。研究显示,TSLP在调节T2免疫中很活跃。同时,它也可以通过向多种类型的细胞(如肥大细胞,嗜碱性粒细胞)激活或发出信号,从而在非T2驱动的炎症中发挥作用。
此次tezepelumab注射液在中国获批临床,拟开发适应症为重度慢性鼻窦炎伴鼻息肉(CRSwNP)。
慢性鼻窦炎伴鼻息肉影响了全球高达4%的人群,其特征是在鼻窦或鼻腔的内衬上存在良性炎性息肉(鼻息肉),这可以阻断正常的气流,并且导致鼻塞、流涕、面部疼痛/压迫感和嗅觉减退或丧失等症状。
研究表明,TSLP的表达水平与鼻窦粘膜中Th2细胞因子的表达呈正相关,在人原代鼻粘膜上皮细胞培养中,TSLP可以诱导ST2L的表达。在嗜酸粒细胞性伴鼻息肉的慢性鼻-鼻窦炎中,TSLP及其受体形成的正反馈环和Th2细胞因子可以促进Th2炎症反应的发生发展。因此,针对TSLP的生物制剂有望成为治疗鼻窦炎伴鼻息肉的新选择。
目前,在鼻内皮质类固醇标准治疗之后,手术和全身性皮质类固醇是治疗这种疾病的主要治疗方法。然而,由于鼻息肉的重新生长,随着时间的推移,它们往往不能有效地控制慢性症状。
祝贺阿斯利康奥拉帕利拟纳入优先审评,以及两款新药在中国获批临床,希望这些疗法在中国的临床研究进展顺利,早日为更多中国患者带来新的治疗选择。
版权说明:本文来自药明康德内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。转载授权请在「医药观澜」微信公众号留言联系我们。
欢迎扫码关注“医药观澜”微信公众号,了解更多中国医药创新动态。

参考资料:
[1]中国国家药监局药品审评中心. Retrieved Nov 27,2019, from http://www.cde.org.cn/news.do?method=changePage&pageName=service&frameStr=3
[2] 阿斯利康新药Fasenra 2期结果积极 几乎完全清除致病白细胞. Retrieved April 8,2019, from https://med.sina.com/article_detail_103_2_64050.html
[3]
蒋文中.(2004).气道嗜酸性粒细胞增高与COPD加重.现代临床医学生物工程学杂志,79-81.doi:CNKI:SUN:XDLC.0.2004-01-043.
[4]Tezepelumab Significantly Reduced Asthma Exacerbations For A Broad Population Of Patients With Severe Uncontrolled Asthma. Retrieved September 7, 2018, from https://www.amgen.com/media/news-releases/2017/09/tezepelumab-significantly-reduced-asthma-exacerbations-for-a-broad-population-of-patients-with-severe-uncontrolled-asthma/
[5] 张罗.(2017).展望慢性鼻-鼻窦炎伴鼻息肉的精准治疗.中华耳鼻咽喉头颈外科杂志doi:10.3760/cma.j.issn.1673-0860.2017.02.001.
[6] 廖波. TSLP,IL-33及其受体在嗜酸粒细胞性伴有鼻息肉的慢性鼻—鼻窦炎上皮细胞中的相互作用[D]. 2015.










 个人中心
个人中心
 我是园区
我是园区




