根据医药云端工作室不完全统计,目前已有2682个品规通过一致性评价,303个品规集齐三家以上(含三家)过评
根据医药云端工作室统计,2021年6月20日-2021年6月26日,新增58个品种(视同)通过一致性评价,其中13个为全国首家过评,具体如下:
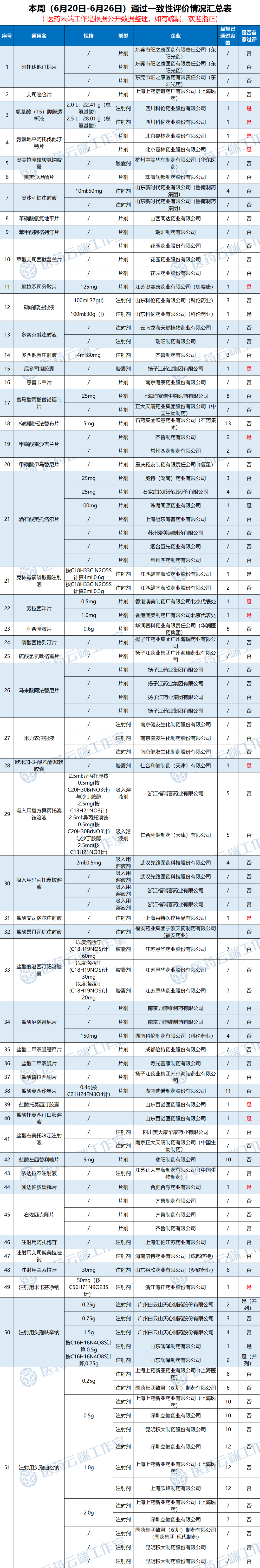
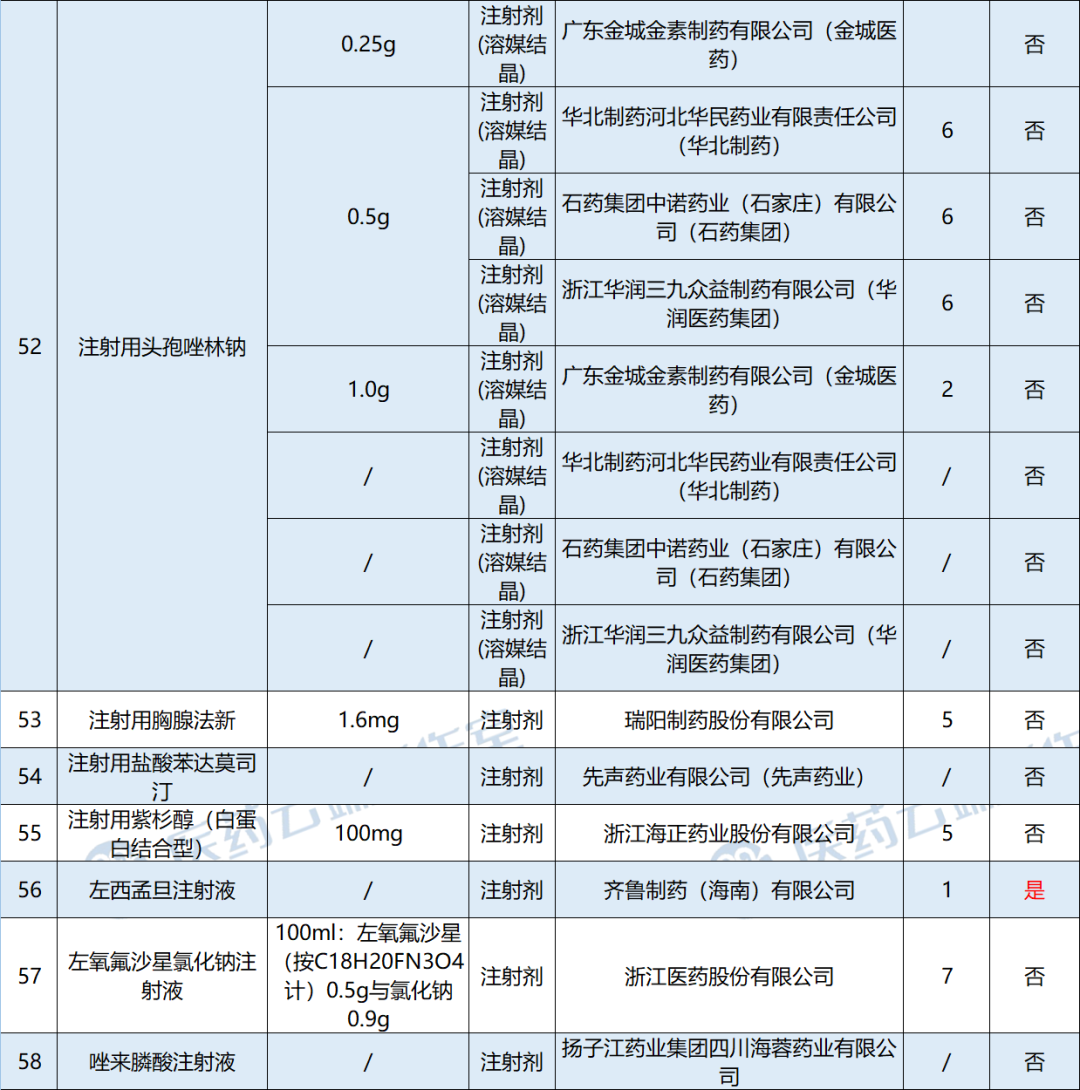
科伦药业:氨基酸(15)腹膜透析液获批视同过评,为全国首家
氨基酸(15)腹膜透析液为百特开发,目前已在英国、意大利、西班牙等多个欧洲国家获批上市,主要用于肾衰竭患者的腹膜透析治疗,尤其适用于营养不良(血清白蛋白低于 35g/L)的慢性肾功能衰竭患者。
氨基酸(15)腹膜透析液为全球唯一含营养成分(多种氨基酸)的腹膜透析液,以氨基酸替代葡萄糖作为渗透剂,可减少对腹膜的损害、纠正钙磷代谢紊乱、改善患者的营养状态,有望为营养不良和糖尿病慢性肾衰竭患者提供更具临床优势的解决方案。
公开数据显示,2020 年中国腹膜透析液销售 42 亿元。
北京嘉林药业:氨氯地平阿托伐他汀钙片获批视同过评,为全国首家
氨氯地平阿托伐他汀钙片兼有降血脂和降血压的功效。目前。仅由美国辉瑞公司获得注册进入中国市场,商品名“多达一”。
据米内网显示,2020年,国内氨氯地平阿托伐他汀钙片终端销售额超过8亿元,其中在中国公立医疗机构终端增速为11.86%,在中国城市实体药店终端增速达4.47%。
奥赛康:地拉罗司分散片获批视同视同过评,为全国首家
地拉罗司是目前治疗铁过载唯一有效的药物。地拉罗司系被 FDA 批准的第一个能够常规使用的口服铁螯合剂,用于治疗 2岁及以上的患者因输血而引起的慢性铁过载,和 10 岁以上非输血依赖性地中海贫血(NTDT)综合征患者的慢性铁过载。
2012 年,地拉罗司在欧盟被批准用于 6岁及以上因频繁输血(红细胞压积≥7ml/kg/月)而导致慢性铁过载地中海贫血患者的治疗。在日本,本品被批准用于治疗因输血引起的铁过载。
地拉罗司分散片被列入了国家卫健委发布的《第一批鼓励仿制药品目录》,也是最新版医保目录品种,2020年全球销售额达 6.53 亿美元;PDB数据库显示,2020年地拉罗司国内样本医院销售额为 1973 万元。
上海百特医疗:盐酸艾司洛尔注射液获批视同视同过评,为全国首家
艾司洛尔属于心血管系统药物选择性的β1肾上腺素受体阻滞剂,常用于心房颤动、心房扑动时控制心室率;围手术期高血压;窦性心动过速。
盐酸艾司洛尔注射液国产批准文号有19个,共10家生产厂家。据重点城市公立医院数据,艾司洛尔2020年销售2.43亿元,同比增长23.92%。齐鲁制药占据高达97.29%的市场,表现优异。
β-受体阻滞剂被广泛的使用在心脑血管及其它疾病领域中,是抗心绞 痛、心衰、心律失常的一线用药,占据着医院用药较大的比例。
艾司洛尔在β-阻滞剂类目中,销售排名第二,以起效快、超短效、高选择著称,2015年被列入了国家出台的《急(抢)救药品直接挂网采购示范药品》。
齐鲁:甲磺酸雷沙吉兰片、左西孟旦注射液全国首家(视同)通过一致性评价
甲磺酸雷沙吉兰片
甲磺酸雷沙吉兰片是一种新型选择性 B 型单胺氧化酶(MAO-B)抑制剂,用于PD治疗疗效明确、顺应性好,还具有潜在的神经保护作用。临床上主要用于原发性帕金森病患者的单药治疗,以及伴有剂末波动患者的联合治疗(与左旋多巴合用)。
该药品是丹麦灵北公司和以色列梯瓦公司共同开发的第二代单胺氧化酶 B (MAO-B) 抑制剂。2005 年 2 月雷沙吉兰在欧盟获批上市,2006 年 5 月获 FDA 批准在美国上市,2017 年 5 月在国内获批进口,商品名为 Azilect(安齐来)。公开资料显示,雷沙吉兰比第一代单胺氧化酶抑制剂司来吉兰功效强 5~10 倍,副作用小且具有一定的神经保护作用。
根据 Insight 数据库,齐鲁的雷沙吉兰片于 2019 年 10 月报产并获受理,2020 年 1 月纳入优先审评审批。目前,除齐鲁外还有常州四药、恩华药业、ALKEM LABS LTD 3 家企业申报;此外江西青森药业和重庆华森制药正处于 BE 试验中。
左西孟旦注射液
雷沙吉兰属于不可逆的MAO-B选择性抑制剂,可增加纹状体细胞外多巴胺水平,临床上适用于原发性帕金森病患者的单一治疗(不用左旋多巴),以及作为左旋多巴的辅助用药用于有剂末波动现象的帕金森患者。
原研产品于2017年6月获批进入国内市场,目前暂无仿制药获批上市。米内网数据显示,该产品在2020年中国公立医疗机构及中国城市实体药店终端合计销售额近5000万元,同比增长328.72%。
目前有3家企业以新注册分类提交甲磺酸雷沙吉兰片上市申请,齐鲁制药的产品首家报产,率先拿下首仿。
山东百诺医药:盐酸托莫西汀胶囊、盐酸托莫西汀口服溶液获批视同视同过评,为全国首家
盐酸托莫西汀原研为礼来制药,2002年在美国上市,适用于治疗儿童和青少年(6岁-18岁)的注意缺陷/多动障碍(ADHD),是FDA唯一批准治疗ADHD的非中枢兴奋剂。
2006年,盐酸托莫西汀胶囊获批在中国上市,口服溶液被国家药监局纳入优先审评并于2018年获批上市。本品是多动症一线治疗用药,是《中国注意缺陷多动障碍防治指南》推荐药物,并被收入2020版《国家医保药品目录》。
米内网数据显示,托莫西汀2020年国内样本医院终端销售额为6577万元,同比增长7.34%,礼来几乎垄断本品全部销售市场,占93.49%,正大丰海有6.51%的市占比。
目前,国内除礼来(原研)、山东百诺(新4类)已获批上市外,还有南京柯菲平(新4类)、合肥合源药业(新4类)、印度瑞迪博士(进口5.2类)在摩拳擦掌,等待通过评审。
扬子江药业集团:厄多司坦胶囊获批视同视同过评,为全国首家
厄多司坦胶囊属粘液溶解剂,用于急性和慢性支气管炎痰液粘稠所致的呼吸道阻塞。
该药原研厂商为意大利FAMAR药业,于1993年在法国上市,2010年7月进口中国。扬子江药业的厄多司坦胶囊为该品种国内首家视同过评的仿制药。
目前,在中国获批生产「厄多司坦」的剂型有胶囊剂、片剂和分散片。其中,胶囊剂为本品的销售大头,占据样本医院市场的77.32%,片剂占22.68%。
海正药业:注射用米卡芬净钠全国首家过评
米卡芬净钠主要用于由曲霉菌和念珠菌引起的下列感染:真菌血症、呼吸道真菌病、胃肠道真菌病。
米卡芬净(Micafungin)由日本安斯泰来制药公司(AstellasPharma Inc)研制开发,首先于2002年10月08日获日本医药品医疗器械综合机构(PMDA)批准上市,然后于2005年3月16日获美国食品药品管理局(FDA)批准上市,之后于2008年4月25日获欧洲药物管理局(EMA)批准上市。
由安斯泰来制药公司在上述各地上市销售,商品名为MYCAMINE®,目前已在全球绝大多数主要国家上市,上市剂型均为注射用冻干粉针剂。该品种于2006年5月12日批准在中国境内上市,商品名米开民®。
目前,注射用米卡芬净钠国内主要生产厂商有江苏豪森药业集团有限公司、四川制药制剂有限公司等。据统计,注射用米卡芬净钠2020年全球销售额约为33,915.26万美元,其中中国销售额约为3,442.73万美元;2021年1-3月全球销售额约为8,263.60万美元,其中中国销售额约为1,181.18万美元(数据来源于IMS数据库)。
据海正药业公告显示,公司注射用米卡芬净钠2020年度销售收入约为3,933万元,2021年1-3月销售收入约为1,252万元。2019 年 1 月 9 日,国家药监局受理了公司递交的注射用米卡芬净钠一致性评价申请。截至目前,公司针对该药品仿制药质量和疗效一致性评价已投入约293.47 万元人民币。
合肥河源:吲达帕胺缓释片获批视同过评,为全国首家
吲达帕胺片为磺胺类利尿剂,具有利尿和钙拮抗作用,是一种强效、长效的降压药,临床上主要用于治疗原发性高血压。
本品最早于1977年12月20日由施维雅开发的在英国批准上市,规格为 2.5mg(以吲达帕胺半水合物计),商品名为Natrilix,后续又批准了缓释片1.5mg 等不同规格。吲达帕胺缓释片为2018版国家基药、2020版国家医保甲类药物。
根据PDB数据库显示,吲达帕胺片2019年在全球销售额为8.68亿美元,同比上涨5.97%。米内网显示,国内样本医院中,2020年吲达帕胺销售额为1639万元,同比下滑19.11%,本品市场由片剂主导,占比高达97.74%,胶囊剂为2.26%。
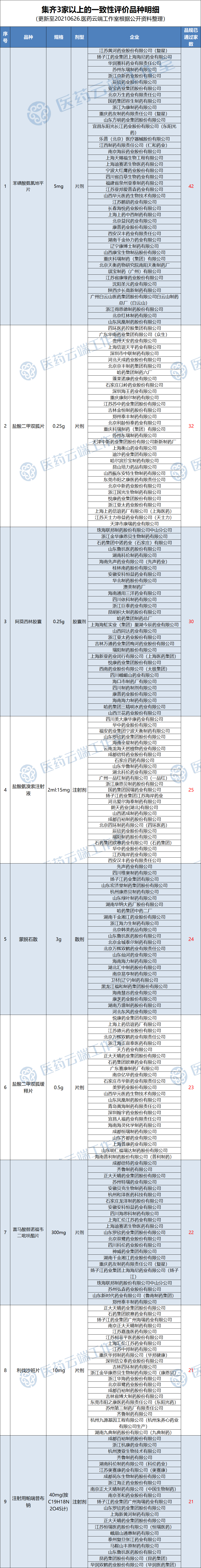
全国最新过评数据通报:
根据医药云端工作室不完全统计,目前已有2682个品规通过一致性评价,303个品规集齐三家以上(含三家)过评。



 个人中心
个人中心
 我是园区
我是园区




