▲点击上方的蓝色“医谷”关注我们
“置顶公众号”获取最有价值行业趋势信息
医谷微信号:yigoonet
据美国证券交易委员会(United States Securities and Exchange Commission,英文简称SEC,以下简称“美国证交会”)官网信息显示,2022年3月30日,计划将百度、富途控股、爱奇艺、凯信远达医药和从事渔业养殖的Nocera加入“有退市风险的清单”。根据美国证交会的说法,这五家公司需要于4月20日前向美国证交会提供证据,证明自己不具备加入名单的条件。若无法证明,则会被列入上述清单。
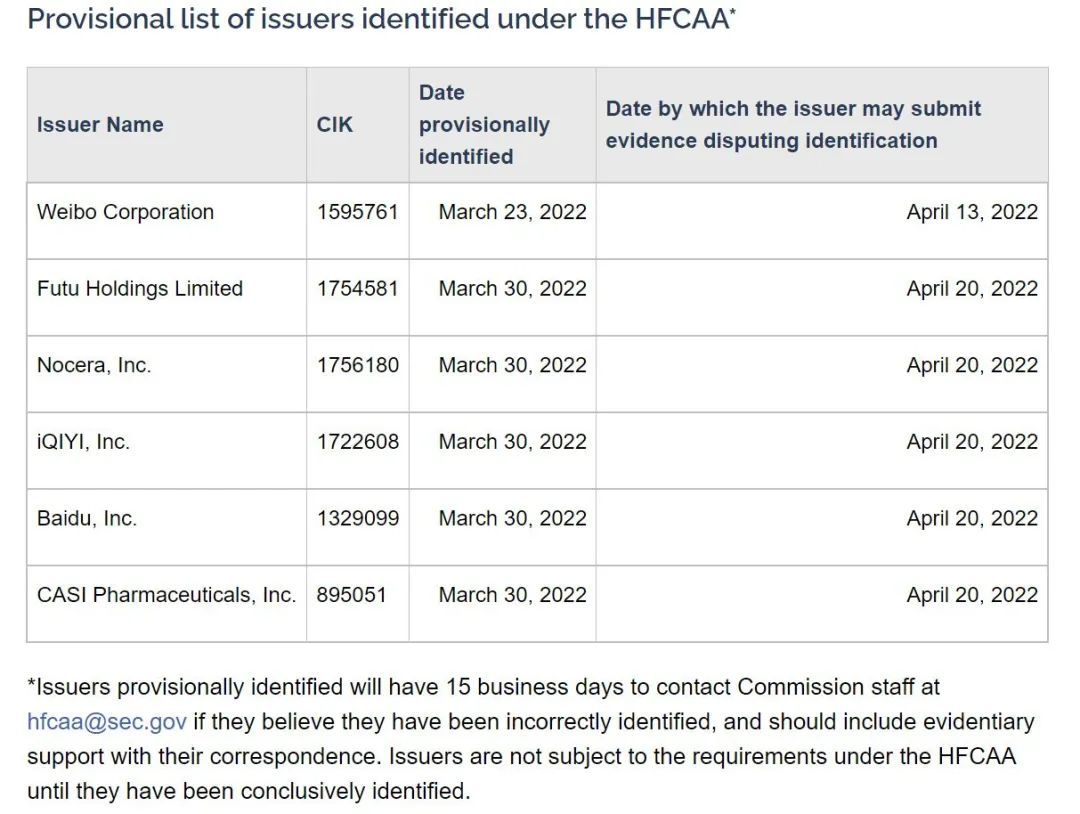
这也是继3月以来又一批计划被纳入名单的中概股。2022年3月8日,5家中国公司被美国证交会计划列入“有退市风险的清单”,其中包括百济神州、再鼎医药、和黄医药三家生物医药企业,百济神州目前在美国纳斯达克、港交所和科创板三地上市,再鼎医药在美国纳斯达克和港交所上市,和黄医药在美国纳斯达克、港交所和英国伦敦AIM市场上市。
美国证交会依持的《外国公司问责法案》
新被计划纳入的凯信远达医药
凯信远达医药官网显示,公司于2012年在美国纳斯达克上市,股票代码为CASI,总部位于美国马里兰州罗克韦尔市,在北京设有全资子公司,在无锡与当地政府设有合资子公司及研发中心。凯信远达医药致力于在血液肿瘤领域为中国患者提供最先进的疾病治疗方案,目前产品及研发管线覆盖了多发性骨髓瘤、B细胞非霍奇金淋巴瘤、急性淋巴细胞白血病等多个疾病领域。
公司董事长兼CEO为何为无博士,其自2012年2月起担任凯信远达医药公司董事会主席,2018年2月起担任董事会执行主席,从2019年起兼任首席执行官,同时其也是ETP基金创始人、合伙人。公司董事会成员还包括IDG、凯鹏华盈的投资代表。
目前,凯信远达医药已有一款上市产品,为迈维宁 (注射用盐酸美法仑),2018年11月经国家药监局批准上市,用于多发性骨髓瘤患者造血干细胞移植前的高剂量预处理治疗,和不适合口服剂型治疗的多发性骨髓瘤患者的姑息治疗。迈维宁也是中国市场上唯一的注射用美法仑产品。截至2021年底,为近6000名患者提供了治疗服务,2021年全年迈维宁销售收入为3000万美元,2020年同期收入为1500万美元。不过,公司整体还处于亏损状态,2021年研发支出为1440万美元,2020年同期为1150万美元。2021年净亏损为3580万美元,2020年同期为4750万美元。截至2021年12月31日,现金及现金等价物合计为3870万美元,而截至2020年12月31日为5710万美元。
除迈维宁外,公司还有CNCT19、BI-1206 (抗FcγRllB抗体)、CB-5339 (VCP/p97 抑制剂)、CID-103 (Anti-CD38 Mab)等产品在研或在合作。
CNCT19为天津合源生物开发的自体抗CD19 CAR-T 细胞治疗产品,2020年,凯信远达医药与合源生物正式签署许可协议,获得其CNCT19项目全球独家商业权益。2022年1月,该款产品获得FDA授予的孤儿药资格认定。
BI-1206 为瑞典生物医药公司 BioInvent International AB 的主要在研产品,2020年10月,凯信远达医药与BioInvent International AB就BI-1206达成临床开发和商业独家许可协议,凯信远达医药获得中国大陆、中国台湾、香港及澳门独家商业权益。BI-1206通过阻断单一抑制性抗体检查点受体FcγRIIB,从而在血液瘤和实体瘤中解锁抗癌免疫力。2021年12月, BI-1206获得国家药监局批准开展I期临床试验,在国外,BI-1206正在进行两项I/II期临床研究:一项是与利妥昔单抗联用,用于治疗复发或难治性非霍奇金淋巴瘤[包括滤泡性淋巴瘤(FL)、套细胞淋巴瘤(MCL)及边缘区淋巴瘤(MZL)];另一项是与抗PD-1药物Keytruda(帕博利珠单抗)联用,用于实体瘤的治疗。2022年1月,BI-1206获得美国食品药品监督管理局(FDA)授予用于治疗一种最常见的惰性非霍奇金淋巴瘤(NHL),滤泡性淋巴瘤(FL)的孤儿药资格认定(ODD)。
CB-5339是一种新型口服二代小分子VCP/p97抑制剂,国内针对复发或难治性多发性骨髓瘤I期临床试验申请已获得国家药监局的受理。Cleave Therapeutics公司负责中国以外地区的CB-5339开发进程,目前针对复发或难治性急性髓性白血病(AML)和骨髓增生异常综合症(MDS)的临床试验正处于I期阶段。
CID-103 是一种全人源IgG1抗CD38单克隆抗体,可识别CD38靶点上的独特表位,目前用于治疗复发或难治性多发性骨髓瘤的I期临床试验 (即剂量递增和剂量扩展试验)正在法国和英国进行。
百济神州、再鼎医药、和黄医药被纳入“有退市风险的清单”
根据美国证交会发布的消息,三家公司需于2022年3月29日前提交相关材料证明不符合被纳入名单的要求,否则,将被纳入“有退市风险的清单”。
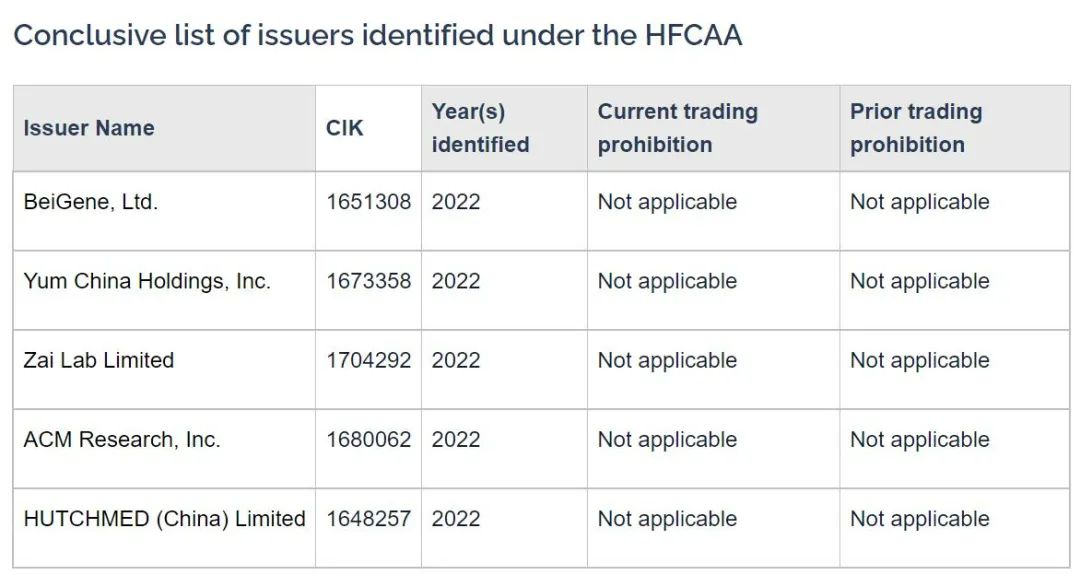
医谷查阅美国证交会官网信息显示,百济神州、再鼎医药、和黄医药三家公司被纳入“有退市风险的清单”(Conclusive list),百度、凯信远达医药目前为(Provisional list)。

针对此,再鼎医药3月28日官网发布《再鼎医药关于美国证券交易委员会(SEC)名单的声明》称,2022年3月8日,根据《外国公司问责法案》(HFCA法案),美国证券交易委员会(SEC)暂时性地认定再鼎医药为使用未经美国公众公司会计监督委员会(PCAOB)审查的审计机构的公司。我们预计,SEC将于2022年3月29日或前后根据HFCA法案对再鼎医药作出最终认定。与SEC之前的暂时性认定一样,这一后续认定也是基于HFCA法案要求进行的常规性操作,在公司的预期中。
这一认定并不意味着再鼎医药将会被SEC从纳斯达克交易所除牌。根据HFCA法案,只有当公司连续三年使用未经PCAOB审查的审计机构,除牌才有可能发生。
我们在2022年3月1日(美国东部时间)发布的2021年度报告中曾披露,我们正在评估、设计和执行额外的业务程序和控制变更,以满足HFCA法案的要求。我们相信这将有望帮助我们满足PCAOB的审查要求,从而在HFCA法案规定的三年(或AHFCA法案规定的两年)期限届满之前,遵守SEC和其他相关要求。
SEC于2022年3月对再鼎医药作出的此次认定不会改变我们相关的立场。

3月31日,和黄医药官网发布《有关状况的更新》消息。消息称于2022年3月30日,诚如美国证券交易委员会(“美国证交会”)根据该法案采纳实施规则后所预期,美国证交会将和黄医药列入其根据该法案认定的发行人最终清单上。
本公司正继续留意市场发展及评估所有的战略选项,并在适当咨询和指导下,本公司谨此指出这一更新对业务营运并无影响。
和黄医药了解该法案的初衷是确保适当的透明度和披露,让投资者能够作出知情的投资决定。我们对此全力支持且亦是我们自2006年在伦敦首次上市以来的一贯承诺。我们将一如既往继续遵守我们上市所在所有司法管辖区的相关法律和法规。
此外,我们正与中国证券监督管理委员会(中国证监会)保持沟通,以了解他们与美国当局就设于中国的公司如何能满足该法案的要求所进行的讨论是否有进一步更新。我们将继续评估保持在美国上市的所有选项,包括在我们的国际业务对集团的贡献超过中国业务时,评估在中国境外委聘审计师的好处。
百济神州方面,针对被纳入“有退市风险的清单”,3月11日,百济神州曾发布公告称,公司一直在积极寻求解决方案,以满足《外国公司问责法案》(HFCAA)的要求,并期待保持公司在纳斯达克市场、香港联合交易所有限公司和上海证券交易所科创板的挂牌。
根据 HFCAA 规定,只有连续三年使用未经美国公众公司会计监督委员会(PCAOB)审查的审计机构,上市公司在纳斯达克市场的挂牌才会受到影响。2022 年 3 月 8 日,公司被美国证券交易监督委员会(SEC)列入基于 HFCAA 的暂时性认定名单。此项认定可能是因为公司于 2022 年 2 月 28 日向 SEC 递交了截至 2021 年 12 月 31 日的年度报告 10-K 表格。
公司认为这份暂时性认定名单是 SEC 采取的行政性措施,表明在这几家公司近期发布了 2021 年度财务业绩报告后,SEC 开始对使用未经 PCAOB 审查的审计机构的公司进行认定。
正如公司此前已经披露的,自 2020 年 12 月 HFCAA 出台后,公司一直在采取积极行动,评估、设计和推进额外的业务流程,以期提早达到相关方的要求,目前相关工作正在积极推进中。
中国证监会回应,列入清单的公司是否在未来两年真正退市,最终取决于中美审计监管合作的进展与结果
3月31日,中国证监会国际部负责人就相关问题回答了记者的提问。中国证监会国际部负责人表示:
我们注意到近日美国SEC主席接受媒体电视采访时就双方审计监管合作的表态。正如根斯勒先生所言,双方监管部门进行了深思熟虑、相互尊重和富有成效的对话。自去年8月以来,中国证监会主席易会满和根斯勒主席已三次召开视频会议,商讨解决中美审计监管合作中的遗留问题。中方与美国公众公司会计监督委员会(PCAOB)更是进行了多轮坦诚、专业和高效的会谈,总体进展顺利,双方的沟通还将继续。双方都有意愿解决分歧和问题,最终结果如何,要看双方的智慧和初心。
此外,对于一些企业被SEC列入有退市风险的清单,经向美国SEC了解,这是美国监管部门执行《外国公司问责法》的一个正常程序,列入清单的公司是否在未来两年真正退市,最终取决于中美审计监管合作的进展与结果。
文 | 医谷






 个人中心
个人中心
 我是园区
我是园区




