Dupilumab 无疑是在 Humira 和K药之后,下一个药王的有力争夺者,在 2022 年销售额达到 83 亿、2023 年将突破 100 亿的情况下,Sanofi 在今年初 JPM 给出的峰值销售指引是 130 亿。
https://www.sanofi.com/dam/jcr:5f231c31-398f-4960-a64d-9ec265fb4fbf/Sanofi_JPM_January_2023.pdf
https://www.sanofi.com/dam/jcr:7b69cea0-7ef9-420b-a9b5-cd43e204929a/2023_02_03_Sanofi_Q4FY_2022_Results_Presentation.pdf
这 130 亿有个重要的前提,是不包括 COPD 预期的,毕竟生物制剂在 COPD 上都尚无胜绩,Dupilumab 在这个疾病领域的前景也备受质疑。如今,这通往药王之巅的最后一扇大门,正在徐徐打开。
3 月 23 日,Regeneron 和 Sanofi 共同宣布(作为脑残粉,笔者偏要引用前者的PR),Dupilumab 治疗 COPD 的三期注册临床试验成功,成为首个证明对该疾病有临床获益的生物制剂。
https://investor.regeneron.com/news-releases/news-release-details/dupixentr-dupilumab-demonstrates-potential-become-first-biologic
在 BOREAS 三期临床试验中(作为两个注册临床之一,代号 BOREAS 和 NOTUS 分别为北风之神和南风之神),共入组 939 例中重度 COPD 患者、且全部为 2 型炎症(每 µL 血中嗜酸性粒细胞数大于 300),试验组使用 Dupi、对照组使用安慰剂,两个组都使用 ICS+LABA+LAMA 的三联标准疗法;Dupi 与安慰剂相比,主要临床终点 52 周时的中重度 COPD 恶化比例降低 30%(p=0.0005),次要临床终点 12 周时肺功能 FEV1 从基线改善幅度为 160 vs 77mL(p<0.0001)且一直延续到 52 周(p=0.0003),不良反应发生率为 77% vs 76%、主要包括头疼、腹泻、背痛等 Dupi 常见副作用。
众所周知,在 2 型炎症疾病治疗药物中,Dupi 抑制 IL-4 和 IL-13 这两条上游通路激活,而还有很多其他机制的免疫调节剂,如靶向 IgE、IL-5、嗜酸性粒细胞相关因子等。
然而过去在 2 型炎症通路上,已经有各种不同机制的生物药在 COPD 领域折戟沉沙,这都让纵然英武如 Dupi 的征途笼罩着阴影,包括靶向 IL-5(R) 的 Benralizumab 和 Mepolizumab(尽管他们在哮喘适应症上效果不错)、靶向 IL-13(R) 的 Lebrikizumab 和 Tralokinumab(这俩是 COPD 和哮喘都失败了)、以及同样靶向 IL-4/13 的 Pitrakinra 和 AMG317 等。

https://www.astrazeneca.com/media-centre/press-releases/2018/update-on-terranova-phase-iii-trial-for-fasenra-in-chronic-obstructive-pulmonary-disease-30052018.html

https://www.gsk.com/en-gb/media/press-releases/gsk-announces-headline-phase-iii-results-of-mepolizumab-in-patients-with-severe-chronic-obstructive-pulmonary-disease/

https://www.roche.com/investors/updates/inv-update-2016-02-29

https://www.astrazeneca.com/media-centre/press-releases/2017/astrazeneca-provides-update-on-tralokinumab-phase-iii-programme-in-severe-uncontrolled-asthma-01112017.html
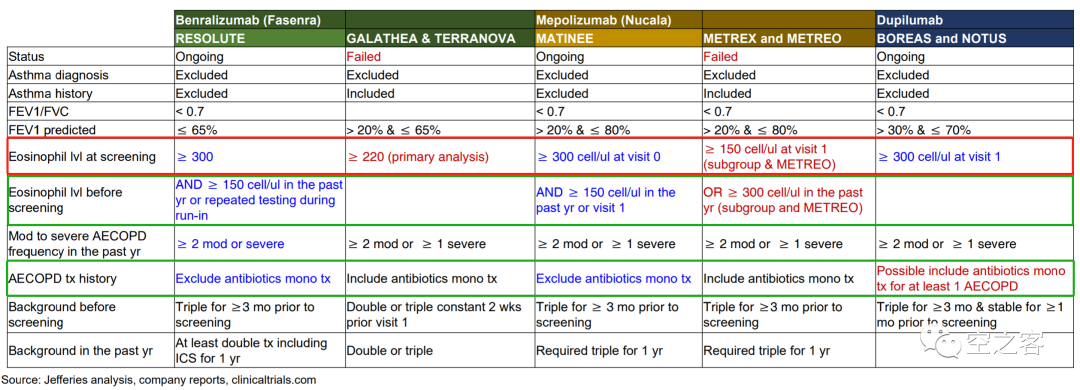
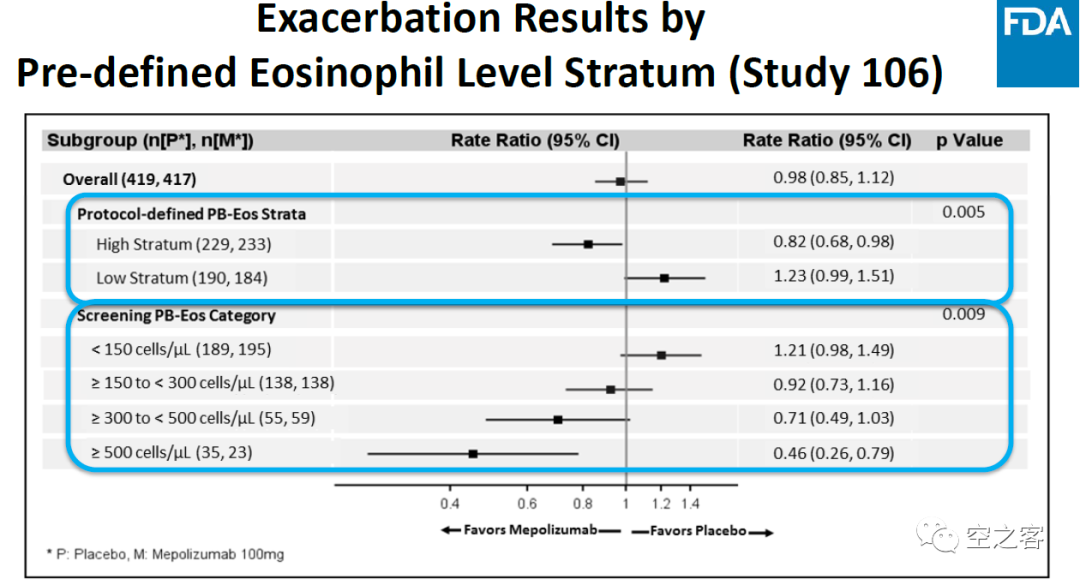
基于这些教训、特别是那俩 IL-5(R) 单抗在 COPD 的失利,Dupi 在临床设计上作出了一定针对性改进,比如在入组标准中明确限制了基线嗜酸性粒细胞 >300 cell/µL,以防此前临床中出现过的 2 型炎症较低的患者响应率偏低的问题;但也仍有一些入排标准受到过质疑,比如未能明确要求嗜酸性粒细胞数量持续保持较高水平、未能排除抗生素经治患者等。
如今「北风」已经横行、「南风」也将刮起,Dupilumab 一只脚迈进了 COPD这 个广阔市场的 Best-in-class 门槛,很有可能将销售额天花板提高到 200 亿美元以上,真正进入下一代「药王」的竞争行列。
免责声明:本文仅作信息分享,不代表 Insight 立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。
投稿:微信 insightxb;邮箱 insight@dxy.cn
点击阅读原文,立刻解锁!




















 个人中心
个人中心
 我是园区
我是园区




