康诺亚SWOT分析:数个靶点领域研发领先,核心产品IL4α抗体进III期 | 研究院
收藏
关键词:
研发
资讯来源:研发客 + 订阅账号
发布时间:
2022-04-19
• 依托自有nTCE双特异性抗体平台、自主抗体发现平台等多个研发平台,开发了IL4α、TSLP、MASP-2等差异化的创新热门靶点。
• 已建有1,600L产能设施,在建产能还将增设16,000L,并有100多名成员规模的商业化团队。
• 2021年实现收入1.1亿元,主要来自于授权许可的合作收入。
近日,康诺亚生物公布港交所上市后第一年的业绩报告。核心产品IL4α抗体CM310分别在慢性鼻窦炎伴鼻息肉和特应性皮炎的II期临床研究均取得了积极成果。
康诺亚生物领导团队实力雄厚。创始人之一的陈博曾是君实生物的创始人兼首席科学家,领导开发首个国产PD-1特瑞普利单抗;王常玉曾是“O药”开发的领导者,徐刚博士曾为罗氏的高级科学家。
公司创立之初就专注自身免疫及肿瘤治疗领域,避开PD-1/L1的红海竞争,依托自有nTCE双特异性抗体平台、自主抗体发现平台等多个研发平台,开发了IL4α、TSLP、MASP-2等差异化的创新热门靶点,建立了覆盖单抗、双抗、ADC多种创新疗法的产品管线。
2021年以来,康诺亚动作迅速,陆续推动了5款自主研发产品进入临床阶段,以满足特应性皮炎、哮喘、慢性鼻窦炎及胃癌等多领域疾病。
同时公司还与石药、诺诚健华、乐普生物等多家企业有授权交易和合作研发。商业化准备方面,康诺亚已建有1,600L产能设施,在建产能还将增设16,000L,并有100多名成员规模的商业化团队,为产品上市推广做准备。
IL4α抗体CM310是康诺亚的核心产品,也是进展最快的产品。首选的适应症是中重度特应性皮炎(AD),在已完成IIb期临床试验中显示出积极疗效。
2021年最新年报显示,CM310已启动治疗AD的III期临床研究,以及成人慢性鼻窦炎伴鼻息肉的II期临床。呼吸系统方面的适应症,康诺亚在2021年3月授权给石药,石药已开始了治疗中重度哮喘的II期临床。公司预计在2023年向国家药监局提交BLA上市申请。
度普利尤单抗是中国乃至全球唯一上市的IL4α抗体,在中国获批治疗AD,其他适应症在III期临床阶段。2021年,度普利尤单抗的全球销售收入同比增长了52.7%,达到了52.49亿美元。成功的销售业绩也吸引了众多国产创新药企进军IL4α领域。
根据2021年11月公布的最新临床数据,CM310在特应性皮炎中展现出不逊于度普利尤单抗的疗效。另一方面,CM310治疗慢性鼻窦炎伴鼻息肉II期临床研究也达到了全部疗效终点,并获得积极结果,两个主要疗效终点16周双侧鼻内镜息肉评分(NPS)、鼻塞评分(NCS)较基线变化均完全达标,CM310组治疗16周NPS和NCS较基线分别降低2.32和1.23,皆显著优于安慰剂组(分别降低0.19和0.30),具备显著的统计学差异。
国内方面,CM310的主要竞争者是康乃德的CBP-201,国外还有阿斯利康的AZD1402处在II期临床。
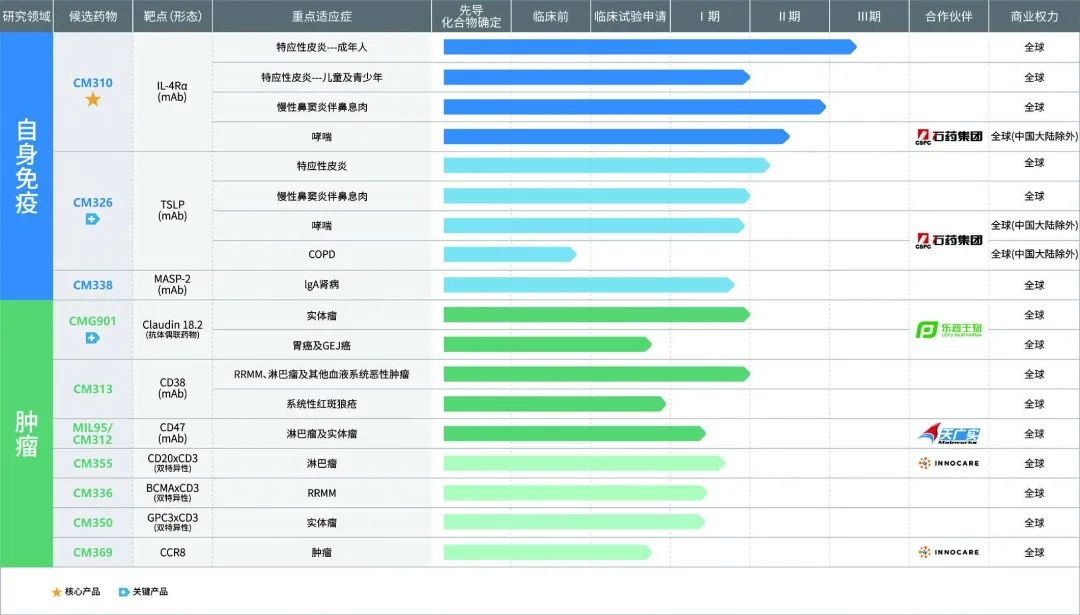
康诺亚的管线有9款在研产品,8个处在临床阶段,其中有5款是国内同领域首个申报IND产品。管线产品差异化避开了PD-1/L1的红海竞争,聚集在TSLP、MASP-2、Claudin 18.2等潜力靶点,虽竞争激烈但研发进展大部分处于行业前列。
CM326是国内首个申报临床的TSLP抗体,是嗜酸性粒细胞依赖性和非依赖性炎性疾病的潜在药物。TSLP是促炎性刺激诱发产生的上皮细胞因子,已被证明在II型炎症中具有多种作用,引发炎症和哮喘的症状。CM326可与TSLP结合,阻断其与受体相互作用,抑制促动II型免疫应答的促炎信号传导,从而控制过敏性疾病。
目前CM326正在开展治疗中重度特应性皮炎和慢性鼻窦炎伴有鼻息肉的Ib/IIa期临床。同竞争领域里,安进/阿斯利康的tezepelumab进展最快,其治疗严重哮喘的III期临床已经达到了治疗终点,可有效降低哮喘恶化率,并在美国提交了BLA申请。
CMG901是管线中唯一一款ADC产品,在中国和美国都是首个获批临床的靶向Claudin 18.2的ADC药物。Claudin 18.2在60%胃癌病例中表达,胰腺癌中的表达率是50%,已成为ADC领域的候选热门靶点之一,国内至少5家企业入局。
另外,康诺亚还有三个处于I期临床阶段的单抗药物,分别是MIL95/CM312(CD47抗体)、CM313(CD38抗体)、CM338(MASP-2抗体)。
其中CM313是首个获得IND批准的CD38抗体,用于治疗复发/难治性多发性骨髓瘤、淋巴瘤及其他血液系统恶性肿瘤。此外,康诺亚还在2022年1月向国家药监局提交了CM313治疗系统性红斑狼疮(SLE)的临床试验申请。
CD47抗体CM312由康诺亚与天广实共同开发,双方分别在中国分摊49%及51%的费用/收入。新型促炎蛋白靶点MASP-2抗体CM338的I期临床在2021年12月启动,用于治疗IgA肾病,是全球第二、中国第一进入临床研究阶段的同靶点药物。
康诺亚的双抗管线包括3款产品,依托新型T细胞重定向(nTCE)平台打造,分别是CM355(CD20xCD3双特异性)、CM336(BCMAxCD3双特异性)和CM350(GPC3xCD3双特异性)。
其中CM336主要用于治疗复发性或难治性多发性骨髓瘤,CM350用于肝细胞癌的治疗,两个产品都已启动了I期临床。CM355是康诺亚与诺诚健华合作开发的产品,2021年10月启动了治疗复发或难治性B细胞非霍奇金淋巴瘤(B-NHL)的I/II期临床试验。
2021年康诺亚与石药三度合作,交易总金额达3.7亿元,涉及康诺亚的2款核心产品。将CM310有关哮喘、慢性阻塞性肺病以及其他呼吸系统适应症在大中华区的权益授权给石药开发,自身保留了AD及慢性鼻窦炎其他适应症。另外康诺亚还保留了CM310全球生产的权利,也就是石药只能开发和商业化CM310,产品的生产和供应将由康诺亚负责。
另一款授权给石药的是TSLP抗体CM326,石药获得在中国(不包括港澳台地区)开发中重度哮喘和慢性阻塞性肺病(COPD)等呼吸系统疾病的授权,并成为上市许可持有人。康诺亚因这笔交易获得1 亿元首付款及1亿元开发里程碑付款。
与大型药企的交易合作,不仅能给康诺亚汇入高额现金流,还能利用对方的成熟销售渠道补充自身的商业推广实力。
另一方面,与合作方成立合资公司的方式也是康诺亚的融资手段之一。公司成立以来,康诺亚相继与诺诚健华和乐普生物成立了两家合资公司,用于CD20xCD3双抗CM355、以及Claudin 18.2靶向ADC产品CMG901的开发和商业化活动,康诺亚基于合资公司的股份获得相应的分成。
在2021年9月,康诺亚和诺诚健华还进一步加深了研发合作。最新年报信息披露了一款两家公司共同开发的在研抗趋化因子受体8(CCR8)单克隆抗体CM369,计划2022第二季度递交临床试验申请。
康诺亚成立于2016年,2021年7月于港交所主板上市。上市前公司共经历过4轮融资,投资者包括高瓴资本、联想之星、汉康资本、礼来亚洲基金及博裕投资等。
公司创始人之一陈博曾是君实生物、华鑫康源生物的创始人,主导研发了中国首个国产PD-1特瑞普利单抗。负责药物发现工作的王常玉副总裁,曾在Chiron、Medarex、百时美施贵宝及瑞辉担任高级研究及管理角色,领导开发了世界首款PD-1抗体“O药”纳武利尤单抗。徐刚博士负责领导公司的药物发现及早期研究,曾为罗氏的高级科学家,是北京协和医学院的免疫学博士。
截止2021年底,康诺亚共有325名员工,临床开发和运行的人员超过120人。2019年至2021年,公司的研发投入0.65亿元、1.27亿元及3.58亿元,2021年研发开支同比增长了181%,增加主要由于雇员薪酬增加1.42亿元、临床试验开支及临床前研究开支增加7660万元所致。
公司在成都、上海及北京都设立了研发中心,其中成都基地拥有总容量达1,600L的生物反应器,分别是三个200L及一个1,000L。另外还将增设16,000L产能(八条2,000L),首条生产线预计在2022年年中试运营。
商业化方面,康诺亚已开始筹备商业化团队,初步有100多名成员组成,负责产品的市场推广。
2021年康诺亚实现收入1.1亿元,主要来自于授权许可的合作收入。2021年经调整后的全面亏损总额达到2.96亿元,同比增长了141%,年报分析主要归因于对研发活动的大量投资。










 个人中心
个人中心
 我是园区
我是园区




