
超重和肥胖的发展趋势在中西方世界中愈演愈烈,而全球(尤其在中国)由肥胖引发的慢性代谢性疾病发病数量逐年攀升,相关社会医疗资源的投入不断增加,造成了严重的公共健康危机和社会经济负担。
脂肪组织是人体内重要的代谢组织,不仅是体内储存能量物质的场所,而且还是重要的内分泌组织(如分泌Adiponectin、Leptin等脂肪因子)、炎症调节和器官保护组织,并在机体物质和能量稳态中起到至关重要的调控作用。小鼠白色脂肪组织重要组分血小板衍生生长因子受体阳性(PDGFR+)血管周围细胞被证实是一类活跃的脂肪前体细胞,一方面可分化成为为脂肪细胞,另一方面可作用于脂肪内免疫细胞而调控脂肪生理和病理微环境的形成,且具有高度的细胞异质性【1】。美国德州大学西南医学中心Rana K. Gupta课题组长期关注脂肪组织功能方面的研究,在前期的研究工作中,利用单细胞转录组测序技术率先在基因表达层面鉴定出不同脂肪组织中脂肪前体细胞的高度异质性:1)腹腔脂肪组织:脂肪前体细胞(APC细胞),和表达高水平炎性、纤维化基因的纤维化/炎性前体细胞(FIP细胞)【2】;2)皮下脂肪组织:脂肪分化能力较强的DPP4阴性(DPP4-)前体细胞和具有免疫调节能力的DPP4阳性(DPP4+)前体细胞【3】。
在后续的研究中,Gupta课题组逐步揭示了脂肪前体细胞亚群存在显著的功能特异性,例如,腹腔脂肪中的FIP细胞不仅能抑制APC细胞向脂肪细胞的分化,而且可以最早感知能量过度摄入并驱动脂肪炎性病理微环境的形成,FIP细胞受高脂饮食喂养激活后,通过产生炎性细胞因子,诱导炎性巨噬细胞浸润和脂肪代谢炎症(详见BioArt报道:Nat Metab | 闪波/邵孟乐等揭示PDGFRβ+细胞在肥胖脂肪组织代谢性炎症中的重要作用)【4】;皮下脂肪中的DPP4+细胞,通过特异性表达IL-33维持了正常状态下脂肪抗炎型免疫微环境,在冷刺激后,交感神经信号激活DPP4+细胞肾上腺素能受体(-AR)信号通路,并通过下游CREB蛋白促进IL-33的表达,进而募集ILC2细胞诱导促脂肪产热免疫微环境的形成,揭示了DPP4+脂肪前体细胞偶联神经和免疫细胞的关键角色(详见BioArt报道:Gene & Dev两篇连发+封面故事 | 邵孟乐/闪波/张倩彬等揭示调控脂肪组织米脂化重要机制)【5】。但是这些脂肪前体细胞亚群的功能差异性及其决定机制,以及这些细胞特性的性别差异,此前并不清楚。
在蛋白质组学研究领域,基于液相色谱-质谱联用 (LC-MS/MS) 的技术是目前应用最广泛的研究手段之一。该类技术中,基于数据依赖采集质谱(data-dependent acquisition mass spectrometry, DDA-MS)模式的发现蛋白质组学使得在样品中检测和相对定量数千个蛋白质成为可能。这种方法的局限性在于重复性差,数据完整性低,同时低丰度蛋白质检测难度大。另一方面,靶向蛋白质组学方法可以对几十到上百个蛋白质提供重复性高,数据完整性高,且灵敏度高的定量,但该方法通量相对较低,难以实现高通量的蛋白质精确定量。近几年发展的数据非依赖性采集质谱(data-independent acquisition mass spectrometry, DIA-MS)技术,结合了传统蛋白质组学技术的高通量和靶向蛋白质组学高重复性,高灵敏度的优点,可以在多个复杂样品中精确定量数千个蛋白质,实现了该领域技术上的突破。在本课题中,该技术首次被成功运用于脂肪前体细胞的研究。
2022年4月20日,日本理化学研究所(RIKEN)蛋白质组学专家伍一博教授,联合Gupta课题组合作在Cell Metabolism杂志上发表了Multilayered omics Reveal Sex- and Depot-dependent Adipose Progenitor Cell Heterogeneity,针对脂肪前体细胞亚群的异质性进行深入研究,在多维度上深入、系统地对雌、雄小鼠内脏和皮下脂肪组织中脂肪前体细胞亚群进行了多组学整合分析,发现并揭示了不同脂肪前体细胞亚群间在基因表达和功能方面的高度差异性及其决定机制。

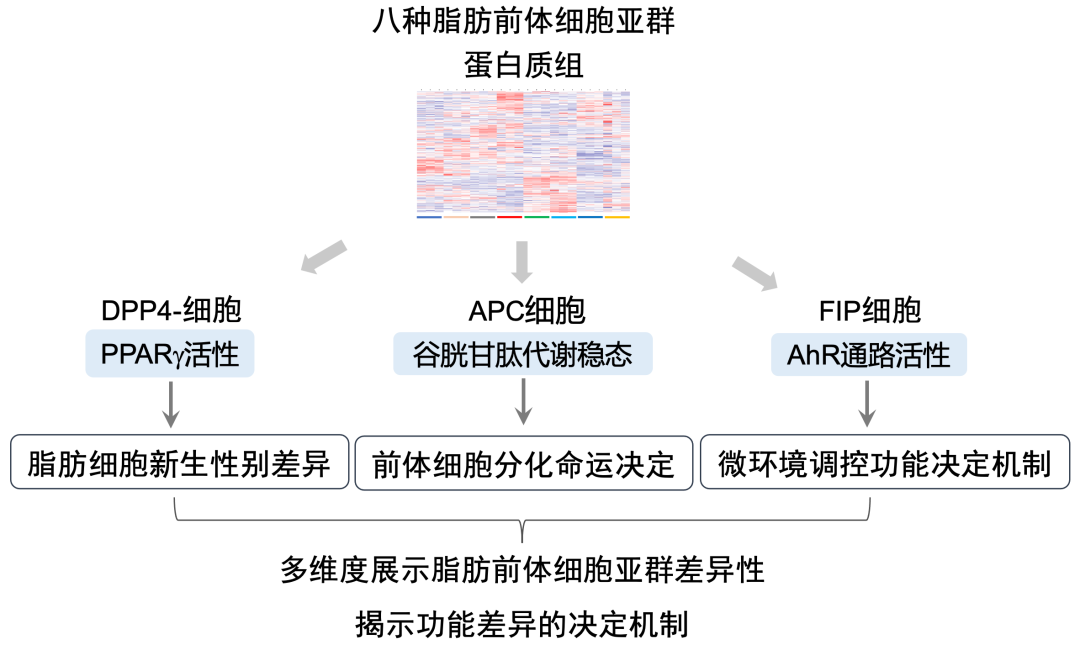
研究人员从决定细胞特性的mRNA和蛋白质两个层面出发,利用流式分选技术分别从从雌、雄小鼠的腹腔和皮下脂肪组织中分离FIP、APC和DPP4-、DPP4+细胞亚群,然后利用DIA-MS技术和RNAseq技术分别的获取上述八种前体细胞亚群的蛋白谱和转录谱,这些数据使得研究人员可以从三个不同维度(性别、细胞类型、组织来源)上全景式比较了各前体细胞亚群的差异性。
虽然蛋白组和转录组数据很大程度上保持了一致性,但是各细胞亚群在蛋白层面上表现的差异性与mRNA层面上又有一定的不同。研究人员通过对蛋白组数据挖掘,预测了脂肪前体细胞亚群功能差异性的决定机制,并结合动物和细胞实验成功地对预测结果进行了验证,主要包括:
1. PPARγ活性依赖的皮下脂肪细胞新生的性别差异;
参考文献
转载须知
【非原创文章】本文著作权归文章作者所有,欢迎个人转发分享,未经作者的允许禁止转载,作者拥有所有法定权利,违者必究。




 个人中心
个人中心
 我是园区
我是园区




